网址:http://m.1010jiajiao.com/timu3_id_303193[举报]
工业生产碘酸钾的流程如下:
(1)已知步骤①反应器发生的反应中,单质碘和氯酸钾的物质的量之比为6:11,则反应器中发生反应的化学方程式为
(2)参照碘酸钾的溶解度:
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100gH2O | 8.08 | 12.6 | 18.3 | 24.8 |
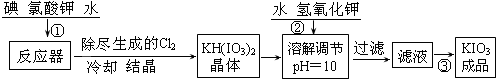
操作③得到碘酸钾晶体,方法是
已知:KIO3+5KI+3H2SO4→3K2SO4+3I2+3H2O;
I2+2S2O32-→2I-+S4O62-.
(3)检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应.用四氯化碳检验碘单质时,看到的明显现象有
(4)测定加碘食盐中碘的含量,学生乙设计的实验步骤如下:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
③以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全.
则加碘食盐样品中的碘元素含量是
(5)学生丙又对纯净的NaCl进行了下列实验:
| 操 作 步 骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡. | 溶液无变化 |
| 然后再滴入1滴1mol/L的H2SO4,振荡. | 溶液变蓝色 |
根据学生丙的实验结果,请对学生乙的实验结果作出简要评价:
加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应.
问题1 工业生产碘酸钾的流程如下:

(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同.请写出反应器中发生反应的化学方程式:______;
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,你建议的方法是______.
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
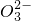 =2I-+S4
=2I-+S4  .
.(1)测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全.则加碘食盐样品中的碘元素含量是______mg/kg(以含w的代数式表示).
(2)学生乙又进行了下列实验:
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡. | 溶液无变化 |
| 然后再滴入1滴1mol/L的H2SO4,振荡. | 溶液变蓝色 |
②根据学生乙的实验结果,请对学生甲的实验结果作出简要评价:______(填“偏大”、“偏小”或“正确”).
其原因是______. 查看习题详情和答案>>
问题1 工业生产碘酸钾的流程如下:
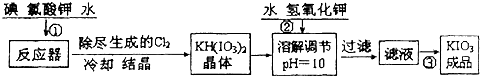
(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同.请写出反应器中发生反应的化学方程式:
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,你建议的方法是
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
| O | 2- 3 |
| O | 2- 6 |
(1)测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全.则加碘食盐样品中的碘元素含量是
| 1270 |
| 3W |
| 1270 |
| 3W |
(2)学生乙又进行了下列实验:
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡. | 溶液无变化 |
| 然后再滴入1滴1mol/L的H2SO4,振荡. | 溶液变蓝色 |
②根据学生乙的实验结果,请对学生甲的实验结果作出简要评价:
其原因是
产品标准 产品等级 配料 碘含量(以Ⅰ计算) 分装日期 分装企业 | GB5461 一级 食盐、碘酸钾、抗结剂 20—50mg/kg 2007.1.25
|
1.上述精制盐属于_________(填“纯净物”或“混合物”)。
2.如果含碘量达到50mg/kg,则精制食盐中碘酸钾的质量分数为___________。
3.配平下列化学方程式。
______KIO3+______KI+______H2SO4![]() ______K2SO4+______I2+______H2O
______K2SO4+______I2+______H2O
(1)反应中作氧化剂的是________;
(2)当溶液中生成0.5 mol I2时,电子转移总数为________________个。
4.已知:I2+2![]()
![]() 2I-+
2I-+![]() 某学生测定食用精盐的碘含量,步骤为:
某学生测定食用精盐的碘含量,步骤为:
a.准确称取W g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3和KI完全反应;
c.以淀粉为指示剂,逐滴加入物质的量浓度为
2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好完全反应。
(1)判断c中反应恰好完全的依据现象是________________;
(2)b中反应所产生的I2的物质的量是________________mol;
(3)计算:根据以上实验和包装袋上的说明所测精制盐的碘含量(以含W的代数式表示)。
查看习题详情和答案>>纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
(1)工业上二氧化钛的制备是: 资料卡片:
物质熔点SiCl4 -70 ℃ 、 TiCl4 -25 ℃;物质沸点SiCl457.6 ℃、TiCl4136.5 ℃
Ⅰ.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4。
Ⅱ.将SiCl4分离,得到纯净的TiCl4。
Ⅲ.在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
Ⅳ.经过滤、水洗除去其中的Cl—,再烘干、焙烧除去水分得到粉体TiO2 。
①在常温下分离TiCl4与SiCl4所采取的操作名称是 ;
②Ⅲ中反应的化学方程式是 ;
③ 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
(2)TiO2粒子的大小可以用现代分析仪器测定,而用氧化还原滴定法可测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。回答下列问题:
①下列可用于测定TiO2粒子大小的方法是_____________________(填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
②配制NH4Fe(SO4)2标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的_____(填字母代号)。

③滴定终点的现象是___________________________________________________。
④滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为_________________________。
⑤若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,对TiO2质量分数测定结果的影响_________________________。(填“偏高”、“偏低”或“无影响”)
查看习题详情和答案>>