摘要:7.已知当△H-T·△S<0时化学反应能自发进行.下列化学反应肯定能自发的是 A.N2(g)+3H2(g)2NH3+2H2O(l) ==2K+(aq)+2OH-(aq) +H2↑ C.2Mg(s)+O2 D.CaCO3+CO2(g)
网址:http://m.1010jiajiao.com/timu3_id_300621[举报]
灰锡结构松散,不能用于制造器皿,而白锡结构坚固,可以制造器皿.现把白锡制成的器皿放在0℃、100kPa的室内存放,它会不会变成灰锡而不能再继续使用(已知在0℃、100kPa条件下白锡转化为灰锡反应的焓变和熵变分别为△H=-2 180.9J?mol-1,△S=-6.6J?mol-1?K-1当△H-T?△S<0时能自发反应)( )
| A、会变 | B、不会变 | C、不能确定 | D、升高温度才会变 |
灰锡结构松散,不能用于制造器皿,而白锡结构坚固,可以用于制造器皿。现把白锡制成的器皿放在0℃、100kPa 的室内存放,它会不会变成灰锡而不能再继续使用(已知在0℃、100kPa条件下白锡转化为灰锡的反应焓变和熵变分别为 △H=-2180.9J.mol-1,△S=-6.61J.mol-1.K-1,当△H- T△S <0时能自发反应)
[ ]
A.会变
B.不会变
C.不能确定
D.升高温度才会变
查看习题详情和答案>>
B.不会变
C.不能确定
D.升高温度才会变
灰锡结构松散,不能用于制造器皿,而白锡结构坚固,可以制造器皿。把白锡制成的器皿放在0 ℃(T = 273K)和1.01×105 Pa的室内保存,它能否变成灰锡(已知:该条件下白锡转化为灰锡的焓变和熵变分别是△H = -2181 kJ·mol-1,△S = -6.61 J·mol-1·K-1;当△H-T△S<0时反应能自发进行)
[ ]
A.不能
B.能
C.不能确定
D.升温后能
查看习题详情和答案>>
B.能
C.不能确定
D.升温后能
能源是人类生存和发展的重要支柱.研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义.已知下列热化学方程式
①2H2(g)+O2(g)=2H2O(l)△H=-570kJ/mol;
②H2(g)+
O2(g)=H2O(g)△H=-242kJ/mol;
③C(s)+
O2(g)=CO(g)△H=-110.5kJ/moL;
④C(s)+O2(g)=CO2(g)△H=-393.5kJ/moL;
⑤CO2(g)+2H2O(g)=2CH4(g)+2O2(g)△H=+890kJ/moL
回答下列问题
(1)H2的燃烧热为 .
(2)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然难直接测定,但可通过间接的方法求得.已知C(s)+H2O(g)=H2(g)+CO(g)△H=akJ/moL;
则a= ;该反应的熵△S 0(选填“>”、“=”、“<”);已知自由能△G=△H-T△S,当△G<0时可自发进行.则该反应在什么条件下可自发进行 .
(3)事实证明,能设计成原电池的反应通常是放热反应.
①下列化学反应在理论上可以设计成原电池的是 .
A.C(s)+H2O(g)=CO(g)+H2(g)△H>0
B.2H2(g)+O2(g)=2H2O(l)△H<0
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H<0
②以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式为 .
(4)有同学利用CuSO4溶液,进行以下实验探究.
①图一是根据反应Zn+CuSO4=Cu+ZnSO4 设计成的锌铜原电池.
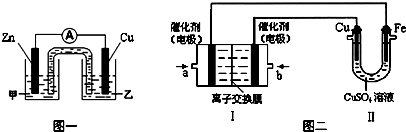
电解质溶液乙是 (填“ZnSO4”或“CuSO4”)溶液;Cu极的电极反应式是 .
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是 (填“CH4”或“O2”),a处电极上发生的电极反应式是 .
查看习题详情和答案>>
①2H2(g)+O2(g)=2H2O(l)△H=-570kJ/mol;
②H2(g)+
| 1 |
| 2 |
③C(s)+
| 1 |
| 2 |
④C(s)+O2(g)=CO2(g)△H=-393.5kJ/moL;
⑤CO2(g)+2H2O(g)=2CH4(g)+2O2(g)△H=+890kJ/moL
回答下列问题
(1)H2的燃烧热为
(2)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然难直接测定,但可通过间接的方法求得.已知C(s)+H2O(g)=H2(g)+CO(g)△H=akJ/moL;
则a=
(3)事实证明,能设计成原电池的反应通常是放热反应.
①下列化学反应在理论上可以设计成原电池的是
A.C(s)+H2O(g)=CO(g)+H2(g)△H>0
B.2H2(g)+O2(g)=2H2O(l)△H<0
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H<0
②以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式为
(4)有同学利用CuSO4溶液,进行以下实验探究.
①图一是根据反应Zn+CuSO4=Cu+ZnSO4 设计成的锌铜原电池.

电解质溶液乙是
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是
(1)为实现废旧印刷线路板综合利用,可用H2O2和稀H2SO4的混合液溶解处理产生的铜粉末,以制备硫酸铜.已知:
①Cu(s)+2H+(aq)+
O2(g)=Cu2+(aq)+H2O(l)△H=-221.45KJ?mol-1
②2H2O2(l)=2H2O(l)+O2(g)△H=-196.46KJ?mol-1
Cu与H2O2和稀H2SO4的混合液反应生成Cu2+和H2O的热化学方程式为
(2)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2(aq)?2(t-BuNO)(aq)
①当(t-BuNO)2的起始浓度为0.50mol/L时,实验测得20℃时的平衡转化率(α)是65%.计算20℃时上述反应的平衡常数K=
②一定温度下恒容容器中,随着(t-BuNO)2的起始浓度增大,其平衡转化率
③实验测得该反应的△H=50.5KJ/mol,该反应的△S
查看习题详情和答案>>
①Cu(s)+2H+(aq)+
| 1 | 2 |
②2H2O2(l)=2H2O(l)+O2(g)△H=-196.46KJ?mol-1
Cu与H2O2和稀H2SO4的混合液反应生成Cu2+和H2O的热化学方程式为
Cu(s)+H2O2 (l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ/mol
Cu(s)+H2O2 (l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ/mol
(离子方程式形式).(2)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2(aq)?2(t-BuNO)(aq)
①当(t-BuNO)2的起始浓度为0.50mol/L时,实验测得20℃时的平衡转化率(α)是65%.计算20℃时上述反应的平衡常数K=
2.4
2.4
(保留小数点后一位有效数字,下同).②一定温度下恒容容器中,随着(t-BuNO)2的起始浓度增大,其平衡转化率
减小
减小
(填“增大”、“不变”或“减小”).已知20℃时该反应在CCl4溶剂中的平衡常数为1.9,若将反应溶剂正庚烷改成CCl4,并保持(t-BuNO)2起始浓度相同,则它在CCl4溶剂中的平衡转化率小于
小于
(填“大于”、“小于”或“等于”)其在正庚烷溶剂中的平衡转化率.③实验测得该反应的△H=50.5KJ/mol,该反应的△S
>
>
0(填“>”、“<”“=”),较高
较高
(填“较高”或“较低”)温度下有利于该反应自发进行.