网址:http://m.1010jiajiao.com/timu3_id_300517[举报]
实验室利用如右图装置进行中和热的测定。回答下列问题:
⑴该图中有两处实验用品未画出,它们是________________、____________________;
⑵在操作正确的前提下提高中和热测定的准确性的关键是:_____________________________________ _
⑶如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将________ (填“偏大”、“偏小”、“不变”)原因是______________________________________
查看习题详情和答案>>选用图中所列仪器和导管组装实验装置。
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
导 管 及 仪 器 |
|
|
|
|
|
|
|
每个橡皮塞上都打了两个孔 | |||||||
(1)气体发生器置于左侧,气体向右方流动,所用仪器与导管依次连接序号为6接______接______接______接______接______。
(2)进行实验时的操作如下(每项进行一次):
①从分液漏斗中逐滴把无水酒精加入烧瓶中,并控制反应速率,酒精加完后关闭活塞;
②在广口瓶中注入适量的水;
③待烧瓶冷却到室温后对量筒读数;
④把定量的V mL酒精无损地倒入分液漏斗中;
⑤检查装置的气密性;
⑥预先将小钠块在二甲苯中熔化成小钠珠,冷却后倒入烧瓶中,塞紧橡皮塞;
⑦估计反应接近完成,用酒精灯对烧瓶略加微热,使反应完成,再撤掉酒精灯。
正确的操作序号是______。
(3)①利用96%的乙醇制无水酒精的方法是 ________________________。
②将小钠块制成小钠珠的目的是 _______________________________。
(4)出现下列情况时,对实验结果的影响怎样?(A. 偏高 B. 偏低 C. 无影响 )
①此反应是放热反应,反应速率太快,使实验结果________________。
②如果无水酒精中混有少量甲醇,使实验结果____________________。
③读数时,如果量筒内的液面高于广口瓶内的液面,使实验结果__________。
(5)如果此实验的数据视作标准状况下的数据,无水乙醇的密度为ρg·cm-3, V mL乙醇反应完全后,量筒内的液面读数为m mL,则乙醇分子中能被取代的氢原子数是________ 。
查看习题详情和答案>>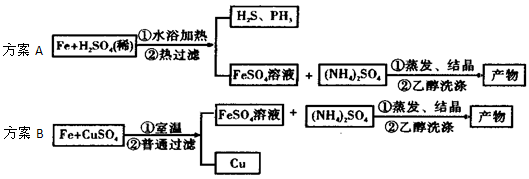
(1)实验前都需将废铁屑放入碳酸钠溶液中煮沸,倾倒出液体,用水洗净铁屑。从以下仪器中选择组装,完成该操作必需的仪器有________ (填编号)。
①铁架台 ②玻璃棒 ③广口瓶 ④石棉网 ⑤烧杯 ⑥漏斗 ⑦酒精灯
(2)方案A中FeSO4溶液的制备:将处理好的铁屑放入锥形瓶,加入过量的3 mol/LH2SO4溶液,加热至充分反应为止。趁热过滤,收集滤液和洗涤液。下右图装置中方框内选择更适合用于实验方案A的装置是__________ (填“甲”或“乙”)。

(4)实验方案B中FeSO4溶液的制备:用“五水硫酸铜结晶水的测定”实验中的废弃物--无水硫酸铜粉末代替稀硫酸与铁屑反应制备硫酸亚铁。当用无水硫酸铜配制的溶液由蓝色完全变为浅绿色时停止反应,过滤,收集滤液即得硫酸亚铁溶液。此方案的优点有_________ (填编号)。
a. 充分利用了实验室废弃物--硫酸铜粉末,避免了药品浪费,又回收了金属铜,实现了变废为宝
b. 避免了有毒气体的排放对环境造成的污染
c. 原子利用率达到100%
d. 避免了在加热中Fe2+被氧化成Fe3+, 有利于产品质量等级的提高,并节约了能源
(5)产品中Fe3+杂质的定量分析
①配制Fe3+浓度为1.0mg/mL的标准溶液100mL。称取_________mg高纯度的硫酸铁铵(NH4)Fe(SO4)2·12H2O,加 2.00 mL经处理的去离子水,振荡溶解后,加入2mol/L HBr 溶液 l m L和 l mol/L KSCN溶液0.5 mL,加水制成100 mL溶液。配制过程中必须用到的定量仪器为________(选填编号)。
a. 精确度为0.001g的电子天平
b.精确度为0.1mg的电子天平
c.100 mL容量瓶
d.酸式滴定管
e.10mL量筒
②将上述溶液稀释为浓度分别为0.2、1.0、3.0、5.0、7.0、10.0(单位:mg/L)的溶液。分别测定不同浓度溶液对光的吸收程度,并将测定结果绘制成曲线如下。



