摘要:量子力学告诉我们:ns能级各有1个轨道.np能级各有3个个轨道.nd能级各有5个轨道.nf能级各有7个个轨道.而每个轨道里最多能容纳2个电子.通常称为电子对.用方向相反的箭头“↑↓ 来表示. 一个原子轨道里最多只能容纳2个电子.而且自旋方向相反.这个原理成为泡利原理. 当电子排布在同一能级的不同轨道时.总是优先单独占据一个轨道而且自旋方向相反 .这个规则是洪特规则. 洪特规则的特例:对于同一个能级.当电子排布为全充满.半充满或全空时.是比较稳定的.
网址:http://m.1010jiajiao.com/timu3_id_298459[举报]
(2010?安徽模拟)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系
(3)请你预测Br与I元素的X数值的大小关系
(4)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于
查看习题详情和答案>>
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是
共价键
共价键
.(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系
元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强)
元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强)
;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系原子半径越小,X的数值越大
原子半径越小,X的数值越大
.(3)请你预测Br与I元素的X数值的大小关系
Br大于I
Br大于I
.(4)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于
N
N
原子(填元素符号).不同元素的原子在分子内吸引电子的能力大小可用x表示,x越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下面是某些短周期元素的x值.
(1)通过分析x值的变化规律,确定Mg、N的x值范围
Mg:
(2)短周期元素x值的变化特点体现了元素性质的
(3)某有机物分子中含有S-N键,你认为电子对偏向
(4)经验规律告诉我们,当成键的两原子相应元素的x差值△x大于l.7时一般形成离子键,△x小于1.7时一般形成共价键,试预测:AlBr3中化学键的类型是
查看习题详情和答案>>

(1)通过分析x值的变化规律,确定Mg、N的x值范围
Mg:
0.93~1.57
0.93~1.57
、N:2.55~3.44
2.55~3.44
.(2)短周期元素x值的变化特点体现了元素性质的
周期性
周期性
变化规律.(3)某有机物分子中含有S-N键,你认为电子对偏向
N
N
原子(填元素符号).(4)经验规律告诉我们,当成键的两原子相应元素的x差值△x大于l.7时一般形成离子键,△x小于1.7时一般形成共价键,试预测:AlBr3中化学键的类型是
共价键
共价键
.设计实验验证你的预测测定熔融状态下是否导电,若不导电则为共价键.
测定熔融状态下是否导电,若不导电则为共价键.
.(1)下表是一些短周期元素的气态原子失去核外不同电子所需的能量(kJ?mol-1):
通过表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量
X在周期表中位置:第
(2)1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念.电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
①上表中电负性最小的元素是
②经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为
查看习题详情和答案>>
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 520 | 580 |
| 失去第二个电子 | 7296 | 4570 | 1820 |
| 失去第三个电子 | 11799 | 6920 | 2750 |
| 失去第四个电子 | 9550 | 11600 |
Li原子失去一个电子后,Li+已经形成了稳定结构,此时再失去电子很困难
Li原子失去一个电子后,Li+已经形成了稳定结构,此时再失去电子很困难
X在周期表中位置:第
三
三
期,ⅡA
ⅡA
族,Y的最高正价为+3
+3
.(2)1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念.电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5] | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
①上表中电负性最小的元素是
K
K
(填元素符号),估计钙元素的电负性的取值范围:0.8
0.8
<X<1.2
1.2
.②经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为
共价键
共价键
,其理由是AlCl3中Cl和Al的电负性差值为1.5,而Br的电负性小于Cl,所以AlBr3中两元素的电负性差值小于1.5
AlCl3中Cl和Al的电负性差值为1.5,而Br的电负性小于Cl,所以AlBr3中两元素的电负性差值小于1.5
.不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在形成的化学键中成为带负电荷的一方,下面是某些短周期元素的x值;
(1)推测x值与原子半径的关系是 ;
(2)某有机化合物结构式为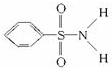 ,其中S-N中,你认为共用电子对偏向 .
,其中S-N中,你认为共用电子对偏向 .
(3)经验规律告诉我们:当成键的两原子相应元素的x差值(△x)即△x>1.7时,一般为离子键,△x<1.7,一般为共价键,试推断:BeCl3中化学键类型是 .
(4)预测元素周期表中x值最小的元素的位置 (放射性元素除外).
查看习题详情和答案>>
| 元素素素素 | Li | Be | B | C | O | F |
| x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 |
| 元素 | Na | Al | Si | P | S | Cl |
| x值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)某有机化合物结构式为
 ,其中S-N中,你认为共用电子对偏向
,其中S-N中,你认为共用电子对偏向(3)经验规律告诉我们:当成键的两原子相应元素的x差值(△x)即△x>1.7时,一般为离子键,△x<1.7,一般为共价键,试推断:BeCl3中化学键类型是
(4)预测元素周期表中x值最小的元素的位置