摘要:12.可逆反应:2A 2C(g),在温度分别为T1.T2.压强分别为 P1.P2的条件下.测得C的百分含量与时间t的关系如图所示,下列判断正确的是 A.P2<P1.逆反应为放热反应 B.P2>P1.正反应为放热反应 C.P2>P1.正反应为吸热反应 D.P2<P1.逆反应为吸热反应
网址:http://m.1010jiajiao.com/timu3_id_297376[举报]
在一定条件下,已达平衡的可逆反应:2A(g)+B(g)  2C(g),下列说法中正确的是( )
2C(g),下列说法中正确的是( )
A.平衡时,此反应的平衡常数K与各物质的浓度有如下关系:K=
B.改变条件后,该反应的平衡常数K一定不变
C.如果改变压强并加入催化剂,平衡常数会随之变化
D.若平衡时增加A和B的浓度,则平衡常数会减小
查看习题详情和答案>>
一定温度下,有可逆反应:2A(g)+2B(g) ![]() C(g)3D(g);
C(g)3D(g);![]()
![]() 学科网
学科网
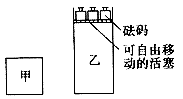
现将2mol A和2 mol B充人体积为V的甲容器,将2mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同。下列说法正确的是![]() 学科网
学科网
![]() 学科网
学科网
A.甲、乙两容器中的反应达到化学平衡时,两容器内压强相等![]() 学科网
学科网
B.甲、乙两容器中的反应达到化学平衡时,C的体积分数相等![]() 学科网
学科网
C.向甲容器中再充人2 molA和2 molB,平衡后甲中物质C的浓度不变![]() 学科网
学科网
D.向乙容器中再充入2 molC和6 molD,平衡后乙中物质C的浓度为原来的2倍![]() 学科网
学科网
等容积的四个密闭容器中,进行同样的可逆反应:2A(g)+B(g)  3C(g)+2D(g),起始时四个容器中A、B的物质的量分别如下表所示(mol),在相同条件下建立平衡,A或B的转化率大小关系为( )
3C(g)+2D(g),起始时四个容器中A、B的物质的量分别如下表所示(mol),在相同条件下建立平衡,A或B的转化率大小关系为( )
|
|
甲 |
乙 |
丙 |
丁 |
|
A |
2 |
1 |
2 |
1 |
|
B |
1 |
1 |
2 |
2 |
A. A的转化率为:甲<丙<乙<丁 B.A的转化率为:甲<乙<丙<丁
C.B的转化率为:甲>丙>乙>丁 D.B的转化率为:甲>乙>丙>丁
查看习题详情和答案>>
 2C(g);△H<0,下列图象正确的是( )
2C(g);△H<0,下列图象正确的是( )
 2C(g) △H <0,下列各图正确的是( )
2C(g) △H <0,下列各图正确的是( )