网址:http://m.1010jiajiao.com/timu3_id_297140[举报]
②B元素原子最外层电子数是次外层电子数的2倍.
③C元素最高正价与最低负价的代数和为2.
④A与D能以原子个数比1:1、2:1形成两种液态化合物.
⑤E2+离子的电子层结构与氖原子相同.
⑥F元素有多种化合价,且常温下F元素的单质与强碱溶液反应,可得到两种含F元素的化合物.
⑦C、F两种元素质子数之和是B元素质子数的4倍.
回答下列问题:
(1)A元素中没有中子的同位素的原子组成符号为




(2)由C、F两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里C、F两种原子最外层均达到8个电子的稳定结构.X遇水蒸气可形成一种常见的漂白性物质.则X的分子式
(3)B、C两种元素可形成一种硬度比金刚石还大的化合物Y.在化合物Y中,B、C两原子以单键相结合,且每个原子的最外层均达到8个电子的稳定结构.则Y的化学式为
(1)A、B、C三种元素的第一电离能由大到小顺序是
(2)D元素基态原子的介电子排布式是
(3)白色晶体白色晶体C3AB4、可由CAB2和C2B2在银皿中于300℃条件下七天后制得,该白色晶体白色晶体C3AB4中阴离子的空间立体构名称是
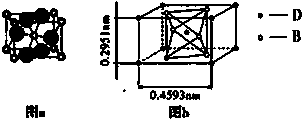
(4)B、D两元素组成的某种化合物的晶体结构(晶胞示意图)如图a、图b所示,写出该化合物的化学式
A、CH4中碳原子的成键轨道的示意图为 | B、氢气的燃烧热为285.8kJ/mol,则表示氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g);△H=-571.6 kJ/mol | C、CH4Si的结构式: | D、氢氧化铁胶体的制备:Fe3++3H2O═Fe(OH)3↓+3H+ |
原子序数由小到大排列的五种短周期元素X、Y、Z、M、W,其中X、Z、M、W四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,元素Y原子的最外层电子数是其电子层数的2倍,Z、M左右相邻,M、W位于同主族。
(1)元素W在周期表中的位置是 。W的阴离子结构示意图是 ;
(2)元素Z的单质的电子式为 。标况下,试管中收集满Z的氢化物,倒立于水中(溶质不扩散),一段时间后,试管内溶液的物质的量浓度为 。
(3)元素Y常见的同素异形体有 。 Y最高价氧化物中的化学键类型为 。Y的氢化物中含氢量最高的物质是常见的燃料,1g该燃料燃烧产生CO2(g)和H2O(l)时放热55.6kJ,试写出表示该燃料燃烧热的热化学反应方程式
。
(4)由X、Z、M、W四种元素中的三种组成的一种强酸,该酸的稀溶液能与铜反应,离子方程式为 。
(5)由X、Z、、M、W和Fe五种元素组成的摩尔质量为392g/ mol的化合物甲,1 mol甲中含有6mol结晶水。对化合物甲进行如下实验:
a.取甲的溶液加入过量的浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取甲的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
①甲的化学式为 。
② 已知100mL 1 mol/L 的甲溶液能与20mL 1 mol/L的酸性KMnO4溶液恰好反应。写出反应的离子方程式 。
查看习题详情和答案>>原子序数由小到大排列的五种短周期元素X、Y、Z、M、W,其中X、Z、M、W四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,元素Y原子的最外层电子数是其电子层数的2倍,Z、M左右相邻,M、W位于同主族。
(1)元素W在周期表中的位置是 。W的阴离子结构示意图是 ;
(2)元素Z的单质的电子式为 。标况下,试管中收集满Z的氢化物,倒立于水中(溶质不扩散),一段时间后,试管内溶液的物质的量浓度为 。
(3)元素Y常见的同素异形体有 。 Y最高价氧化物中的化学键类型为 。Y的氢化物中含氢量最高的物质是常见的燃料,1g该燃料燃烧产生CO2(g)和H2O(l)时放热55.6kJ,试写出表示该燃料燃烧热的热化学反应方程式
。
(4)由X、Z、M、W四种元素中的三种组成的一种强酸,该酸的稀溶液能与铜反应,离子方程式为 。
(5)由X、Z、、M、W和Fe五种元素组成的摩尔质量为392g/ mol的化合物甲,1 mol甲中含有6mol结晶水。对化合物甲进行如下实验:
a.取甲的溶液加入过量的浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取甲的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
①甲的化学式为 。
② 已知100mL 1 mol/L 的甲溶液能与20mL 1 mol/L的酸性KMnO4溶液恰好反应。写出反应的离子方程式 。
查看习题详情和答案>>