网址:http://m.1010jiajiao.com/timu3_id_296621[举报]
(1)M由两种短周期元素组成,每个M分子含有18个电子,其分子球棍模型如图所示。测得M的摩尔质量为32g/mol。画出编号为2的原子结构示意图: 。

(2)已知1.0mol·L—1NaHSO3溶液的pH为3.5,加入氯水,振荡后溶液pH迅速降低。溶液pH降低的原因是 (用离子方程式表示)。
(3)在常温常压和光照条件下,N2在催化剂(TiO2)表面与H2O反应,生成1molNH3和O2时的能量变化值为382.5kJ,达到平衡后此反应NH3生成量与温度的实验数据如下表。则该反应的热化学方程式为 。
|
T/K |
303 |
313 |
323 |
|
NH3生成量/(10—1mol) |
4.3 |
5.9 |
6.0 |
(4)在溶液中,一定浓度的NH4+能溶解部分Mg(OH)2固体,反应如下:
2NH4+(aq) + Mg(OH)2(s)
 Mg2+(aq)
+2NH3·H2O(aq)
Mg2+(aq)
+2NH3·H2O(aq)
写出上述反应的平衡常数表达式
某研究性学习小组为探究Mg2+与NH3·H2O反应形成沉淀的情况,设计如下两组实验
|
实验① |
等体积1 mol/L氨水和0.1 mol/L MgCl2溶液混合 |
生成白色沉淀 |
|
实验② |
等体积0.1 mol/L氨水和1 mol/L MgCl2溶液混合 |
无现象 |
请分析实验①、②产生不同现象的原因: 。
(5)在室温下,化学反应I—(aq)+ ClO—(aq) = IO—(aq) + Cl—(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
|
实验编号 |
I—的初始浓度 (mol·L—1) |
ClO—的初始浓度 (mol·L—1) |
OH—的初始浓度 (mol·L—1) |
初始速率v (mol·L—1· s—1) |
|
1 |
2 × 10—3 |
1.5 × 10—3 |
1.00 |
1.8 × 10—4 |
|
2 |
a |
1.5 × 10—3 |
1.00 |
3.6 × 10—4 |
|
3 |
2 × 10—3 |
3 × 10—3 |
2.00 |
1.8 × 10—4 |
|
4 |
4 × 10—3 |
3 × 10—3 |
1.00 |
7.2 × 10—4 |
已知表中初始反应速率与有关离子浓度关系可以表示为v= k [I—]1 [ClO—]b [OH—]c(温度一定时,k为常数)。
①设计实验2和实验4的目的是 ;
②若实验编号4的其它浓度不变,仅将溶液的酸碱值变更为pH = 13,反应的初始速率v= 。
查看习题详情和答案>>
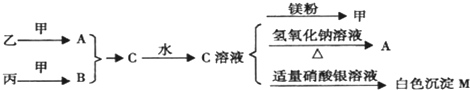
请回答下列问题:
(1)C溶液显
(2)一定条件下,乙气体与甲气体充分反应生成6.8g A气体,可放出18.44KJ热量,则该反应的热化学方程式为
(3)在一定温度下,向容积不变(容积为10L)的密闭容器中加入2mol乙气体、8mol甲气体及固体催化剂.10分钟后反应达到平衡状态,容器内气体压强变为起始的80%,用乙气体表示的反应速率为:
(4)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯、二甲苯等有害物质可转化为二氧化碳和水,达到无害化.有关甲醛、苯、二甲苯、二氧化碳及水说法正确的是
A.苯与B3N3H6互为等电子体,分子中原子共平面,且都有三种二氯代物;
B.二氧化碳、甲醛、氯仿(CHCl3)中碳原子分别采用sp、sp2、sp3杂化;
C.对二甲苯是非极性分子,邻二甲苯和间二甲苯都是极性分子;
D.氨比甲醛易溶于水,是因为甲醛与水分子间不能形成氢键.
(3)日常生活中广泛使用的不锈钢就是含铬合金,铬元素原子中末成对电子数为
(4)①短周期某主族元素M的逐级电离能情况如下图A所示,则M元素形成化合物时,表现的主要化合价为
②第三周期八种元素按单质熔点高低的顺序如下图B所示,其中序号“8”代表

(5)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.科学家把C60和K掺杂在一起制造了一种富勒烯
 化合
化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质的K原子和C60分子的个数比为
(6)在配合物Fe(SCN)2+离子中,提供空轨道接受孤对电子的微粒是
 水的电离平衡曲线如图所示.?
水的电离平衡曲线如图所示.?(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(2)将常温下的pH=8的Ba(OH)2溶液升至100℃,则Ba(OH)2溶液的pH:
A、>10 B、=6 C、6~8 D、>8 E、不能确定
(3)已知AnBm的离子积=[c(Am+)]n?[c(Bn-)]m?,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度幂.在某温度下,Ca(OH)2的浓度为0.02mol?L-1,其离子积为
 (2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
(2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:第1步:取适量碳酸钠溶解于一定量水中,倒入烧瓶中;再加入少量稳定剂(MgCl2和Na2SiO3),搅拌均匀.
第2步:将适量30%的H2O2溶液在搅拌状态下滴入烧瓶中,于15℃左右反应1h.
第3步:反应完毕后再加入适量无水乙醇,静置、结晶,过滤、干燥得产品.
(1)第1步中,稳定剂与水反应生成2种常见的难溶物,其化学方程式为
(2)第2步中,反应保持为15℃左右可采取的措施是
(3)第3步中,无水乙醇的作用是
(4)H2O2的含量可衡量产品的优劣.现称取m g(约0.5g)样品,用新煮沸过的蒸馏水配制成250mL溶液,取25.0mL于锥形瓶中,先用稀硫酸酸化,再用c mol?L-1 KMnO4溶液滴定至终点.
①配制250mL溶液所需的玻璃仪器有烧杯、玻璃棒、量筒、
②滴定终点观察到的现象是
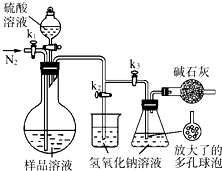
(5)可模拟用蒸馏法测定样品中碳酸钠的含量.装置如图所示(加热和固定装置已略去),实验步骤如下:
步骤1:按右图所示组装仪器,检查装置气密性.
步骤2:准确量取(4)中所配溶液50mL于烧瓶中.
步骤3:准确量取40.00mL约0.2mol?NaOH溶液2份,分别注入烧杯和锥形瓶中.
步骤4:打开活塞k1、k2,关闭活塞k3,缓缓通入氮气一段时间后,关闭k1、k2,打开k3;经滴液漏斗向烧瓶中加入10mL 3mol?硫酸溶液.
步骤5:加热至烧瓶中的液体沸腾,蒸馏,并保持一段时间.
步骤6:经k1再缓缓通入氮气一段时间.
步骤7:向锥形瓶中加入酸碱指示剂,用c1 mol?H2SO4标准溶液滴定至终点,消耗H2SO4标准溶液V1 mL.
步骤8:将实验步骤1~7重复2次.
①步骤3中,准确移取40.00mL NaOH溶液所需要使用的仪器是
②步骤1~7中,确保生成的二氧化碳被氢氧化钠溶液完全吸收的实验步骤是
③为获得样品中碳酸钠的含量,还需补充的实验是