网址:http://m.1010jiajiao.com/timu3_id_296525[举报]
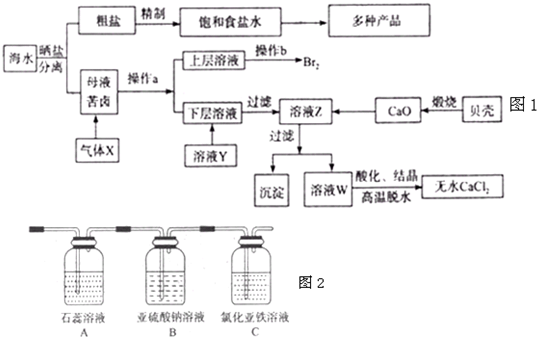
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,梢制时所用的试剂为:A.盐酸B.氯化钡溶 液C.氢氧化钠溶液D.碳酸钠溶液,则加入试剂的顺序是(填编号)
(2)气体X的化学式为
(3)加入溶液Y的目的是
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |
①通入气体X后,A中出现的现象是
②C装置中发生反应的离子方程式为
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤)
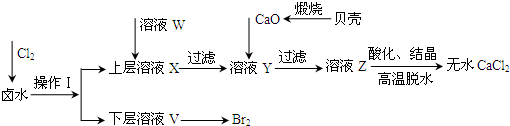
(1)操作Ⅰ使用的试剂是
(2)加入溶液W的目的是
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |
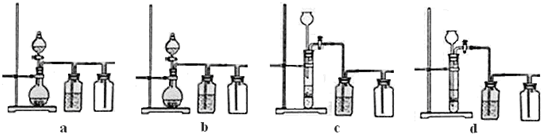
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11.某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3.该实验设计不正确,错误在于
设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论).
方案一:配制相同物质的量浓度的NaHSO3和NaHCO3溶液.用酸度计(或pH试纸)测两溶液的pH.前者的pH小于后者,证明H2SO3酸性强于H2CO3.
方案二:将SO2气体依次通过NaHCO3(或Na2CO3)溶液、酸性KMnO4溶液、品红溶液、澄清石灰水.品红溶液不褪色,且澄清石灰水变浑浊,证明H2SO3酸性强于H2CO3.
方案三:将CO2气体依次通过NaHSO3(或Na2SO3)溶液、品红溶液.品红溶液不褪色,证明H2SO3酸性强于H2CO3
方案一:配制相同物质的量浓度的NaHSO3和NaHCO3溶液.用酸度计(或pH试纸)测两溶液的pH.前者的pH小于后者,证明H2SO3酸性强于H2CO3.
方案二:将SO2气体依次通过NaHCO3(或Na2CO3)溶液、酸性KMnO4溶液、品红溶液、澄清石灰水.品红溶液不褪色,且澄清石灰水变浑浊,证明H2SO3酸性强于H2CO3.
方案三:将CO2气体依次通过NaHSO3(或Na2SO3)溶液、品红溶液.品红溶液不褪色,证明H2SO3酸性强于H2CO3
仪器自选.
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸.
(12分)Ⅰ、(1)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵,则①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(2)已知某温度下,纯水中的C(H+)=5×10-7mol/L,则此时溶液的C(OH-)为 mol/L;若温度不变,将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= 。
Ⅱ、在一个容积固定的密闭容器中,要求通过调节体系的温度使反应A(g)+2B(g) 2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
⑴若x=5.5时,需要降低体系温度使反应在平衡时达到题设条件,则正反应是 热反应。
⑵欲使反应维持向逆反应方向移动,则x的取值范围为 。
⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g) 2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为
(用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为
(用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
查看习题详情和答案>>
(共12分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2按1:1正好完全反应,则反应方程式为 。
(2)上述反应中的还原剂是 ,为了防止大气污染,反应产生的气体可用 吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++ 10 NO-3 = 2H3AsO4+3S↓+10NO2↑+ 2H2O
若生成1mol NO2 ,则反应中转移的电子数为 。若将该反应设计成一原电池,则NO2应该在 (填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 (选填编号)。
a.等于0.5mol b.小于0.5 mol c.大于0.5mol d.无法确定
查看习题详情和答案>>
12分)已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| |温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时c(A)=
mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ,如果这时将该密闭容器体积扩大1倍,则反应速率的变化是 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变
b.气体的密度不随时间改变
c. c(A)不随时问改变
d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g)
 A(g)+B(g)的平衡常数值是 。若
A(g)+B(g)的平衡常数值是 。若此时给反应体系升温,(其他条件不变)则该平衡常数将 _____________ 。(填增大或减小或不变) 查看习题详情和答案>>