摘要:2.已知在101kPa.25℃条件下.1mol氢气燃烧生成水蒸气放出242kJ热量.下列热化学方程式正确的是 A.H2(g)+ O2(g)=H2O(g) ΔH=+242kJ•mol-1 B.2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ•mol-1 C.H2(g)+ O2(g)=H2O(l) ΔH=-242kJ•mol-1 D.2H2(g)+O2(g)=2H2O(g) ΔH=-242kJ•mol-1
网址:http://m.1010jiajiao.com/timu3_id_295882[举报]
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),图1表示该反应进行过程中能量的变化.
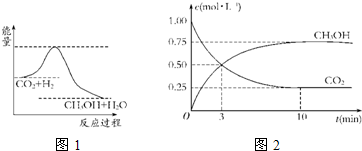
(1)关于该反应的下列说法中,正确的是
A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0.
(2)该图中能量的最高点和最低点之间的差值代表
(3)为探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1mol CO2
和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡用氢气浓度变化表示的平均反应速率v(H2)
(4)肼(N2H4)是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是:
查看习题详情和答案>>

(1)关于该反应的下列说法中,正确的是
C
C
.A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0.
(2)该图中能量的最高点和最低点之间的差值代表
逆反应的活化能
逆反应的活化能
(3)为探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1mol CO2
和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡用氢气浓度变化表示的平均反应速率v(H2)
0.225
0.225
mol?L-1?min-1.(4)肼(N2H4)是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是:
N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol
.SO2和O2是在催化剂表面上接触时发生反应的,所以这种生产硫酸的方法叫接触法,接触法制硫酸的工艺中SO2的转化率为90%,已知在101kPa 时每l mol SO2被氧化成l mol SO3放出热量98.3kJ,则下列热化学方程式正确的是( )
 硫酸生产过程中关键阶段的反应为:
硫酸生产过程中关键阶段的反应为:2SO2(g)+O2(g)
| 催化剂 | 加热 |
(1)能判断该反应达到化学平衡状态的依据是
A.容器中气体密度保持不变
B.混合气体中c(SO3)不再发生变化
C.2v正(SO2)═v逆(O2)
D.c(SO2)═c(SO3)
(2)反应达到平衡时,测得SO3的体积分数为40.0%,则SO2的转化率为
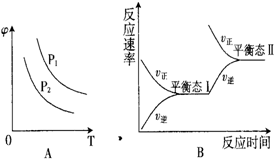
(3)如图A为在不同温度、不同压强下达到平衡时,混合气体中SO3的体积分数φ随度变化的曲线.图B为恒温下平衡态I到平衡态Ⅱ的变化,下列说法正确的是
A.图A中P1>P2
B.图A中P1<P2
C.图B为减小体系压强,平衡发生移动,达到平衡态Ⅱ
D.图B为增大反应物浓度,平衡发生移动,达到平衡态Ⅱ
(4)我国工业制备SO2常用煅烧FeS2方法,而有的国家用燃烧S制备SO2.已知在101kPa时,4g硫粉在氧气中完全燃烧生成SO2,放出27kJ的热量,硫的燃烧热为
 2C(g),若容器体积不变,下列措施可以增加C的产率的是( )
2C(g),若容器体积不变,下列措施可以增加C的产率的是( )