摘要:将除去氧化镁的条投入到盛有溶液的试管中.发现发生的速率变化如右图所示.其中时间段速率变化的主要原因是 .段速率变化的主要原因是 .
网址:http://m.1010jiajiao.com/timu3_id_294626[举报]
某同学设计了一套实验方案研究第11-18号部分元素的性质变化
(1)指出②中的实验现象:
(2)实验Ⅰ的设计中能达到实验目的实验项目是
(3)写出③中发生反应的离子方程式:
(4)④中密封油H2S的玻璃管加热后出现黄色固体,分析产生这种现象的原因是:
查看习题详情和答案>>
| 实验 | 实验目的 | 实验内容 |
| Ⅰ | 探究Mg、Al的金属性强弱 | 1将除去氧化膜的镁条和铝条分别投入稀盐酸中 2将除去氧化膜的镁条和铝条分别放入试管中,加入 少量水,加热至沸腾,再向溶液中滴加酚酞溶液 3向MgCl2和AlCl3溶液中分别加氨水至过量 |
| Ⅱ | 探究Cl、S的非金属性强弱 | ④分别加热密封于玻璃管中的H2S和HCl气体 |
镁条和铝条表面均有气泡产生,且溶液变红
镁条和铝条表面均有气泡产生,且溶液变红
(2)实验Ⅰ的设计中能达到实验目的实验项目是
①②
①②
(填序号)(3)写出③中发生反应的离子方程式:
Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+
Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+
、Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
(4)④中密封油H2S的玻璃管加热后出现黄色固体,分析产生这种现象的原因是:
H2S不稳定,加热分解成H2和S,S为黄色固体
H2S不稳定,加热分解成H2和S,S为黄色固体
.密封有HCl的玻璃管无明显现象.该实验说明非金属性:S弱于
弱于
Cl(填“强于”或“弱于”)将除去氧化膜的镁条投入到盛有稀盐酸的试管中,产生H2的速率变化情况如下图所示。

图中t1~t2速率变化的主要原因是??????????????______ ____ _,t2~t3速率变化的主要原因是 _。
查看习题详情和答案>>(10分)某同学做同周期元素性质递变规律实验时,设计了一套实验方案,并记录了有关实验现象(见下表,表中左右的“实验方案”与“实验现象”不一定是对应关系)。
| 实验方案 | 实验现象 |
| ①镁条除去氧化膜后,放入试管中,加入少量水,加热至沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将除去氧化膜的镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将除去氧化膜的铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
(1)实验目的:研究第3周期元素性质的递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH
溶液,酚酞溶液等。
仪器:砂纸,试管,试管夹,① ,火柴,胶头滴管,烧杯,镊子,小刀,玻璃片,
② 等。
(3)实验内容:
| 实验方案 | ② | ④ | ⑥ |
| 实验现象(填A~F) | | | |
①的化学方程式 ,
②的离子方程式 。
(4)实验结论: 。 查看习题详情和答案>>
 将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是( )
将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是( )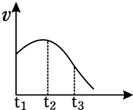 将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是( )
将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是( )