网址:http://m.1010jiajiao.com/timu3_id_288355[举报]
(13分)物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识的回答:
(1)A为0.1 mol•L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为 。
(2)B为0.1 mol•L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(共3个,分别用离子方程式表示): ;实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因: 。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入 ,目的是 ;若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为 。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:
AgCl(s)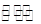 Ag+(aq)+Cl-(aq), 在25℃时,AgCl的Ksp=1.8×10-10
Ag+(aq)+Cl-(aq), 在25℃时,AgCl的Ksp=1.8×10-10
25oC时,现将足量AgCl分别放入:①l00mL蒸馏水;②l00mL 0.2 mol•L-1AgNO3溶液;③100mL 0.1 mol•L-1氯化铝溶液;④100mL 0.1 mol•L-1盐酸溶液。充分搅拌后,相同温度下Ag+浓度由大到小的顺序是 (填写序号);②中C1-的浓度为 _ mol•L-1。
查看习题详情和答案>>
(13分)物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识的回答:
(1)A为0.1 mol•L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为 。
(2)B为0.1 mol•L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(共3个,分别用离子方程式表示): ;实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因: 。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入 ,目的是 ;若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为 。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:
AgCl(s)![]() Ag+(aq)+Cl-(aq), 在25℃时,AgCl的Ksp=1.8×10-10
Ag+(aq)+Cl-(aq), 在25℃时,AgCl的Ksp=1.8×10-10
25oC时,现将足量AgCl分别放入:①l00mL蒸馏水;②l00mL 0.2 mol•L-1AgNO3溶液;③100mL 0.1 mol•L-1氯化铝溶液;④100mL 0.1 mol•L-1盐酸溶液。充分搅拌后,相同温度下Ag+浓度由大到小的顺序是 (填写序号);②中C1-的浓度为 _mol•L-1。
查看习题详情和答案>>

其操作步骤是:
加热前,由A向B先通入足够的空气,并准确称量B、C、D的质量;充分加热后,再由A向装置通入足够空气至B恢复到常温,再分别准确称量 B、C、D的质量;
| 装置质量(含药品) | m(B) | m(C) | m(D) |
| 加热前 | b1 | c1 | d1 |
| 加热后 | b2 | c2 | d2 |
(1)探究沉淀成分前,须将沉淀从溶液中分离并净化.其三个主要的操作步骤依次为:
(2)装置A中碱石灰的作用是
(3)分析b1、c1、d1、b2、c2、d26个数据间的关系,以此位依据,可以判断出沉淀的成分.
| 沉淀成分 | 可作判断的依据一 | 可作判断依据二 |
| 只是CuCO3 | ||
| 只是Cu(OH)2 | ||
| 是CuCO3和Cu(OH)2的混合物 |

(1)该反应的化学平衡常数表达式为K=
| c2(C) |
| c(A)×c(B) |
| c2(C) |
| c(A)×c(B) |
(2)若25min、35min时的化学平衡常数分别为K1、K2,则二者的大小关系是
(3)在甲、乙、丙三个相同的密闭容器中按表中所述投料,在恒温、恒容的条件下进行反应,平衡后测得A的浓度如表中所示:
| 容器 | 甲 | 乙 | 丙 |
| 起始投料 | 1molA和1molB | 2molC | 2molA和2molB |
| A的平衡浓度 | C1 | C2 | C3 |

(1)该反应的化学平衡常数表达式为K= (x要算出具体的数字).在该条件下,当v(B)正:v(C)逆= 时反应达到了化学平衡状态.
(2)若25min、35min时的化学平衡常数分别为K1、K2,则二者的大小关系是 .
(3)在甲、乙、丙三个相同的密闭容器中按表中所述投料,在恒温、恒容的条件下进行反应,平衡后测得A的浓度如表中所示:
| 容器 | 甲 | 乙 | 丙 |
| 起始投料 | 1molA和1molB | 2molC | 2molA和2molB |
| A的平衡浓度 | C1 | C2 | C3 |