摘要:9.改变以下反应条件能提高反应物活化分子百分率的是①温度②浓度③压强④正催化剂 A.①④ B.②③ C.①② D.③④
网址:http://m.1010jiajiao.com/timu3_id_288277[举报]
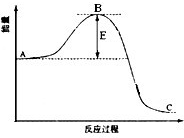 合成氨反应过程中的能量变化如图所示,据图回答下列问题:
合成氨反应过程中的能量变化如图所示,据图回答下列问题:(1)该反应通常用活性铁作催化剂,加活性铁会使图中B点
降低
降低
(填升高、降低或不变),理由是因为催化剂改变了反应的历程使活化能E降低
因为催化剂改变了反应的历程使活化能E降低
;(2)该反应平衡常数表达式为:K=
| [NH3]2 |
| [N2][H2]3 |
| [NH3]2 |
| [N2][H2]3 |
<
<
K(填“<”、“>”或“=”)时,反应向右进行.(3)450℃时该反应的平衡常数
>
>
500℃时的平衡常数(填“<”、“>”或“=”).(4)一定条件下的密闭容器中,该反应达到平衡,要提高H2的转化率,可以采取的措施是
ce
ce
(填字母代号).a.高温高压 b.加入催化剂 c.增加N2的浓度
d.增加H2的浓度 e.分离出NH3
(5)在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol?L-1) | c1 | c2 | c3 |
| 反应物转化率 | a1 | a2 | a3 |
BC
BC
.A.c1<c2 B.2c1<c3 C.a1+a2=1 D. a2<a3.