网址:http://m.1010jiajiao.com/timu3_id_287994[举报]
(7分)已知: A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平的标志。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
回答下列问题:
(1)B、D分子中官能团名称分别是 、 。
(2)写出下列反应的反应类型:① 反应,
②  反应,④ 反应。
反应,④ 反应。
(3)写出下列反应的化学方程式:
③  ;④
;④
(7分)已知: A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平的标志。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
回答下列问题:
(1)B、D分子中官能团名称分别是 、 。
(2)写出下列反应的反应类型:① 反应,
② 反应,④ 反应。
(3)写出下列反应的化学方程式:
③ ;④
查看习题详情和答案>>
(7分)已知: A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平的标志。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。

回答下列问题:
(1)B、D分子中官能团名称分别是 、 。
(2)写出下列反应的反应类型:① 反应,
② 反应,④ 反应。
(3)写出下列反应的化学方程式:
③ ;④
查看习题详情和答案>>
(7分)火箭推进器中盛有强还原剂液态胼(N H
H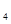 凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
(1)反应的热化学方程式为 。
(2)又已知H 0(I)=H
0(I)=H 0(g);△H=+44 kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是
KJ。
0(g);△H=+44 kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是
KJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
(4)已知N (g)+2O
(g)+2O (g)=2N0
(g)=2N0 (g)
△H=+67.7kJ/mol
(g)
△H=+67.7kJ/mol
N H
H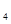 (g)+0
(g)+0 (g)=N
(g)=N (g)+2H
(g)+2H 0(g)
△H=-534kJ/mol
0(g)
△H=-534kJ/mol
则肼与N0 完全反应生成氮气和液态水的热化学方程式为
完全反应生成氮气和液态水的热化学方程式为
查看习题详情和答案>>