摘要:11下列反应中.有机物被氧化的是: A. 葡萄糖发生银镜反应 B. 乙醛制乙醇 C. 乙醛制乙酸 D. 乙酸和碳酸钠反应12.在化学反应中.如果某元素由化合态变为游离态.则该元素 A. 被氧化 B. 被还原 C. 可能被氧化.也可能被还原 D. 化合价降为零价
网址:http://m.1010jiajiao.com/timu3_id_279935[举报]
(2010?南通模拟)利用焦炭或天然气制取廉价的CO和H2,再用于有机合成是目前工业生产的重要途径.回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O═CO+3H2.部分物质的燃烧热数据如下表:
已知1mol H2O (g)转变为1mol H2O(l)时放出44.0kJ热量.则CH4和水蒸气在高温下反应生成1mol H2的反应热为
(2)用CO和H2在一定条件下合成甲醇:CO+2H2?CH3OH.工业上采用稍高的压强(5MPa)和250℃,其可能原因是
(3)1,3-丙二醇是重要的化工原料,用乙烯合成1,3-丙二醇的路线如下:
CH2=CH2 HOCH2CH2CHO
HOCH2CH2CHO  HOCH2CH2CH2OH
HOCH2CH2CH2OH
某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O
CO+H2 CH4+H2O
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
查看习题详情和答案>>
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O═CO+3H2.部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
+68.7kJ/mol
+68.7kJ/mol
.(2)用CO和H2在一定条件下合成甲醇:CO+2H2?CH3OH.工业上采用稍高的压强(5MPa)和250℃,其可能原因是
从平衡常数与温度的变化关系可知该反应为放热反应,温度低,甲醇的产率高,但反应速率慢,经济效益低;又因为该反应是气体体积缩小的反应,采用稍高的压强有利于提高原料气的转化率
从平衡常数与温度的变化关系可知该反应为放热反应,温度低,甲醇的产率高,但反应速率慢,经济效益低;又因为该反应是气体体积缩小的反应,采用稍高的压强有利于提高原料气的转化率
.| 反应温度/℃ | 平衡常数 | 反应温度/℃ | 平衡常数 |
| 0 | 667.30 | 200 | 1.909×10-2 |
| 100 | 12.92 | 300 | 2.42×10-4 |
CH2=CH2
 HOCH2CH2CHO
HOCH2CH2CHO  HOCH2CH2CH2OH
HOCH2CH2CH2OH某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O
| ||
| ||
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
需要焦炭3.0 t、甲烷4.0 t
需要焦炭3.0 t、甲烷4.0 t
.(2009?南京二模)选做题,本题有A、B两题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容,请选择其中一题作答,并把所选题目对应字母后的方框涂黑.若两题都作答,将按A题评分.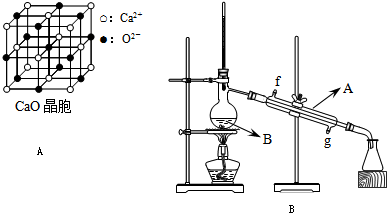
A.可以由下列反应合成三聚氰胺:
CaO+3C
CaC2+CO↑ CaC2+N2
CaCN2+C↑ CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺.
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
(2)尿素分子中C原子采取
 ,其中碳氧原子之间的共价键是
,其中碳氧原子之间的共价键是
A.2个σ键 B.2个π键 C.1个σ键、1个π键
(3)三聚氰胺(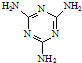 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸( 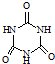 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过
(4)CaO晶胞如图A所示,CaO晶体中Ca2+的配位数为
B.实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的物理性质如下表.请回答有关问题.
Ⅰ.乙酸正丁酯粗产品的制备
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)本实验过程中可能产生多种有机副产物,写出其中两种的结构简式:
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是:
Ⅱ.乙酸正丁酯粗产品的制备
(1)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠洗涤,正确的操作步骤是
A.①②③④B.③①④②C.①④①③②D.④①③②③
(2)将酯层采用如图B所示装置蒸馏.
1.出图中仪器A的名称
2.②蒸馏收集乙酸正丁酯产品时,应将温度控制在
Ⅲ.计算产率
测量分水器内由乙酸与正丁醇反应生成的水体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率
查看习题详情和答案>>

A.可以由下列反应合成三聚氰胺:
CaO+3C
| ||
| ||
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
1s22s22p63s23p63d104s2或[Ar]3d104s2
1s22s22p63s23p63d104s2或[Ar]3d104s2
.CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和CO2
CO2
(填化学式),由此可以推知CN22-离子的空间构型为直线形
直线形
.(2)尿素分子中C原子采取
sp2
sp2
杂化.尿素分子的结构简式是

C
C
(填字母)A.2个σ键 B.2个π键 C.1个σ键、1个π键
(3)三聚氰胺(
 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(  )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过分子间氢键
分子间氢键
结合,在肾脏内易形成结石.(4)CaO晶胞如图A所示,CaO晶体中Ca2+的配位数为
6
6
.CaO晶体和NaCl晶体的晶格能分别为:CaO 3401kJ/mol、NaCl 786kJ/mol.导致两者晶格能差异的主要原因是CaO晶体中Ca 2+、O 2-的带电量大于NaCl晶体中Na+、Cl-的带电量
CaO晶体中Ca 2+、O 2-的带电量大于NaCl晶体中Na+、Cl-的带电量
.B.实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的物理性质如下表.请回答有关问题.
| 化合物 | 密度/g?cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | ∞ |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)本实验过程中可能产生多种有机副产物,写出其中两种的结构简式:
CH3CH2CH2CH2OCH2CH2CH2CH3
CH3CH2CH2CH2OCH2CH2CH2CH3
、CH2=CHCH2CH3
CH2=CHCH2CH3
.(2)实验中为了提高乙酸正丁酯的产率,采取的措施是:
用分水器及时移走反应生成的水,减少生成物的浓度;
用分水器及时移走反应生成的水,减少生成物的浓度;
、使用过量醋酸,提高正丁醇的转化率
使用过量醋酸,提高正丁醇的转化率
.Ⅱ.乙酸正丁酯粗产品的制备
(1)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠洗涤,正确的操作步骤是
C
C
(填字母).A.①②③④B.③①④②C.①④①③②D.④①③②③
(2)将酯层采用如图B所示装置蒸馏.
1.出图中仪器A的名称
冷凝管
冷凝管
.冷却水从下
下
口进入(填字母).2.②蒸馏收集乙酸正丁酯产品时,应将温度控制在
126.1℃
126.1℃
左右.Ⅲ.计算产率
测量分水器内由乙酸与正丁醇反应生成的水体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率
79.4%
79.4%
.利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径.回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O=CO+3H2.部分物质的燃烧热数据如表:
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0kJ热量.写出CH4和水蒸气在高温下反应的热化学方程式
(2)500℃、50MPa时,在容积为V L的容器中加入1mol N2、3mol H2,,此时N2的转化率为a.则平衡时NH3的浓度为
mol/L
mol/L.
(3)1,3-丙二醇是重要的化工原料,用乙烯合成1,3-丙二醇的路线如下:

某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O
CO+H2 CH4+H2O
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭
查看习题详情和答案>>
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O=CO+3H2.部分物质的燃烧热数据如表:
| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1
.(2)500℃、50MPa时,在容积为V L的容器中加入1mol N2、3mol H2,,此时N2的转化率为a.则平衡时NH3的浓度为
| 2a |
| V |
| 2a |
| V |
(3)1,3-丙二醇是重要的化工原料,用乙烯合成1,3-丙二醇的路线如下:

某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O
| ||
| ||
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭
3.0
3.0
吨、甲烷4.0
4.0
吨,才能满足生产需要.(2011?顺义区二模)甲烷是一种重要的基础化工原料,不仅可制备多种重要有机产品,还可用于环境保护.请回答下列问题:(1)用甲烷催化还原氮的氧化物可消除氮氧化物的污染.已知:
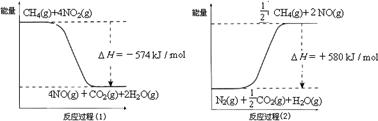
反应过程(2)是
(2)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应:
CCl4(g)+H2(g)?CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应).
在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
①此反应在110℃时平衡常数为
③判断该反应的正反应是
④为提高实验3中CCl4的转化率,可采取的措施是
a.使用高效催化剂 b.向容器中再投入1mol CCl4和1mol H2
c.温度升高到200℃d.向容器中再投入1mol HCl e.向容器中再投入1mol H2.
查看习题详情和答案>>

反应过程(2)是
吸热
吸热
反应(填“放热”或“吸热”),甲烷还原NO2生成H2O(g)、N2和CO2时的热化学方程式是2CH4(g)+4NO2(g)=2CO2(g)+2N2(g)+4H2O(g)△H=-1734kJ/mol
2CH4(g)+4NO2(g)=2CO2(g)+2N2(g)+4H2O(g)△H=-1734kJ/mol
.(2)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应:
CCl4(g)+H2(g)?CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应).
在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
| 实验 序号 |
温度℃ | 初始n(CCl4) (mol) |
初始n(H2) (mol) |
平衡时n(CHCl3) (mol) |
| 1 | 110 | 0.8 | 1.2 | |
| 2 | 110 | 2 | 2 | 1 |
| 3 | 100 | 1 | 1 | 0.6 |
1
1
. ②实验l中,CCl4的转化率为60%
60%
.③判断该反应的正反应是
放热
放热
(填“放热”或“吸热”),理由是温度为100℃时,K=2.25,大于110℃时的平衡常数,所以该反应为放热反应
温度为100℃时,K=2.25,大于110℃时的平衡常数,所以该反应为放热反应
.④为提高实验3中CCl4的转化率,可采取的措施是
e
e
.a.使用高效催化剂 b.向容器中再投入1mol CCl4和1mol H2
c.温度升高到200℃d.向容器中再投入1mol HCl e.向容器中再投入1mol H2.
醋酸是重要的一元酸,在有机和无机反应中都有应用.现有25℃时pH=3的醋酸.请回答下列问题:
(1)若向醋酸中加入少量醋酸钠固体,此时溶液中
将
(2)若向醋酸中加入稀NaOH溶液,使其恰好完全反应,所得溶液的pH
(3)若向醋酸中加入pH=11的NaOH溶液,且二者的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是:
(4)若向醋酸中加入稀NaOH溶液至溶液恰好呈中性,此时c(Na+)
(5)若向醋酸中加入一定量的NaOH溶液,所得混合溶液的pH=6,则此溶液中c(CH3COO-)-c(Na+)=
查看习题详情和答案>>
(1)若向醋酸中加入少量醋酸钠固体,此时溶液中
| c(H+) | c(CH3COOH) |
减小
减小
(填“增大”、“减小”或“不变”).(2)若向醋酸中加入稀NaOH溶液,使其恰好完全反应,所得溶液的pH
>
>
7(填“>”、“<”或“=”);用离子方程式表示其原因CH3COO-+H2O?CH3COOH+OH-
CH3COO-+H2O?CH3COOH+OH-
.(3)若向醋酸中加入pH=11的NaOH溶液,且二者的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是:
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
.(4)若向醋酸中加入稀NaOH溶液至溶液恰好呈中性,此时c(Na+)
=
=
c(CH3COO-)(填“>”“<”“=”).(5)若向醋酸中加入一定量的NaOH溶液,所得混合溶液的pH=6,则此溶液中c(CH3COO-)-c(Na+)=
(10-6-10-8)mol/L
(10-6-10-8)mol/L
(填写准确数据).