网址:http://m.1010jiajiao.com/timu3_id_279878[举报]
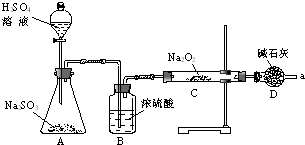 某同学想通过如图装置实验,探究SO2与Na2O2反应的产物.
某同学想通过如图装置实验,探究SO2与Na2O2反应的产物.Ⅰ.检验反应中是否有O2生成的方法是
Ⅱ.A中盛装H2SO4溶液的仪器名称是
Ⅲ.(1)C中固体产物可能只有Na2SO3、只有
(2)若Na2O2反应完全,为确定C中固体产物的成分,该同学设计如下,请您利用限选试剂和仪器帮助他完成该探究过程,并将答案写在答题卡相应位置.
限选试剂和仪器:0.1mol/LKMnO4酸性溶液、0.01mol/LKMnO4酸性溶液、0.1mol/LBa(NO3)2溶液、0.1mol/LBaCl2溶液、1mol/L HNO3溶液、1mol/L盐酸、试管、胶头滴管.
| 实验操作 | 预期现象和结论 | 步骤一:取少量C中固体产物于试管中,加入适量的蒸馏水、搅拌溶解,分别取少量于A、B试管中. | 固体完全溶解,得到无色透明溶液 | 步骤二:取试管A,向溶液中加入 |
若 则 |
步骤三:取试管B,向其中先加入 |
产生 再加入另一试剂看到产生白色沉淀,则固体C中还含有 |
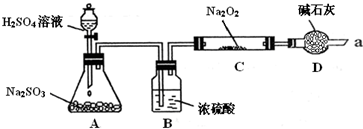
Ⅰ如何检验反应中是否有O2生成
Ⅱ装置D除起了防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应作用外,还可以
Ⅲ对C中固体产物提出如下假设:
假设1:只有Na2SO3 假设2:只有Na2SO4 假设3:
(1)假设1的反应方程式:2SO2+2Na2O2=
(2)若Na2O2反应完全,为确定C中固体产物的成分,该同学设计如下,请您利用限选试剂和仪器帮助他完成该探究过程,并将答案写在答题卡相应位置.限选试剂和仪器:酸性KMnO4溶液、Ba(NO3)2溶液、BaCl2溶液、1mol/L HNO3溶液、4mol/L盐酸、试管、胶头滴管
| 实验操作 | 预期现象 | 结 论 |
| 步骤一:取少量C中固体产物于试管中,加入适量的蒸馏水溶解,分别取少量于A、B试管中 | 固体完全溶解,得到无色透明溶液 | / |
| 步骤二:取试管A,向溶液中加入 |
假设1 或假设3成立;若没有该现象则假设2成立. | |
| 步骤三:取试管B,向其中先加入 再加入 |
产生 再加入试剂看到产生白色沉淀. |
假设3成立.若无白色沉淀产生则假设1成立. |
某课外活动小组对一氧化碳还原氧化铁的实验中最后的产物产生浓厚的兴趣,试通过实验来探究其成分。
Ⅰ.实验装置:
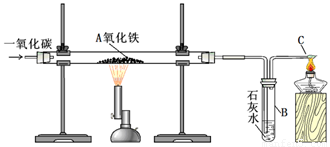
用一氧化碳还原氧化铁的实验装置
该装置B中发生的离子方程式是
装置B的作用是
Ⅱ.实验现象:玻璃管A中的粉末由红色逐渐变为黑色时,停止加热,继续通一氧化碳,冷却到室温,停止通气,同时观察到澄清的石灰水变浑浊。
Ⅲ.实验结论:
甲认为:依据上述实验现象可以判断出生成的黑色固体为金属铁。
乙认为:仅从上述实验现象,不足以证明生成的黑色固体为金属铁,她增加了一个实验:用磁铁靠近生成的黑色固体,看到有黑色固体被磁铁吸引。于是得出生成的黑色固体为金属铁的结论。
请你通过该反应的相关资料对他们结论作出判断并通过实验检验其合理性:
(1)在一定条件下:一氧化碳与氧化铁在加热条件下,可发生如下反应
3Fe2O3+CO 2Fe3O4+CO2
2Fe3O4+CO2
Fe3O4+4CO 4Fe+4CO2
4Fe+4CO2
(2)四氧化三铁(Fe3O4)为黑色固体,有强磁性,能够被磁铁吸引。
甲、乙同学的结论: 你对此评价的理由是:
Ⅳ.实验探究
对反应后固体成分提出假设:
假设1:反应后固体中只有Fe;
假设2:反应后固体中只有Fe3O4;
假设3:反应后固体中__ _____________________
为确定实验中最后的产物的成分,丙同学设计如下实验,请您利用限选试剂和仪器帮助他完成该探究过程,并将答案写在答题卡相应位置。
限选试剂和仪器: 1mol/LCuSO4 、0.01mol/L KSCN溶液、1mol/L盐酸、0.01mol/L氯水、试管、玻璃棒、胶头滴管。
|
实验操作 |
预期现象和结论 |
|
步骤一:取硬质玻璃管中固体产物少量分别于A、B试管中,加入足量1mol/LCuSO4溶液、搅拌溶解。 |
(1)若A试管中黑色固体不溶解,并且没有观察到其他现象,则黑色固体为 (2)若B试管中有红色固体析出,则说明黑色固体中含有Fe。 |
|
步骤二:对试管B中溶液过滤,将所得固体洗涤干净后,加足量1mol/L盐酸后,再依次分别加入适量0.01mol/L氯水、少量0.01mol/L KSCN溶液 |
(1)若溶液不变红色,则
(2)若溶液变红色,则
|
Ⅴ.延伸探究:丁同学试图通过反应前后固体质量的变化来确定黑色固体的成分,你认为可行吗?(假设氧化铁在反应中完全反应) (填“行”或“不行”)理由是 。
查看习题详情和答案>>
某同学想通过下图装置实验,探究SO2与Na2O2反应的产物。
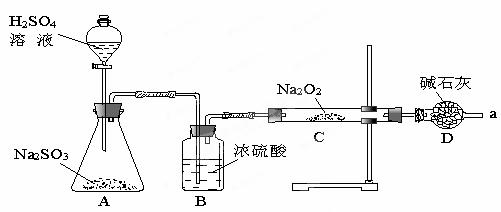
Ⅰ.检验反应中是否有O2生成的方法是 ;若有O2生成,请写出装置C中的化学方程式 。
Ⅱ .A中盛装H2SO4溶液的仪器名称是____________;D装置除起了防止空
气中的水蒸气和二氧化碳进入C装置与Na2O2反应作用外,还可以 。
Ⅲ.(1)C中固体产物可能只有Na2SO3、只有 、Na2SO3和Na2SO4两种都有。
(2)若Na2O2反应完全,为确定C中固体产物的成分,该同学设计如下,请您利用限选试剂和仪器帮助他完成该探究过程,并将答案写在答题卡相应位置。
限选试剂和仪器: 0.1mol/LKMnO4酸性溶液、0.01mol/LKMnO4酸性溶液、0.1mol/LBa(NO3)2溶液、0.1mol/LBaCl2溶液、1mol/L HNO3溶液、1mol/L盐酸、试管、胶头滴管。
| 实验操作 | 预期现象和结论 |
| 步骤一:取少量C中固体产物于试管中,加入适量的蒸馏水、搅拌溶解,分别取少量于A、B试管中。 | 固体完全溶解,得到无色透明溶液 |
| 步骤二:取试管A,向溶液中加入 ,振荡,观察溶液颜色变化。 | 若 ; 则 。 |
| 步骤三:取试管B,向其中先加入 ,振荡;再加入 ,振荡。 | 产生 , 再加入另一试剂看到产生白色沉淀,则 固体C中还含有 。 |
(1)I2O5可使H2S、CO、HCl等氧化,常用于定量测定CO的含量.已知:
2I2(s)+5O2(g)=2I2O5(s);△H=-75.56kJ?mol-1
2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ?mol-1
写出CO(g)与I2O5(s)反应生成I2(s)和CO2(g)的热化学方程式:
(2)CO可制做燃料电池,以KOH溶液作电解质,向两极分别充入CO和空气,工作过程中,K+
(3)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应.该技术的优点除了能回收利用SO2外,还能得到一种复合肥料.
①该复合肥料可能的化学式为
②若氨水与SO2恰好完全反应生成正盐,则此时溶液呈
常温下弱电解质的电离平衡常数如下:氨水 Kb=1.8×10-5mol?L-1
H2SO3 Ka1=1.3×10-2mol?L-1,Ka2=6.3×10-8mol?L-1
③向②中溶液中通入
此时溶液中
| ||
|
(4)NOx可用强碱溶液吸产生硝酸盐.在酸性条件下,FeSO4溶液能将
| NO | - 3 |