摘要:13.假设白化病的致病基因为a.色盲的致病基因为b.一表现型正常的男性.与一正常的女性婚配.则他们婚配后生一个只患一种病小孩的概率是( ) A.3/16 B. 3/8 C.3/4 D.1/4
网址:http://m.1010jiajiao.com/timu3_id_279580[举报]
 已知某燃料含碳、氢、氧三种元素,为了测定该燃料的组成:将该燃料放入足量氧气中燃烧,并使产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收).
已知某燃料含碳、氢、氧三种元素,为了测定该燃料的组成:将该燃料放入足量氧气中燃烧,并使产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收).| 实验前 | 实验后 | |
| 甲的质量/g | 101.1 | 103.8 |
| 乙的质量/g | 82.0 | 86.4 |
(1)该燃料完全燃烧生成水的质量为
2.7
2.7
g,生成CO2的质量为4.4
4.4
g.(2)该燃料分子中碳、氢原子的数目比为
1:3
1:3
.(3)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为
C2H6O
C2H6O
,结构简式为CH3CH2OH(或CH3OCH3)
CH3CH2OH(或CH3OCH3)
.已知X、Y、Z为单质,其他为化合物.其中Y为气体,G溶液呈黄色,E是不溶于水的酸性氧化物,能与氢氟酸反应,它们之间存在如下转化关系(部分产物已略去).请回答下列问题:
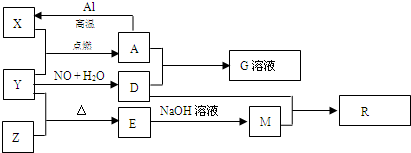
(1)E的化学式是
(2)M的水溶液俗称
(3)写出A和D的稀溶液反应生成G的离子方程式
(4)向含2mol D的稀溶液中,逐渐加入X粉末至过量.假设生成的气体只有一种,则n(Xm+)的最大值为
查看习题详情和答案>>

(1)E的化学式是
SiO2
SiO2
.(2)M的水溶液俗称
水玻璃
水玻璃
,它与D反应的化学方程式为Na2SiO3+2HNO3=H2SiO3↓+2NaNO3
Na2SiO3+2HNO3=H2SiO3↓+2NaNO3
.(3)写出A和D的稀溶液反应生成G的离子方程式
3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O
3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O
.(4)向含2mol D的稀溶液中,逐渐加入X粉末至过量.假设生成的气体只有一种,则n(Xm+)的最大值为
0.75
0.75
.氢溴酸在医药和石化工业上有广泛用途.下图是模拟工业制备氢溴酸粗品并精制流程:

根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为
(2)混合①中使用冰水的目的是
(3)操作Ⅱ和操作Ⅲ的名称分别是
操作Ⅲ一般适用于分离
a.固体和液体 b.固体和固体 c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na2SO3的目的是
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色.于是甲乙两同学设计了简单实验加以探究:
甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为
乙同学假设工业氢溴酸呈淡黄色是因为
查看习题详情和答案>>

根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为
SO2+Br2+2H2O=2HBr+H2SO4
SO2+Br2+2H2O=2HBr+H2SO4
.(2)混合①中使用冰水的目的是
降低体系温度,防止溴蒸发,使反应完全
降低体系温度,防止溴蒸发,使反应完全
.(3)操作Ⅱ和操作Ⅲ的名称分别是
过滤
过滤
、蒸馏
蒸馏
.操作Ⅲ一般适用于分离
d
d
混合物.(选填编号)a.固体和液体 b.固体和固体 c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na2SO3的目的是
除去粗品中未反应完的溴
除去粗品中未反应完的溴
.(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色.于是甲乙两同学设计了简单实验加以探究:
甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为
KSCN溶液
KSCN溶液
,若假设成立可观察到的现象为溶液变成血红色
溶液变成血红色
.乙同学假设工业氢溴酸呈淡黄色是因为
含有Br2
含有Br2
,其用于证明该假设所用的试剂为CCl4
CCl4
.某研究性学习小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X.有人认为X不一定只是Fe,因为温度不同、受热不均时会生成Fe3O4,Fe3O4也能被磁铁吸引.,为探究X的组成,进行如下实验.
(一)提出假设①X的成分为Fe
②X的成分为Fe3O4
③X的成分为Fe与Fe3O4的混合物
(二)设计方案
I-定性探究
(1)将适量固体X加入盐酸中,充分反应后,加入适量的KSCN溶液,若溶液未变红色, (填“能”或“不能”)表明固体X中不含Fe304.简述理由
(2)某同学采用还原法检验X中是否含有Fe304.

①按如图连接装置,并检查装置的气密性.
②打开止水夹,通入纯净的H2.在点燃A处的酒精灯之前,需排尽装置内的空气,原因是 .
③若加热一段时间后,装置B中的白色固体部分变为蓝色,可得出的结论是
(3)若要进一步证明X的组成,还得进行的实验是(简述实验操作、现象)
结论: .
II.定量探究
某同学利用(2)装置,通过定量实验也可探究X的组成.
①己知a管质量为122.0g,取18.0g干燥X粉末加入a中.
②按(2)进行实验至B中无水硫酸铜颜色不再变化,停止加热,继续通H2至a管恢复室温
③相同条併吓称量,a管质量(含粉末)为138.4g.试通过计算分析X的组成.(要求写出计算过程)
查看习题详情和答案>>
(一)提出假设①X的成分为Fe
②X的成分为Fe3O4
③X的成分为Fe与Fe3O4的混合物
(二)设计方案
I-定性探究
(1)将适量固体X加入盐酸中,充分反应后,加入适量的KSCN溶液,若溶液未变红色,
(2)某同学采用还原法检验X中是否含有Fe304.

①按如图连接装置,并检查装置的气密性.
②打开止水夹,通入纯净的H2.在点燃A处的酒精灯之前,需排尽装置内的空气,原因是
③若加热一段时间后,装置B中的白色固体部分变为蓝色,可得出的结论是
(3)若要进一步证明X的组成,还得进行的实验是(简述实验操作、现象)
结论:
II.定量探究
某同学利用(2)装置,通过定量实验也可探究X的组成.
①己知a管质量为122.0g,取18.0g干燥X粉末加入a中.
②按(2)进行实验至B中无水硫酸铜颜色不再变化,停止加热,继续通H2至a管恢复室温
③相同条併吓称量,a管质量(含粉末)为138.4g.试通过计算分析X的组成.(要求写出计算过程)