摘要:30.(1)c(Ag+)=1×10-7mol/L. 本资料由 提供!
网址:http://m.1010jiajiao.com/timu3_id_278563[举报]
|
按下图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示
(1)c(Ag+) (2)c(NO3-) (3)a棒的质量 (4)b棒的质量 (5)溶液的pH | |
| [ ] | |
A. |
(1)(3) |
B. |
(3)(4) |
C. |
(1)(2)(4) |
D. |
(1)(2)(5) |
现有A、B、C、D、E五种盐溶液,分别由K+、NH4+、Ag+、Ba2+、Al3+、Cl-、Br-、CO32-、SO42-、NO3- 中的阳离子和阴离子各一种组成(五种盐所含阴、阳离子各不相同)已知:
①A+B→白色沉淀 ②A+D→白色沉淀 ③A+C→白色沉淀
④D+B→白色沉淀+无色气体 ⑤A溶液中c(H+)=c(OH-)
⑥B溶液中c(H+)=1×10-12mol?L-1 ⑦C、D、E三种溶液的pH<7,
根据以上实验事实可以推出(用分子式表示)
A为
写出以上①②③④各步反应的离子方程式:
①
③
查看习题详情和答案>>
①A+B→白色沉淀 ②A+D→白色沉淀 ③A+C→白色沉淀
④D+B→白色沉淀+无色气体 ⑤A溶液中c(H+)=c(OH-)
⑥B溶液中c(H+)=1×10-12mol?L-1 ⑦C、D、E三种溶液的pH<7,
根据以上实验事实可以推出(用分子式表示)
A为
BaCl2
BaCl2
;B为K2CO3
K2CO3
;C为AgNO3
AgNO3
;D为Al2(SO4)
Al2(SO4)
;E为NH4Br
NH4Br
.写出以上①②③④各步反应的离子方程式:
①
Ba2++CO32-═BaCO3↓
Ba2++CO32-═BaCO3↓
,②Ba2++SO42-═BaSO4↓
Ba2++SO42-═BaSO4↓
,③
Ag++Cl-═AgCl↓
Ag++Cl-═AgCl↓
,④2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑
2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑
.某同学称取9g淀粉溶于水,测定淀粉的水解率,其程序如下:
(1)各步所加试剂为:A
(2)
(3)当析出2.16g单质沉淀时,淀粉的水解率为
查看习题详情和答案>>

(1)各步所加试剂为:A
稀硫酸
稀硫酸
;BNaOH
NaOH
;C[Ag(NH3)2]OH
[Ag(NH3)2]OH
.(2)
不可以
不可以
(填“可以”或“不可以”)只加C溶液而不加B溶液,原因是银镜反应必须在碱性条件下发生,所以必须加入NaOH溶液将催化剂H2SO4中和掉
银镜反应必须在碱性条件下发生,所以必须加入NaOH溶液将催化剂H2SO4中和掉
.(3)当析出2.16g单质沉淀时,淀粉的水解率为
18%
18%
.(1)ag铁粉放入含bmolHNO3的浓硝酸中,加热充分反应后,再加入稀硫酸,铁粉恰好完全溶解,经测定溶液中只含Fe3+(一种金属离子)和SO42-(一种酸根离子).
①写出反应开始时溶液中发生反应的化学方程式
②写出加入硫酸后,所发生反应的离子方程式
(2)硫酸是基础化学工业的重要产品目前,我国采用“接触法”制硫酸,简单流程如图所示: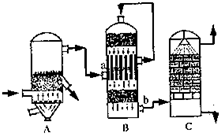
①设备B中名称是
②设备C中用98.3%的H2SO4来吸收SO2的原因是
③燃烧1t含硫质量分数为48%的黄铁矿石,在理论上能生产98%H2SO4
查看习题详情和答案>>
①写出反应开始时溶液中发生反应的化学方程式
Fe+4HNO3(浓)
Fe(NO3)2+2NO2↑+2H2O
| ||
Fe+4HNO3(浓)
Fe(NO3)2+2NO2↑+2H2O
.
| ||
②写出加入硫酸后,所发生反应的离子方程式
Fe+4H++NO3-═Fe3++NO↑+2 H2O; 3Fe2++4H++NO3-═3Fe3++NO↑+2 H2O
Fe+4H++NO3-═Fe3++NO↑+2 H2O; 3Fe2++4H++NO3-═3Fe3++NO↑+2 H2O
.(2)硫酸是基础化学工业的重要产品目前,我国采用“接触法”制硫酸,简单流程如图所示:

①设备B中名称是
接触室
接触室
,图中b处导出气体的成分是(写化学式)SO3、SO2、O2、N2
SO3、SO2、O2、N2
.②设备C中用98.3%的H2SO4来吸收SO2的原因是
为了提高SO3的吸收效率,防止形成酸雾
为了提高SO3的吸收效率,防止形成酸雾
.③燃烧1t含硫质量分数为48%的黄铁矿石,在理论上能生产98%H2SO4
1.5
1.5
t.