网址:http://m.1010jiajiao.com/timu3_id_278305[举报]
(15分)50mL 0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在右图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算反应热。

请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 ;(由图可知该装置有两处不妥之处:(1) 。(2 ) 。
(2)烧杯间填满碎塑料泡沫的作用是________。
(3)大烧杯上如不盖硬纸板,则求得的反应热数值___。(填“偏大”、“偏小’、“无影响”)。
(4)若实验过程中,测得盐酸和NaOH溶液的起始温度的平均值为25.2℃.溶液混合后的最高温度为28.6℃.试经过计算写出表示该反应中和热的热化学方程式:________
(混合溶液的比热容c=4.18J/( ℃),盐酸和NaOH溶液的密度认为都是1
℃),盐酸和NaOH溶液的密度认为都是1
 )
)
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会____(填“偏大”、“偏小”、“无影响”)。
查看习题详情和答案>>
(15分)50mL 0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在右图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算反应热。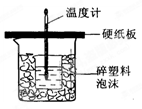
请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 ;(由图可知该装置有两处不妥之处:(1) 。(2 ) 。
(2)烧杯间填满碎塑料泡沫的作用是________。
(3)大烧杯上如不盖硬纸板,则求得的反应热数值___。(填“偏大”、“偏小’、“无影响”)。
(4)若实验过程中,测得盐酸和NaOH溶液的起始温度的平均值为25.2℃.溶液混合后的最高温度为28.6℃.试经过计算写出表示该反应中和热的热化学方程式:________
(混合溶液的比热容c=4.18J/(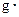 ℃),盐酸和NaOH溶液的密度认为都是1
℃),盐酸和NaOH溶液的密度认为都是1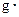
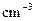 )
)
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会____(填“偏大”、“偏小”、“无影响”)。
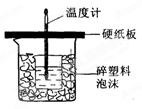
请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 ;(由图可知该装置有两处不妥之处:(1) 。(2 ) 。
(2)烧杯间填满碎塑料泡沫的作用是________。
(3)大烧杯上如不盖硬纸板,则求得的反应热数值___。(填“偏大”、“偏小’、“无影响”)。
(4)若实验过程中,测得盐酸和NaOH溶液的起始温度的平均值为25.2℃.溶液混合后的最高温度为28.6℃.试经过计算写出表示该反应中和热的热化学方程式:________
(混合溶液的比热容c=4.18J/(
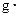 ℃),盐酸和NaOH溶液的密度认为都是1
℃),盐酸和NaOH溶液的密度认为都是1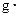
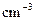 )
)(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会____(填“偏大”、“偏小”、“无影响”)。