摘要:25.配制硫酸铁溶液常出现浑浊现象,其原因是: , 如何操作即可得到透明溶液而又不引进杂质离子: . 26在氧化铝溶液中加入少量的氢氧化钠溶液.可观察到的现象: 继续加入氢氧化钠并不断振荡可观察到现象: 27用金属铝制成的易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口,经过一段时间后,罐变瘪,再经过一段时间后, 瘪的罐又重新变鼓起来. (1)罐变瘪的原因是 , (2)经过一段时间后, 瘪的罐又重新变鼓起来的原因是 . 三.实验题 28实验室通常用固体氯化铵和熟石灰共热制取氨气.请填写下列空白 A B C D (1)上图中.用于该实验制取的气体发生装置是 (2)收集氨气的方法是 A.向下排空气法 B.向上排空气法 C.排水法 (3)制取氨气的化学方程式是 (4)干燥氨气时可选用的干燥剂是 A.浓硫酸 B.碱石灰 C.五氧化二磷 29用已知浓度的盐酸滴定未知浓度的NaOH溶液时.滴定时左手 右手 眼睛注视 ,若用酚酞做指示剂,达到滴定终点的判断标准 .已知盐酸的浓度为Cmol·L-1滴定时消耗的体积为V1ml,量取的溶液的体积为V2 ml,则NaOH的物质的量的浓度为
网址:http://m.1010jiajiao.com/timu3_id_277445[举报]
硫酸的消费量常被视为一个国家工业发达水平的标志.我国主要以黄铁矿(FeS2)为原料采用接触法生产硫酸.其主要涉及到的反应有(没有配平)A.FeS2+O2→Fe2O3+SO2 B. SO2(g)+O2 (g)→SO3(g) C.SO3+H2O→H2SO4
回答下列问题:
(1)已知FeS2与足量氧气反应生成1molSO2时放出426.5kJ的热量.则其反应的热化学方程式为
(2)已知某温度时反应B的平衡常数为800.在体积恒为10L的密闭容器中充入10mol SO2、30mol O2和10mol SO3,反应开始将向
A.容器内压强不变 B.混合气体的密度不变 C.v正(SO2)=2v正(O2)
D.c(SO2):c(O2):c(SO3)=2:1:2 E.混合气体的摩尔质量不变
(3)反应A的副产物Fe2O3是铁锈的主要成分.N2H4(肼)能使锅炉内壁的铁锈(主要成分Fe2O3)变成磁性氧化铁(Fe3O4)层,可以减缓锅炉锈蚀.若反应过程中肼转化为氮气,每生成1mol Fe3O4,转移电子的物质的量为
(4)铁盐溶液可以洗涤做过银镜实验的试管,原理是Fe3++Ag(s)?Fe2++Ag+.甲同学将银粉加入到Fe2(SO4)3溶液中进行了实验,观察到的现象是
(5)用10mol/L的浓硫酸配制2mol/L的稀硫酸,所用的玻璃仪器除量筒和玻璃棒外,还有
A.容量瓶 B.烧杯 C.烧瓶 D.胶头滴管.
查看习题详情和答案>>
回答下列问题:
(1)已知FeS2与足量氧气反应生成1molSO2时放出426.5kJ的热量.则其反应的热化学方程式为
4FeS2(s)+11O2(g)
2Fe2O3(s)+8SO2(g)△H=-3412kJ/mol
| ||
4FeS2(s)+11O2(g)
2Fe2O3(s)+8SO2(g)△H=-3412kJ/mol
.
| ||
(2)已知某温度时反应B的平衡常数为800.在体积恒为10L的密闭容器中充入10mol SO2、30mol O2和10mol SO3,反应开始将向
正
正
(填“正”或“逆”)方向进行.在该容器中,能说明该反应已达到平衡状态的依据是A、E
A、E
(填字母序号)A.容器内压强不变 B.混合气体的密度不变 C.v正(SO2)=2v正(O2)
D.c(SO2):c(O2):c(SO3)=2:1:2 E.混合气体的摩尔质量不变
(3)反应A的副产物Fe2O3是铁锈的主要成分.N2H4(肼)能使锅炉内壁的铁锈(主要成分Fe2O3)变成磁性氧化铁(Fe3O4)层,可以减缓锅炉锈蚀.若反应过程中肼转化为氮气,每生成1mol Fe3O4,转移电子的物质的量为
1mol
1mol
,需要消耗肼的质量为8
8
g.(4)铁盐溶液可以洗涤做过银镜实验的试管,原理是Fe3++Ag(s)?Fe2++Ag+.甲同学将银粉加入到Fe2(SO4)3溶液中进行了实验,观察到的现象是
银粉逐渐溶解,溶液由棕黄色逐渐变为浅绿色,溶液出现白色沉淀
银粉逐渐溶解,溶液由棕黄色逐渐变为浅绿色,溶液出现白色沉淀
.丙同学认为向试管中加入几块铅笔芯也有利于除去银,你认为他的理由是银与铅笔中的石墨在溶液中形成了原电池,银为负极,石墨为正极,加快了反应速率
银与铅笔中的石墨在溶液中形成了原电池,银为负极,石墨为正极,加快了反应速率
.(5)用10mol/L的浓硫酸配制2mol/L的稀硫酸,所用的玻璃仪器除量筒和玻璃棒外,还有
A、B、D
A、B、D
A.容量瓶 B.烧杯 C.烧瓶 D.胶头滴管.
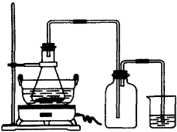 绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.
绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.请回答下列问题:
(1)图是某研究性学习小组用于制备绿矾的装置,其中集气瓶的作用是
(2)如图锥形瓶中的反应物是铁屑和28%的硫酸,反应前常用98%的硫酸配制500g 28%的硫酸,要算出所需98%的硫酸的体积,还要知道的数据是
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁,并对产品质量进行检测.检测结果如下:
| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
(4)该小组在继续研究由绿矾制备Fe(OH)2的过程中,发现出现白色的沉淀会逐渐转变为灰绿色,最后变为红褐色.甲同学查资料该灰绿色沉淀可能是Fe3(OH)8,请用氧化物的形式写出该沉淀
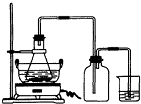 (2009?广东模拟)绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.请回答下列问题:
(2009?广东模拟)绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.请回答下列问题:(1)右图锥形瓶中的反应物是铁屑和28%的硫酸,反应前常用98%的硫酸配制500g 28%的硫酸,要算出所需98%的硫酸的体积,还要知道的数据是
98%硫酸的密度
98%硫酸的密度
.(2)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁,并对产品质量进行检测.检测结果如下:
| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
铁
铁
过量为最佳.(3)该小组在继续研究由绿矾制备Fe(OH)2的过程中,发现出现白色的沉淀会逐渐转变为灰绿色,最后变为红褐色.甲同学查资料该灰绿色沉淀可能是Fe3(OH)8,请用氧化物的形式写出该沉淀
FeO?Fe2O3?4H2O
FeO?Fe2O3?4H2O
;乙同学查资料后认为该灰绿色沉淀是由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3的缘故,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色.或者可以将Fe(OH)3和Fe(OH)2混合后观察其颜色
向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色.或者可以将Fe(OH)3和Fe(OH)2混合后观察其颜色
.
绿矾是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.请回答下列问题:
(1)右图锥形瓶中的反应物是铁屑和28%的硫酸,反应前常用98%的硫酸配制500g 28%的硫酸,要算出所需98%的硫酸的体积,还要知道的数据是______.
(2)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁,并对产品质量进行检测.检测结果如下:
已知产品质量标准:Fe3+的质量分数等于0.005%,产品质量定为Ⅰ级;Fe3+的质量分数等于0.01%,产品质量定为Ⅱ级,从实验结果中,可得出制备硫酸亚铁溶液时,反应控制______过量为最佳.
(3)该小组在继续研究由绿矾制备Fe(OH)2的过程中,发现出现白色的沉淀会逐渐转变为灰绿色,最后变为红褐色.甲同学查资料该灰绿色沉淀可能是Fe3(OH)8,请用氧化物的形式写出该沉淀______;乙同学查资料后认为该灰绿色沉淀是由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3的缘故,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)右图锥形瓶中的反应物是铁屑和28%的硫酸,反应前常用98%的硫酸配制500g 28%的硫酸,要算出所需98%的硫酸的体积,还要知道的数据是______.
(2)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁,并对产品质量进行检测.检测结果如下:
| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
(3)该小组在继续研究由绿矾制备Fe(OH)2的过程中,发现出现白色的沉淀会逐渐转变为灰绿色,最后变为红褐色.甲同学查资料该灰绿色沉淀可能是Fe3(OH)8,请用氧化物的形式写出该沉淀______;乙同学查资料后认为该灰绿色沉淀是由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3的缘故,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路______.
 查看习题详情和答案>>
查看习题详情和答案>>
绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.请回答下列问题:
(1)右图锥形瓶中的反应物是铁屑和28%的硫酸,反应前常用98%的硫酸配制500g 28%的硫酸,要算出所需98%的硫酸的体积,还要知道的数据是______.
(2)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁,并对产品质量进行检测.检测结果如下:
已知产品质量标准:Fe3+的质量分数等于0.005%,产品质量定为Ⅰ级;Fe3+的质量分数等于0.01%,产品质量定为Ⅱ级,从实验结果中,可得出制备硫酸亚铁溶液时,反应控制______过量为最佳.
(3)该小组在继续研究由绿矾制备Fe(OH)2的过程中,发现出现白色的沉淀会逐渐转变为灰绿色,最后变为红褐色.甲同学查资料该灰绿色沉淀可能是Fe3(OH)8,请用氧化物的形式写出该沉淀______;乙同学查资料后认为该灰绿色沉淀是由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3的缘故,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路______.
查看习题详情和答案>>
(1)右图锥形瓶中的反应物是铁屑和28%的硫酸,反应前常用98%的硫酸配制500g 28%的硫酸,要算出所需98%的硫酸的体积,还要知道的数据是______.
(2)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁,并对产品质量进行检测.检测结果如下:
| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
(3)该小组在继续研究由绿矾制备Fe(OH)2的过程中,发现出现白色的沉淀会逐渐转变为灰绿色,最后变为红褐色.甲同学查资料该灰绿色沉淀可能是Fe3(OH)8,请用氧化物的形式写出该沉淀______;乙同学查资料后认为该灰绿色沉淀是由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3的缘故,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路______.
