摘要:3.试题难度与分值 试题类型 难度系数 分 值 容易题 0.85以上 约70分 稍难题 0.65~0.85 约20分 较难题 0.50~0.65 约10分
网址:http://m.1010jiajiao.com/timu3_id_277023[举报]
硫元素具有可变价态,据此完成以下有关含硫化合物性质的试题.
(1)将H2S气体通入FeCl3溶液中,现象是 ;反应的离子方程式是 .
(2)为了探究-2价硫的化合物与+4价硫的化合物反应的条件,设计了下列实验.
已知:电离平衡常数:H2S K1=1.3×10-7;K2=7.1×10-15
H2SO3 K1=1.7×10-2;K2=5.6×10-8
①根据上述实验,可以得出结论:在 条件下,+4价硫的化合物可以氧化-2价硫的化合物.
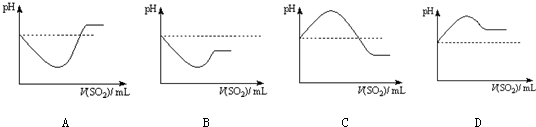
②将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是 (选填编号).
(3)现有试剂:溴水、硫化钠溶液、Na2SO3溶液、稀硫酸、NaOH溶液、氨水.要证明Na2SO3具有还原性,应选用的试剂有 ,看到的现象是 .要证明Na2SO3具有氧化性,应选用的试剂有 ,反应的离子方程式是 .
(4)文献记载,常温下H2S可与Ag发生置换反应生成H2.现将H2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H2S与Ag发生了置换反应 .
查看习题详情和答案>>
(1)将H2S气体通入FeCl3溶液中,现象是
(2)为了探究-2价硫的化合物与+4价硫的化合物反应的条件,设计了下列实验.
| 实验操作 | 实验现象 | |
| 实验1 | 将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 | 无明显现象 |
| 实验2 | 将H2S通入Na2SO3溶液中 | 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 | 将SO2通入Na2S溶液中 | 有浅黄色沉淀产生 |
H2SO3 K1=1.7×10-2;K2=5.6×10-8
①根据上述实验,可以得出结论:在
②将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是

(3)现有试剂:溴水、硫化钠溶液、Na2SO3溶液、稀硫酸、NaOH溶液、氨水.要证明Na2SO3具有还原性,应选用的试剂有
(4)文献记载,常温下H2S可与Ag发生置换反应生成H2.现将H2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H2S与Ag发生了置换反应
用Na2SO3可以治理工业SO2尾气污染,这是一种治理SO2污染比较新颖的方法.具体操作:①将含有SO2气体的尾气通入到Na2SO3溶液中,发生化合反应生成NaHSO3;②将反应后的溶液加热,即可逸出SO2气体,这些SO2可以应用于制取H2SO4.该方法中Na2SO3可以循环使用,符合绿色化学的基本原则.请根据上述信息解答下列试题:
(1)写出①、②两步的化学方程式:①
(2)当89.6m3(标准状况)含有SO2的尾气通入溶液中时,恰好与10m3的0.1mol/L的Na2SO3溶液发生反应.求该尾气中SO2气体的体积分数.
查看习题详情和答案>>
(1)写出①、②两步的化学方程式:①
Na2SO3+SO2+H2O=2NaHSO3
Na2SO3+SO2+H2O=2NaHSO3
;②2NaHSO3
Na2SO3+SO2↑+H2O
| ||
2NaHSO3
Na2SO3+SO2↑+H2O
.
| ||
(2)当89.6m3(标准状况)含有SO2的尾气通入溶液中时,恰好与10m3的0.1mol/L的Na2SO3溶液发生反应.求该尾气中SO2气体的体积分数.
硅在材料王国中具有举足轻重的位置.请解答下列试题:
(1)硅的制备方法是制约太阳能发展的瓶颈,硅的制备原料是石英砂,石英与焦炭在高温电炉中反应可以制得硅.该反应的化学方程式是 ,该反应的气体产物是一氧化碳,不是二氧化碳,其原因是 .
(2)氮化硅Si3N4是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取.粉末状Si3N4对空气和水都不稳定.但将粉末状的Si3N4和适量氧化镁在230×1.01×l05Pa和185℃的密闭容器中热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到对水不稳定的Mg3N2.
①写出由SiCl4和NH3反应制取Si3N4的化学反应方程式 ;
②现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,使生成的Si3N4沉积在石墨表面可得较高纯度的氮化硅,该制造方法称为: ;反应的化学方程式为 ;该法还可制造金刚石薄膜,反应的化学方程式为 .
③在Si3N4和适量氧化镁在230×1.01×105 Pa和185℃的密闭容器中热处理的过程中,除生成Mg3N2外,还可能生成 物质.热处理后除去MgO和Mg3N2的方法是 .
查看习题详情和答案>>
(1)硅的制备方法是制约太阳能发展的瓶颈,硅的制备原料是石英砂,石英与焦炭在高温电炉中反应可以制得硅.该反应的化学方程式是
(2)氮化硅Si3N4是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取.粉末状Si3N4对空气和水都不稳定.但将粉末状的Si3N4和适量氧化镁在230×1.01×l05Pa和185℃的密闭容器中热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到对水不稳定的Mg3N2.
①写出由SiCl4和NH3反应制取Si3N4的化学反应方程式
②现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,使生成的Si3N4沉积在石墨表面可得较高纯度的氮化硅,该制造方法称为:
③在Si3N4和适量氧化镁在230×1.01×105 Pa和185℃的密闭容器中热处理的过程中,除生成Mg3N2外,还可能生成
高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)?Fe(s)+CO2(g)△H>0
其平衡常数可表示为K=c(CO2)/c(CO),已知1 100℃时K=0.263,且化学平衡常数只与温度有关,不随浓度和压强的变化而变化.
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值
(2)1 100℃时测得高炉中c(CO2)=0.025mol?L-1,c(CO)=0.1mol?L-1,在这种情况下,该反应是否处于化学平衡状态
(3)试通过计算当20L的高炉中,通入10molCO和矿石在1 100℃时达平衡时,CO的转化率?
查看习题详情和答案>>
其平衡常数可表示为K=c(CO2)/c(CO),已知1 100℃时K=0.263,且化学平衡常数只与温度有关,不随浓度和压强的变化而变化.
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值
增大
增大
,平衡常数K值增大
增大
(均填“增大”、“减小”或“不变”).(2)1 100℃时测得高炉中c(CO2)=0.025mol?L-1,c(CO)=0.1mol?L-1,在这种情况下,该反应是否处于化学平衡状态
否
否
(填“是”或“否”).此时,化学反应速率是v正大于
大于
v逆(填“大于”、“小于”或“等于”),其原因是因难度商Qc=
=
=0.25<K=0.263,温度不变,K值不变,为增大
比值,v(正)大于v(逆)
| c(CO2) |
| c(CO) |
| 0.025mol/L |
| 0.1mol/L |
| c(CO2) |
| c(CO) |
因难度商Qc=
=
=0.25<K=0.263,温度不变,K值不变,为增大
比值,v(正)大于v(逆)
.| c(CO2) |
| c(CO) |
| 0.025mol/L |
| 0.1mol/L |
| c(CO2) |
| c(CO) |
(3)试通过计算当20L的高炉中,通入10molCO和矿石在1 100℃时达平衡时,CO的转化率?