摘要:23.0.15mol某金属单质与足量的稀硫酸充分作用后.在标准状况下生成5.04L氢气和25.65g该金属的硫酸盐.若该金属原子核内的质子数比中子数少1个.试通过计算推导出该元素的原子序数.并指出其在周期表中的位置.
网址:http://m.1010jiajiao.com/timu3_id_276090[举报]
氨在国民经济中占有重要的地位,2008年,我国氨产量接近500万吨.下图是合成氨的简要流程.

(1)下表是空气中部分气体的沸点.将空气液化加热分馏,依据下表数据判断,最先气化得到的气体是
(2)天然气、重油、煤都可以与水反应制得氢气.下表是某合成氨厂采用不同原料的相对投资和能量消耗.
①依据上表信息,你认为采用
②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ?mol-1;
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ?mol-1;
试写出由C于水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式
(3)下表是在某种催化剂作用下用体积比为1:3的氮、氢混合气反应应达到平衡时的一些实验数据.
①依据表中数据判断,合成氨反应N2+3H2 2NH3的△H
2NH3的△H
②该反应的化学平衡常数表达式为
.
③在300℃、10MPa下,合成氨反应达到平衡时,混合气体的体积是反应开始时的
查看习题详情和答案>>

(1)下表是空气中部分气体的沸点.将空气液化加热分馏,依据下表数据判断,最先气化得到的气体是
氦气
氦气
.| 气体名称 | 氨气 | 氧气 | 氦气 | 氖气 | 氩气 | 氪气 | 氚气 |
| 沸点/℃ | -196 | -183 | -269 | -264 | -186 | -153 | -108 |
| 原料 | 天然气 | 重油 | 煤 |
| 相对投资费用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J?t-1 | 28×109 | 38×109 | 48×109 |
天然气
天然气
为原料最好.②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:
CH4+H2O
CO+3H2
| ||
| 高温 |
CH4+H2O
CO+3H2
.
| ||
| 高温 |
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ?mol-1;
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ?mol-1;
试写出由C于水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式
C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ?mol-1
C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ?mol-1
.(3)下表是在某种催化剂作用下用体积比为1:3的氮、氢混合气反应应达到平衡时的一些实验数据.
| NH3含量% 压强/MPa 温度/℃ |
0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
 2NH3的△H
2NH3的△H<
<
(填“>”、“<”或“无法判断”)0,请简要说明理由相同条件下,升高温度,NH3含量减小,平衡左移,逆反应吸热,正反应放热
相同条件下,升高温度,NH3含量减小,平衡左移,逆反应吸热,正反应放热
;②该反应的化学平衡常数表达式为
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
③在300℃、10MPa下,合成氨反应达到平衡时,混合气体的体积是反应开始时的
0.66
0.66
倍.(2012?开封一模)[选修2-化学与技术]合成氨的流程示意图如下:

回答下列问题:
(1)设备A中含有电加热器,触媒和热交换器,其中发生的化学反应方程式为
(2)设备B中m和n是两个通水口,入水口是
(3)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是
(4)天然气、重油、煤都可以与水反应制得氢气.下表是某合成氨厂采用不同原料的相对投资和能量消耗.
①依据上表信息,你认为采用
②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ/mol;
2CO2(g)+O2(g)═CO2(g)△H=-566kJ/mol;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol;
试写出由C与水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式
(5)在合成氨生产中,将生成的氨及时从反应后的气体中分离出来.运用化学平衡的知识分析这样做的理由:
查看习题详情和答案>>

回答下列问题:
(1)设备A中含有电加热器,触媒和热交换器,其中发生的化学反应方程式为
N2+3H2
2NH3
| 催化剂 |
| 高温高压 |
N2+3H2
2NH3
,设备A的名称是| 催化剂 |
| 高温高压 |
合成塔
合成塔
;(2)设备B中m和n是两个通水口,入水口是
n
n
(填“m”或“n”).不宜从相反方向通水的原因是高温气体从冷却塔的上端进入,冷却水应从下端进入,逆向冷却效果好
高温气体从冷却塔的上端进入,冷却水应从下端进入,逆向冷却效果好
;(3)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是
液化
液化
,分馏
分馏
;(4)天然气、重油、煤都可以与水反应制得氢气.下表是某合成氨厂采用不同原料的相对投资和能量消耗.
| 原料 | 天然气 | 重油 | 煤 |
| 相对投资费用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J?t-1 | 28109 | 38109 | 48109 |
天然气
天然气
为原料最好;②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:
CH4+H2O
CO+3H2
| ||
| 催化剂 |
CH4+H2O
CO+3H2
;
| ||
| 催化剂 |
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ/mol;
2CO2(g)+O2(g)═CO2(g)△H=-566kJ/mol;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol;
试写出由C与水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式
C(S)+H2O(g)
CO(g)+H2(g) △H=+131KJ/mol
| ||
C(S)+H2O(g)
CO(g)+H2(g) △H=+131KJ/mol
;
| ||
(5)在合成氨生产中,将生成的氨及时从反应后的气体中分离出来.运用化学平衡的知识分析这样做的理由:
移走氨气,减小生成物浓度,平衡右移,有利于氨合成
移走氨气,减小生成物浓度,平衡右移,有利于氨合成
.
在常温下,某兴趣小组模拟“侯氏制碱法”制取碳酸钠,流程如下: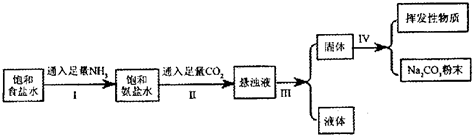
在常温下,有关物质的溶解度为:
(1)操作Ⅲ中的实验操作名称为 ;
(2)操作I和操作II总反应的离子方程式为 ;
(3)操作I和II不能颠倒的原因 ;
(4)检验所得的碳酸钠粉末是否含有NaHCO3,的实验方案是(写出操作步骤、现象、结论): ;
(5)为了测定所制取产物的纯度(假设杂质只有碳酸氢钠).该小组的实验步骤为:
i.使用下列装置组装实验装置,并检查气密性;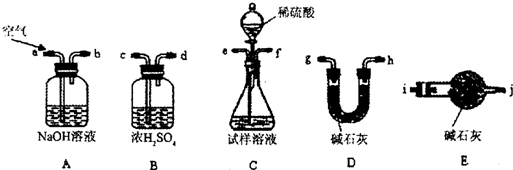
ii.称取Wg产品放入C装置的锥形瓶中,加适量蒸馏水溶解
iii.称量D装置的质量为W1g
iv.从分液漏斗滴入稀硫酸,直到不再产生气体为止
v.从a处缓缓鼓入一定量的空气,再次称量D装置质量为W2g.
vi.重复步骤v的操作,直到D装置的质量不再改变,称得D装置的质量为W3g.
根据上述实验回答如下问题:
①第i步,使用上述装置连接的接口顺序为:(b)→(e)(f)→ →
②产物中碳酸钠的质量分数为(数字可不必化简) .
查看习题详情和答案>>

在常温下,有关物质的溶解度为:
| 物质 | NH4Cl | NaHCO3 | Na2CO3 | NaCl |
| 溶解度/g | 37.2 | 9.6 | 21.5 | 36.0 |
(2)操作I和操作II总反应的离子方程式为
(3)操作I和II不能颠倒的原因
(4)检验所得的碳酸钠粉末是否含有NaHCO3,的实验方案是(写出操作步骤、现象、结论):
(5)为了测定所制取产物的纯度(假设杂质只有碳酸氢钠).该小组的实验步骤为:
i.使用下列装置组装实验装置,并检查气密性;

ii.称取Wg产品放入C装置的锥形瓶中,加适量蒸馏水溶解
iii.称量D装置的质量为W1g
iv.从分液漏斗滴入稀硫酸,直到不再产生气体为止
v.从a处缓缓鼓入一定量的空气,再次称量D装置质量为W2g.
vi.重复步骤v的操作,直到D装置的质量不再改变,称得D装置的质量为W3g.
根据上述实验回答如下问题:
①第i步,使用上述装置连接的接口顺序为:(b)→(e)(f)→
②产物中碳酸钠的质量分数为(数字可不必化简)
(2008?佛山二模)实验室常用铜片、稀硫酸和浓硝酸来制备五水硫酸铜:Cu+2HNO3+H2SO4=CuSO4+2NO2↑+2H2O分以下几个步骤:
①将盛有4.5g铜屑的蒸发皿置于酒精灯火焰上,灼烧至表面呈现黑色,冷却;
②加16mL3mol?L-1硫酸,再缓慢、分批加入7mL12mol?L-1硝酸(在通风橱进行);
③待反应缓和后,盖上表面皿,用水浴加热至铜屑全溶;
④倾析法趁热将溶液转移到另一蒸发皿中,并在水浴上浓缩到溶液出现晶膜,冷却,过滤;
…
请回答下列问题:
(1)将铜屑灼烧的目的是
(2)加入硝酸时,必须缓慢、分批加入的目的是
(3)控制硝酸总量尽可能小除了环保和节约原料外,还可能的原因是
(4)下图是硫酸铜和硝酸铜的溶解度表(单位:g),请根据表回答:
①步骤④溶液冷却时析出的晶体主要是
②将五水硫酸铜粗产品提纯,要采取的实验方法是
(5)实验中取用蒸发皿的仪器是
(6)如不用水浴加热蒸发,五水硫酸铜晶体可能会因温度高转变为白色的硫酸铜,此过程属于
查看习题详情和答案>>
①将盛有4.5g铜屑的蒸发皿置于酒精灯火焰上,灼烧至表面呈现黑色,冷却;
②加16mL3mol?L-1硫酸,再缓慢、分批加入7mL12mol?L-1硝酸(在通风橱进行);
③待反应缓和后,盖上表面皿,用水浴加热至铜屑全溶;
④倾析法趁热将溶液转移到另一蒸发皿中,并在水浴上浓缩到溶液出现晶膜,冷却,过滤;
…
请回答下列问题:
(1)将铜屑灼烧的目的是
除去表面的油污
除去表面的油污
,表面的黑色物质是氧化铜
氧化铜
.(2)加入硝酸时,必须缓慢、分批加入的目的是
防止反应剧烈,有液体溅出;避免硝酸分解
防止反应剧烈,有液体溅出;避免硝酸分解
.(3)控制硝酸总量尽可能小除了环保和节约原料外,还可能的原因是
避免引入过多NO3-,影响后面的实验
避免引入过多NO3-,影响后面的实验
.(4)下图是硫酸铜和硝酸铜的溶解度表(单位:g),请根据表回答:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| CuSO4?5H2O | 23.1 | 32.0 | 44.6 | 61.8 | 83.8 | 114.0 |
| Cu(NO3)2?xH2O | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 |
五水硫酸铜
五水硫酸铜
.②将五水硫酸铜粗产品提纯,要采取的实验方法是
重结晶
重结晶
.(5)实验中取用蒸发皿的仪器是
坩埚钳
坩埚钳
,使用蒸发皿时的注意事项是避免骤冷导致蒸发皿破裂或蒸发溶液时蒸发皿中溶液的体积不超过它体积的2/3或蒸发溶液时不能蒸干等
避免骤冷导致蒸发皿破裂或蒸发溶液时蒸发皿中溶液的体积不超过它体积的2/3或蒸发溶液时不能蒸干等
.(只需写出一项)(6)如不用水浴加热蒸发,五水硫酸铜晶体可能会因温度高转变为白色的硫酸铜,此过程属于
化学
化学
变化.(填“物理”或“化学”)Ⅰ.如图所示是分离混合物时常用的仪器,回答下列问题:

(1)写出仪器A、C、E的名称
(2)分离以下混合物应该主要选用什么仪器?(填字母符号)
食用油和酒精:
Ⅱ.实验室用固体烧碱配制200mL 0.5mol?L-1的NaOH溶液.
(1)需称量
(2)完成此配制实验,除了量筒,烧杯,玻璃棒外还需要的常见的玻璃仪器有
(3)请描述定容操作应采取的具体方法
查看习题详情和答案>>

(1)写出仪器A、C、E的名称
蒸馏烧瓶、分液漏斗、冷凝管
蒸馏烧瓶、分液漏斗、冷凝管
(2)分离以下混合物应该主要选用什么仪器?(填字母符号)
食用油和酒精:
AE
AE
汽油和水:C
C
Ⅱ.实验室用固体烧碱配制200mL 0.5mol?L-1的NaOH溶液.
(1)需称量
5.0
5.0
g 烧碱,应放在烧杯
烧杯
中称量、溶解.(2)完成此配制实验,除了量筒,烧杯,玻璃棒外还需要的常见的玻璃仪器有
250mL容量瓶、胶头滴管
250mL容量瓶、胶头滴管
(3)请描述定容操作应采取的具体方法
向容量瓶内注入蒸馏水至刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线正好水平相切
向容量瓶内注入蒸馏水至刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线正好水平相切
.