摘要:17. “铝热反应 的化学方程式为:2Al+ Fe2O3 高温 Al2O3+ 2Fe.某同学对“铝热反应 的现象有这样的描述:“反应放出大量的热.并发出耀眼的光芒 .“纸漏斗的下部被烧穿.有熔融物落入沙中 .查阅知.Al.Al2O3.Fe.Fe2O3熔点.沸点数据如下: 物质 Al Al2O3 Fe Fe2O3 熔点/℃ 660 2054 1535 1462 沸点/℃ 2467 2980 2750 -- (1) 该同学推测.铝热反应所得到的熔融物应是铁铝合金.这种推测有一定的道理.理由是: . (2) 设计一个简单的实验方案.证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是 .当观察到 现象时.说明熔融物中含有金属铝.反应的离子方程式为 . (3) 实验室溶解该熔融物.最好选用下列试剂中的 . A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液 人教版必修2第四章测试题(A卷)
网址:http://m.1010jiajiao.com/timu3_id_275960[举报]
|
某集团所属铝母铸造分厂发生铝水外溢事故,共造成9人死亡、64人受伤.关于金属铝,下列说法正确的是 | |
| [ ] | |
A. |
冶炼金属铝时铝水温度极高,如外溢极易引发事故 |
B. |
等量的铝分别与足量的盐酸和氢氧化钠溶液反应,消耗酸和碱的物质的量之比为1∶2 |
C. |
将一铝片投入浓硫酸中没有气体产生,说明铝不与浓硫酸反应 |
D. |
发生铝热反应时,铝被置换出来 |
已知D、M、H是常见的非金属单质,其中M是无色气体,H是有色气体,J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素),A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,B与C反应时,每生成1molH同时消耗4molB和1molC,K只知含有CO 或CO2中的一种或两种.它们关系如图:

(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
②
⑤
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为

查看习题详情和答案>>

(1)写出下列物质的化学式:A
Fe3O4
Fe3O4
DC
C
(2)写出下列反应的化学方程式:
②
PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O
PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O
⑤
2HClO═2HCl+O2↑
2HClO═2HCl+O2↑
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用
②
②
方法(填序号)①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为
8mol
8mol
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为
PbO2+2e-+4H++SO42-═PbSO4+2H2O
PbO2+2e-+4H++SO42-═PbSO4+2H2O
当反应转移1mol电子时,负极质量增加48
48
g.
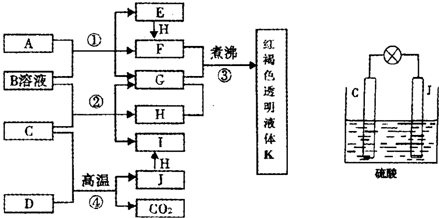
已知D、H是常见的非金属单质,其中H是黄绿色气体.J是一种金属单质,J元素的+2价化合物比+4价化合物稳定.D、J元素在周期表中同主族,D是形成化合物种类最多的元素.A、C是金属氧化物,C和J均是某种常见电池的电极材料,B与C反应时,每生成1mol H同时消耗4mol B和1mol C.它们之间的关系如图:
(1)写出物质A的化学式
(2)写出反应②的化学方程式
(3)由金属氧化物A和C得到其相应的金属单质,在冶金工业上一般可用
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可以用铝热法,若反应中lmolA参加反应,转移电子的物质的量为
(4)用C、J作电极,与硫酸构成如图所示电池,工作时电池发生的总反应式为
(5)向框图中的红褐色透明液体K中逐滴滴入HCl溶液.可以观察到先产生红褐色沉淀,后红褐色沉淀溶解,请解释原因
查看习题详情和答案>>
(1)写出物质A的化学式
Fe3O4
Fe3O4
.(2)写出反应②的化学方程式
PbO2+4HCl=PbCl2+Cl2↑+2H2O
PbO2+4HCl=PbCl2+Cl2↑+2H2O
.(3)由金属氧化物A和C得到其相应的金属单质,在冶金工业上一般可用
②
②
方法(填序号).①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可以用铝热法,若反应中lmolA参加反应,转移电子的物质的量为
8
8
mol.(4)用C、J作电极,与硫酸构成如图所示电池,工作时电池发生的总反应式为
Pb+PbO2+2H2SO4=2PbSO4+2H2O
Pb+PbO2+2H2SO4=2PbSO4+2H2O
,当反应转移1mol电子时,溶液中消耗H+的物质的量为2
2
mol.(5)向框图中的红褐色透明液体K中逐滴滴入HCl溶液.可以观察到先产生红褐色沉淀,后红褐色沉淀溶解,请解释原因
开始加盐酸时,氢氧化铁胶体遇电解质发生聚沉,再继续滴加则氢氧化铁沉淀与盐酸发生酸碱中和反应,沉淀溶解
开始加盐酸时,氢氧化铁胶体遇电解质发生聚沉,再继续滴加则氢氧化铁沉淀与盐酸发生酸碱中和反应,沉淀溶解
