摘要:6. 室温下.下列四种溶液.①氢离子浓度为1mol/L的醋酸 ②0.1mol/L的盐酸 3 0.01mol/L的氢氧化钠溶液 ④氢氧根离子浓度为0.001mol/L的氨水.由电离出的氢离子浓度之比为 ( ) A.1:10:100:1000 B.0:1:12:11 C.14:13:12:11 D.14:13:2:3
网址:http://m.1010jiajiao.com/timu3_id_275044[举报]
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡.请根据所学知识回答下列问题:
(1)NaHCO3溶液中共存在7种微粒,它们是Na+、HCO3-、H+、CO32-、H2O、
(2)常温时,Al2(SO4)3的水溶液呈
(3)常温下,物质的量浓度相同的下列溶液:①NH4Cl ②(NH4)2SO4 ③NH3?H2O ④(NH4)2CO3 ⑤NH4HSO4.溶液中c(NH4+)从大到小的顺序为:
(4)现有浓度均为0.1mol/L的下列溶液:①氢氧化钡;②醋酸;③氢氧化钠;④碳酸钠,四种溶液中由水电离出的OH-浓度由大到小的顺序是(填序号
查看习题详情和答案>>
(1)NaHCO3溶液中共存在7种微粒,它们是Na+、HCO3-、H+、CO32-、H2O、
OH-、
OH-、
、H2CO3
H2CO3
.(填写微粒符号)(2)常温时,Al2(SO4)3的水溶液呈
酸
酸
(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
;实验室在配制Al2(SO4)3的溶液时,为了抑制Al2(SO4)3的水解可加入少量的硫酸
硫酸
(填写物质的名称).把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是Al2O3
Al2O3
.(3)常温下,物质的量浓度相同的下列溶液:①NH4Cl ②(NH4)2SO4 ③NH3?H2O ④(NH4)2CO3 ⑤NH4HSO4.溶液中c(NH4+)从大到小的顺序为:
②>④>⑤>①>③
②>④>⑤>①>③
.(填写溶液的序号)(4)现有浓度均为0.1mol/L的下列溶液:①氢氧化钡;②醋酸;③氢氧化钠;④碳酸钠,四种溶液中由水电离出的OH-浓度由大到小的顺序是(填序号
④>②>③>①
④>②>③>①
. I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是
H2CO3、CO32-
H2CO3、CO32-
.(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点…
指示剂B的变色范围在pH=
4.5
4.5
左右最理想.(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是
HCO3-+H+=H2CO3
HCO3-+H+=H2CO3
.(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=
c(
| ||
c(
|
10
10
.II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A
 H++HA- HA-
H++HA- HA- H++A2-
H++A2-已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(5)c(H+)最大的是
A
A
,c(H2A)最大的是C
C
,c(A2-)最大的是D
D
.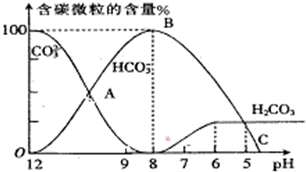 I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是______.
(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点…
指示剂B的变色范围在pH=______左右最理想.
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是______.
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=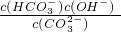 =2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A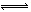 H++HA- HA-
H++HA- HA- H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(5)c(H+)最大的是______,c(H2A)最大的是______,c(A2-)最大的是______.
查看习题详情和答案>>
常温下,0.1mol/L的下列溶液:①HCl ②NaCl ③CH3COONa ④NaOH ⑤FeCl3.
(1)pH由小到大排列顺序为
(2)实验室配制⑤的溶液时常需加入少量盐酸,否则得到的是浑浊的溶液,产生浑浊的原因是(用离子方程式表示)
(3)物质的量浓度相同的①氨水②氯化铵③碳酸氢铵④硫酸氢铵在上述四种溶液中,铵根离子物质的量浓度由大到小的顺序是
(4)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
查看习题详情和答案>>
(1)pH由小到大排列顺序为
①<⑤<②<③<④
①<⑤<②<③<④
(填序号);(2)实验室配制⑤的溶液时常需加入少量盐酸,否则得到的是浑浊的溶液,产生浑浊的原因是(用离子方程式表示)
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
;(3)物质的量浓度相同的①氨水②氯化铵③碳酸氢铵④硫酸氢铵在上述四种溶液中,铵根离子物质的量浓度由大到小的顺序是
NH4HSO4、NH4Cl、NH4HCO3、NH3?H2O
NH4HSO4、NH4Cl、NH4HCO3、NH3?H2O
;(4)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
N2(g)+3H2(g)=2NH3(g)△H=-92kJ/mol
N2(g)+3H2(g)=2NH3(g)△H=-92kJ/mol
. 铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O.
铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O.(1)为确定某温度下Cu(OH)2固体的分解产物.称取9.8gCu(OH)2样品,将该样品在坩埚中加热完全分解,冷却至室温后,测得剩余固体质量为7.6g,该固体的成分为
(2)科学研究发现Cu2O可作为太阳光分解水的催化剂.
Ⅰ通过以下四种方法来制备Cu2O.
a.火法还原:用炭粉在高温条件下还原CuO;
b.用CH3CHO还原新制电解的Cu(OH)2;
c.电解法:2Cu+H2O
| ||
d.最新实验研究用肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2.
①该制法的化学方程式为
②肼性质与氨气相似,易溶于水,可发生如下两步电离过程:
N2H4+H2O?N2H5++OH- I
N2H5++H2O?N2H62++OH- II
常温下,某浓度N2H6C12溶液的pH为4,则该溶液中由水电离产生的c(H+)为
已知在相同条件下过程I的进行程度大于N2H5+的水解程度.常温下,若0.2mol/L N2H4溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H5+、Cl-、OH-、H+离子浓度由大到小的顺序为
Ⅱ用制得的Cu2O进行催化分解水的实验.
用以上四种方法制得的Cu2O在相同条件下分别对水进行催化分解,产生氢气的体积V(H2)随时间t变化如图所示,则下列说法正确的是
A.c、d方法制得的Cu2O催化效率相对较高
B.d方法制得的Cu2O作催化剂时,水的平衡转化率最高
C.催化效果与Cu2O颗粒的粗细、表面活性等有关
D.分解等物质的量的水时,d方法制得的Cu2O作催化剂所需吸收的能量最低.