摘要:20. 10 0C时加热NaHCO3饱和溶液.测得该溶液的PH发生如下变化: 温度(0C) 10 20 30 加热煮沸后冷却到50 0C PH 8.3 8.4 8.5 8.8 甲认为.该溶液的PH升高的原因是HCO3-离子的水解程度增大.所以碱性增强,该反应的离子方程式为 ,乙认为.溶液PH升高的原因是NaHCO3受热分解.生成了Na2CO3.并推断Na2CO3的水解程度 NaHCO3.丙认为甲.乙的判断都不准确.丙认为: (1)只要在加热煮沸的溶液中加入足量的试剂X.如果产生白色沉淀.则 判断正确.该试剂是 A.氢氧化钡溶液 B.氯化钡溶液 C.氢氧化钠溶液 D.澄清石灰水 (2)将加热后的溶液冷却到10 0C.若溶液的PH等于8.3.则 . (3)查阅资料发现.NaHCO3的分解温度为1500C.丙断言 的判断是错误的.理由是 .
网址:http://m.1010jiajiao.com/timu3_id_274947[举报]
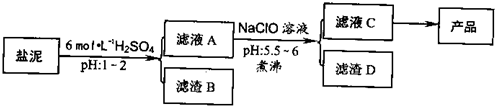
(2009?深圳二模)氯碱厂废渣(盐泥)中含有镁钙铁铝的硅酸盐和碳酸盐,其中含镁(以MgO计)约10%,钙(以CaO计)约15%,铁(Ⅱ、Ⅲ)和铝等的含量低于1%.氯碱厂从盐泥中提取MgSO4.7H2O的流程如下:
部分阳离子以氢氧化物沉淀时溶液pH
溶解度表
回答下列问题: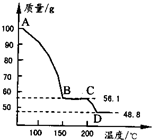
(1)滤渣B的主要成分是:
(2)从滤液A得到滤液C,能否用氨水代替NaClO?
(3)从滤液C中获得产品经过3个操作步骤,分别是
(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式
查看习题详情和答案>>

部分阳离子以氢氧化物沉淀时溶液pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 11.2 |
| 温度0C | 10 | 30 | 40 |
| CaSO4 | 0.19 | 0.21 | 0.21 |

(1)滤渣B的主要成分是:
H2SiO3(或H4SO4)\CaSO4(或CaSO4?2H2O)
H2SiO3(或H4SO4)\CaSO4(或CaSO4?2H2O)
.(2)从滤液A得到滤液C,能否用氨水代替NaClO?
否
否
,什么理由氨水不能将Fe2+氧化成Fe3+,则无法沉淀完全
氨水不能将Fe2+氧化成Fe3+,则无法沉淀完全
,其中加热煮沸的目的是加热能使Fe3+和Al3+水解完全,同时因为氢氧化铁和氢氧化铝是胶状沉淀,加热有利于破坏胶体的稳定性,使沉淀颗粒变大利于后面过滤分离
加热能使Fe3+和Al3+水解完全,同时因为氢氧化铁和氢氧化铝是胶状沉淀,加热有利于破坏胶体的稳定性,使沉淀颗粒变大利于后面过滤分离
.(3)从滤液C中获得产品经过3个操作步骤,分别是
加热浓缩
加热浓缩
,冷却结晶
冷却结晶
,过滤
过滤
.(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式
MgSO4?H2O
MgSO4+H2O↑
| ||
MgSO4?H2O
MgSO4+H2O↑
.
| ||
(8分)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O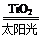 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O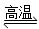 CO+3H2
CO+3H2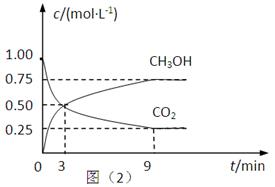
(2)CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化如上图所示。
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化如上图所示。
①从3 min到9 min,v(H2)=________mol·L-1·min-1。
②能说明上述反应达到平衡状态的是____________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g) CH3OH(g)的平衡常数:
CH3OH(g)的平衡常数:
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高 查看习题详情和答案>>
氯碱厂废渣(盐泥)中含有镁钙铁铝的硅酸盐和碳酸盐,其中含镁(以MgO计)约10%,钙(以CaO计)约15%,铁(Ⅱ、Ⅲ)和铝等的含量低于1%.氯碱厂从盐泥中提取MgSO4.7H2O的流程如下:
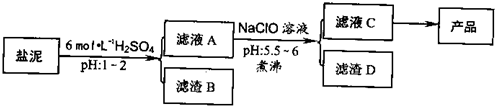
部分阳离子以氢氧化物沉淀时溶液pH
溶解度表
回答下列问题:
(1)滤渣B的主要成分是:______.
(2)从滤液A得到滤液C,能否用氨水代替NaClO?______,什么理由______,其中加热煮沸的目的是______.
(3)从滤液C中获得产品经过3个操作步骤,分别是______,______,______.
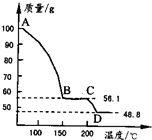
(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式______.
查看习题详情和答案>>

部分阳离子以氢氧化物沉淀时溶液pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 11.2 |
| 温度0C | 10 | 30 | 40 |
| CaSO4 | 0.19 | 0.21 | 0.21 |

(1)滤渣B的主要成分是:______.
(2)从滤液A得到滤液C,能否用氨水代替NaClO?______,什么理由______,其中加热煮沸的目的是______.
(3)从滤液C中获得产品经过3个操作步骤,分别是______,______,______.
(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式______.