摘要:水的电离和溶液的PH值同步素能训练答案
网址:http://m.1010jiajiao.com/timu3_id_272886[举报]
 水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是( )
水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是( )| A、纯水中25°C时的,c(H+)比100℃的时c(H+)大 | B、100℃时某溶液中由水电离产生的c(H+)═1×10-11mol?L-1,则该溶液的Ph可能是11或3 | C、将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10:1 | D、25℃时,某Na2SO4溶液中c(SO 42-)=5.0×10-4mol/L则溶液中c(Na+):c(OH-)为104:1 |
 水的电离平衡曲线如图所示.?
水的电离平衡曲线如图所示.?(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
10-14
10-14
增加到10-12
10-12
.(2)将常温下的pH=8的Ba(OH)2溶液升至100℃,则Ba(OH)2溶液的pH:
B
B
.A、>10 B、=6 C、6~8 D、>8 E、不能确定
(3)已知AnBm的离子积=[c(Am+)]n?[c(Bn-)]m?,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度幂.在某温度下,Ca(OH)2的浓度为0.02mol?L-1,其离子积为
3.2×10-5mol3/L3
3.2×10-5mol3/L3
. (2011?顺德区模拟)(1)在-50℃时,液氨存在如下电离:2NH3?NH4++NH-2,k=2×10-12,液氨的电离达到平衡时,各微粒的浓度大小关系为
(2011?顺德区模拟)(1)在-50℃时,液氨存在如下电离:2NH3?NH4++NH-2,k=2×10-12,液氨的电离达到平衡时,各微粒的浓度大小关系为c(NH3)>c(NH4+)=c(NH2-)
c(NH3)>c(NH4+)=c(NH2-)
,加入NH4Cl固体,K=
=
2×10-12(填“<”、“>”或“=”)(2)已知25℃时Ksp(AgCl)=1.8×10--10,在10mL 0.10mol/L AgNO3溶液中加入10mL0.20mol/LNaCl溶液,充分反应后溶液中的c(Ag+)=
3.6×10-9mol/L
3.6×10-9mol/L
.(3)配平硫酸亚铁加强热制备铁红和生成硫的两种常见氧化物的化学方程式:
2
2
FeSO4| 高温 |
1
1
Fe2O3+1
1
SO2↑
SO2↑
+1
1
SO3↑
SO3↑
(4)已知氯气能溶于水,溶液呈酸性.如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是
BC
BC
A.产生气体的体积:①>②
B.溶液的pH变化:①减小,②增大
C.电极上析出物质的质量:①>②
D.电极反应式:①中阳极 2Cl--2e-?Cl2↑ ②中负极 2H++2e-?H2↑
如图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有第ⅥA族和几种元素的位置.请回答下列问题:

(1)如图中将铁元素在周期表中的位置是______
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是:氢的最外层电子“饱和缺一”.请写出NaH的电子式______
(3)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,该盐溶于水时______(“抑制”、“促进”或“不影响”)水电离,其反应的离子方程式为______.
(4)下列叙述正确的是______.
A.h的最高价氧化物对应的水化物是一种强碱
B.f的氢化物比硒化氢的稳定性弱
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.相同条件下,d与f形成的化合物水溶液的pH大于d与g形成的化合物水溶液的pH,说明相同浓度氢化物水溶液的酸性f弱于g
(5)d的某化合物呈淡黄色,可与氯化亚铁溶液反应.若淡黄色固体与氯化亚铁的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为:______.
查看习题详情和答案>>

(1)如图中将铁元素在周期表中的位置是______
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是:氢的最外层电子“饱和缺一”.请写出NaH的电子式______
(3)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,该盐溶于水时______(“抑制”、“促进”或“不影响”)水电离,其反应的离子方程式为______.
(4)下列叙述正确的是______.
A.h的最高价氧化物对应的水化物是一种强碱
B.f的氢化物比硒化氢的稳定性弱
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.相同条件下,d与f形成的化合物水溶液的pH大于d与g形成的化合物水溶液的pH,说明相同浓度氢化物水溶液的酸性f弱于g
(5)d的某化合物呈淡黄色,可与氯化亚铁溶液反应.若淡黄色固体与氯化亚铁的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为:______.
查看习题详情和答案>>
(1)水的电离平衡曲线如图所示,若A点表示25°C时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度.100°C时1mol?L-1 的
NaOH溶液中,由水电离出的c(H+)=______mol?L-1,
KW(25°C)______ KW(100°C)(填“>”、“<”或“=”之一).25°C时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是______(填“促进”“抑制”或“不影响”之一).
(2)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为______.
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则c(Na+)______c(CH3COO-)(填“>”、“<”或“=”之一).
③向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:______.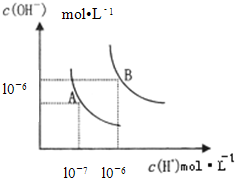
查看习题详情和答案>>
NaOH溶液中,由水电离出的c(H+)=______mol?L-1,
KW(25°C)______ KW(100°C)(填“>”、“<”或“=”之一).25°C时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是______(填“促进”“抑制”或“不影响”之一).
(2)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×l0-10 |
| CH3COOH | K=1.8×l0-5 |
| H2CO3 | K1=4.3×l0-7、K2=5.6×l0-11 |
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则c(Na+)______c(CH3COO-)(填“>”、“<”或“=”之一).
③向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:______.
