摘要:盐的性质 (1)物理性质 ①常温下一般为固体.溶解性各不相同. ②盐的水溶液多为无色,而Cu2+的盐溶液为蓝色,Fe2+的盐溶液为浅绿色. Fe3+的盐溶液为黄色 (2)化学性质 ①盐 + 活泼的金属 → 盐 + 不活泼金属 ②盐 + 酸 → 新盐 + 新酸 ③盐 +碱 → 新盐 + 新碱 ④盐 + 某些盐 → 新的两种盐
网址:http://m.1010jiajiao.com/timu3_id_25923[举报]
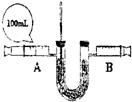 37、氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.
37、氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.(1)你认为用这种方法制氧气的优点是
常温下进行,节约能源、消耗人呼出的二氧化碳
;(2)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如下,请回答下列相关问题:
①简述检查装置气密性的方法
推动A注射器的活塞,则B中活塞向右移动则气密性良好
;②向U形管内盛装过量的Na2O2药品,注射器中为二氧化碳气体,连接好装置.药品为什么需过量
确保二氧化碳完全反应,得到纯净的氧气
;③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,
说明反应
放热
(填“吸热”或“放热”),同时还可以观察到固体粉末发生变化的现象是黄色变白
;(3)小红同学通过查阅资料了解到Na2O2还能与水反应,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.于是她根据这一原理设计了一种测定Na2O2的纯度的方法:①称取20g样品于一只质量为45g的锥形瓶中;②一次性加入20mL蒸馏水后将锥形瓶放置在电子天平上,观察显示数字的变化,并记录(数据见下表);③进行计算.

a.从上表数据判断,
240
秒时已经反应完全;b.请你帮小红同学计算此样品中Na2O2的纯度为
78%
(不需要写出计算过程).(4)Na2O2露置在空气中容易发生变质,如何检验已经变质,简述实验方法、现象和结论.
取样品少许于试管中,加入稀盐酸,若产生气体,通入石灰水,石灰石变浑浊,说明已变质
.某班同学在实验室进行二氧化碳的制取和性质实验,发现实验桌上已摆放了如下图所示的仪器可供选用:
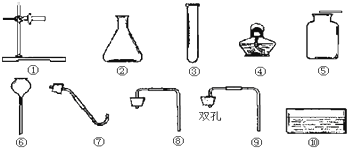
(1)要制取大量的CO2,反应过程要便于添加液态的反应物,组合一套符合要求的装置来制取CO2,你选用的仪器组合是
(2)下列是同学们对实验室制取CO2药品选择的讨论,你认为正确的是
①不能用浓盐酸,因为浓盐酸易挥发,使氯化氢气体混入二氧化碳气体中.
②一般不选用碳酸钠粉末,因为它与酸反应速度太快,不便于收集.
③可用木炭和氧气反应,因为反应可生成二氧化碳.
④可用稀盐酸与石灰石反应,因为反应速度适中,条件要求不高,气体产物纯净,易于收集.
(3)将集满CO2气体的试管倒插入水中并轻轻振荡试管,可观察到的现象是
(4)用制取二氧化碳的气体发生装置还可以制取其它气体.请举出一例:可制取的气体是
(5)以上仪器也可用于实验室制取氨气.实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液呈碱性.
①制取氨气反应的方程式:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2X.X的化学式为:
②实验室制取并收集NH3,可以从上图中选择仪器进行组装,除选择①③⑤外,还必须用到的仪器是
③NH3是一种碱性气体,干燥时不能选用下列干燥剂中的
A.固体氢氧化钠 B.浓硫酸 C.生石灰.
查看习题详情和答案>>

(1)要制取大量的CO2,反应过程要便于添加液态的反应物,组合一套符合要求的装置来制取CO2,你选用的仪器组合是
②⑥⑨
②⑥⑨
(填序号).(2)下列是同学们对实验室制取CO2药品选择的讨论,你认为正确的是
①②④
①②④
(填序号)①不能用浓盐酸,因为浓盐酸易挥发,使氯化氢气体混入二氧化碳气体中.
②一般不选用碳酸钠粉末,因为它与酸反应速度太快,不便于收集.
③可用木炭和氧气反应,因为反应可生成二氧化碳.
④可用稀盐酸与石灰石反应,因为反应速度适中,条件要求不高,气体产物纯净,易于收集.
(3)将集满CO2气体的试管倒插入水中并轻轻振荡试管,可观察到的现象是
试管中液面上升
试管中液面上升
,该现象说明CO2具有的性质是溶于水
溶于水
.(4)用制取二氧化碳的气体发生装置还可以制取其它气体.请举出一例:可制取的气体是
氧气
氧气
,制气反应的化学方程式是2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,可用制二氧化碳的装置制该气体的理由是
| ||
该反应为固体和液体不需加热的反应,与制二氧化碳的反应物状态和条件相同故可用制二氧化碳的装置
该反应为固体和液体不需加热的反应,与制二氧化碳的反应物状态和条件相同故可用制二氧化碳的装置
.(5)以上仪器也可用于实验室制取氨气.实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液呈碱性.
①制取氨气反应的方程式:2NH4Cl+Ca(OH)2
| ||
H2O
H2O
.②实验室制取并收集NH3,可以从上图中选择仪器进行组装,除选择①③⑤外,还必须用到的仪器是
④
④
(填序号).③NH3是一种碱性气体,干燥时不能选用下列干燥剂中的
B
B
(填字母).A.固体氢氧化钠 B.浓硫酸 C.生石灰.
 学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
【提出问题】
1.金属钠能否置换出硫酸铜溶液中的铜?
2.金属钠能否在其他气体(如:CO2)中燃烧?
【查阅资料】金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.金属钠还可以与水剧烈反应放出氢气.
【实验探究】
实验一:
①在实验室中,金属钠保存在煤油中;
②用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中,观察到溶液中出现蓝色沉淀,但没有红色的物质析出;
③按照步骤②将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红.
实验二:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质.
【问题讨论】
(1)金属钠保存在煤油中的原因是:______.
(2)根据上述资料写出钠块投入水中发生反应的化学方程式:______.
(3)实验二中生成的黑色颗粒是______,而白色物质可能是什么呢?
①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是氧化钠,乙认为是碳酸钠,丙认为是氧化钠和碳酸钠的混合物,丁认为是氢氧化钠.我认为丁的猜想是错误的,理由是______.
②对白色物质是什么进行实验再探究,方案设计如下:
方案1:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质中一定有氧化钠.
方案2:取该样品少量于试管里,滴加足量盐酸,溶液中有气泡冒出,结论:白色物质中一定有______.
方案3:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的______溶液(供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液),出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现.则
______(在甲、乙、丙中选)的猜想成立.
③评价与反思:小娟同学认为实验方案1得出的结论不正确,其理由是______;
实验室中的金属钠着火时,你的灭火方法是______.
【拓展应用】
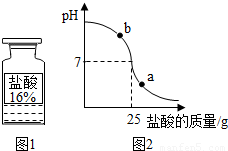
测定实验中使用的标有质量分数为16%的盐酸(图1)的实际质量分数.
(1)为了测定,需配制20%的氢氧化钠溶液100g.配制步骤有:①溶解 ②计算,需氢氧化钠______g ③装瓶并贴标签 ④称取氢氧化钠,量取水______mL(水的密度为1g/mL).其正确的顺序为______(填序号).
配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、滴管及______.
(2)小明同学在烧杯中加入配得的氢氧化钠溶液20g,再逐滴加入该盐酸.用pH测定仪测定滴加过程中溶液的pH.图2为测定仪打印出的滴加盐酸的质量与溶液pH的关系图.
①a点对应的溶液呈______(填“酸性”、“碱性”或“中性”);
b点对应的溶液中的溶质为______(写化学式).
②请以此次测定的数据,列式计算该盐酸的实际质量分数?
(3)该盐酸的实际质量分数与标签上标出的质量分数不一致的可能原因______(不考虑误差).
查看习题详情和答案>>
学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
【提出问题】
1.金属钠能否置换出硫酸铜溶液中的铜?
2.金属钠能否在其他气体(如:CO2)中燃烧?
【查阅资料】金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.金属钠还可以与水剧烈反应放出氢气.
【实验探究】
实验一:
①在实验室中,金属钠保存在煤油中;
②用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中,观察到溶液中出现蓝色沉淀,但没有红色的物质析出;
③按照步骤②将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红.
实验二:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质.
【问题讨论】
(1)金属钠保存在煤油中的原因是:______.
(2)根据上述资料写出钠块投入水中发生反应的化学方程式:______.
(3)实验二中生成的黑色颗粒是______,而白色物质可能是什么呢?
①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是氧化钠,乙认为是碳酸钠,丙认为是氧化钠和碳酸钠的混合物,丁认为是氢氧化钠.我认为丁的猜想是错误的,理由是______.
②对白色物质是什么进行实验再探究,方案设计如下:
方案1:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质中一定有氧化钠.
方案2:取该样品少量于试管里,滴加足量盐酸,溶液中有气泡冒出,结论:白色物质中一定有______.
方案3:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的______溶液(供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液),出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现.则
______(在甲、乙、丙中选)的猜想成立.
③评价与反思:小娟同学认为实验方案1得出的结论不正确,其理由是______;
实验室中的金属钠着火时,你的灭火方法是______.
【拓展应用】
测定实验中使用的标有质量分数为16%的盐酸(图1)的实际质量分数.
(1)为了测定,需配制20%的氢氧化钠溶液100g.配制步骤有:①溶解 ②计算,需氢氧化钠______g ③装瓶并贴标签 ④称取氢氧化钠,量取水______mL(水的密度为1g/mL).其正确的顺序为______(填序号).
配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、滴管及______.
(2)小明同学在烧杯中加入配得的氢氧化钠溶液20g,再逐滴加入该盐酸.用pH测定仪测定滴加过程中溶液的pH.图2为测定仪打印出的滴加盐酸的质量与溶液pH的关系图.
①a点对应的溶液呈______(填“酸性”、“碱性”或“中性”);
b点对应的溶液中的溶质为______(写化学式).
②请以此次测定的数据,列式计算该盐酸的实际质量分数?
(3)该盐酸的实际质量分数与标签上标出的质量分数不一致的可能原因______(不考虑误差).
 查看习题详情和答案>>
查看习题详情和答案>>
【提出问题】
1.金属钠能否置换出硫酸铜溶液中的铜?
2.金属钠能否在其他气体(如:CO2)中燃烧?
【查阅资料】金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.金属钠还可以与水剧烈反应放出氢气.
【实验探究】
实验一:
①在实验室中,金属钠保存在煤油中;
②用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中,观察到溶液中出现蓝色沉淀,但没有红色的物质析出;
③按照步骤②将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红.
实验二:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质.
【问题讨论】
(1)金属钠保存在煤油中的原因是:______.
(2)根据上述资料写出钠块投入水中发生反应的化学方程式:______.
(3)实验二中生成的黑色颗粒是______,而白色物质可能是什么呢?
①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是氧化钠,乙认为是碳酸钠,丙认为是氧化钠和碳酸钠的混合物,丁认为是氢氧化钠.我认为丁的猜想是错误的,理由是______.
②对白色物质是什么进行实验再探究,方案设计如下:
方案1:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质中一定有氧化钠.
方案2:取该样品少量于试管里,滴加足量盐酸,溶液中有气泡冒出,结论:白色物质中一定有______.
方案3:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的______溶液(供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液),出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现.则
______(在甲、乙、丙中选)的猜想成立.
③评价与反思:小娟同学认为实验方案1得出的结论不正确,其理由是______;
实验室中的金属钠着火时,你的灭火方法是______.
【拓展应用】
测定实验中使用的标有质量分数为16%的盐酸(图1)的实际质量分数.
(1)为了测定,需配制20%的氢氧化钠溶液100g.配制步骤有:①溶解 ②计算,需氢氧化钠______g ③装瓶并贴标签 ④称取氢氧化钠,量取水______mL(水的密度为1g/mL).其正确的顺序为______(填序号).
配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、滴管及______.
(2)小明同学在烧杯中加入配得的氢氧化钠溶液20g,再逐滴加入该盐酸.用pH测定仪测定滴加过程中溶液的pH.图2为测定仪打印出的滴加盐酸的质量与溶液pH的关系图.
①a点对应的溶液呈______(填“酸性”、“碱性”或“中性”);
b点对应的溶液中的溶质为______(写化学式).
②请以此次测定的数据,列式计算该盐酸的实际质量分数?
(3)该盐酸的实际质量分数与标签上标出的质量分数不一致的可能原因______(不考虑误差).
 查看习题详情和答案>>
查看习题详情和答案>>
 (2013?高淳县二模)学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
(2013?高淳县二模)学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:【提出问题】
1.金属钠能否置换出硫酸铜溶液中的铜?
2.金属钠能否在其他气体(如:CO2)中燃烧?
【查阅资料】金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.金属钠还可以与水剧烈反应放出氢气.
【实验探究】
实验一:
①在实验室中,金属钠保存在煤油中;
②用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中,观察到溶液中出现蓝色沉淀,但没有红色的物质析出;
③按照步骤②将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红.
实验二:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质.
【问题讨论】
(1)金属钠保存在煤油中的原因是:
防止钠与氧气和水反应变质
防止钠与氧气和水反应变质
.(2)根据上述资料写出钠块投入水中发生反应的化学方程式:
2Na+2H2O═2NaOH+H2↑
2Na+2H2O═2NaOH+H2↑
.(3)实验二中生成的黑色颗粒是
碳
碳
,而白色物质可能是什么呢?①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是氧化钠,乙认为是碳酸钠,丙认为是氧化钠和碳酸钠的混合物,丁认为是氢氧化钠.我认为丁的猜想是错误的,理由是
反应物中没有氢元素
反应物中没有氢元素
.②对白色物质是什么进行实验再探究,方案设计如下:
方案1:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质中一定有氧化钠.
方案2:取该样品少量于试管里,滴加足量盐酸,溶液中有气泡冒出,结论:白色物质中一定有
碳酸钠
碳酸钠
.方案3:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的
B
B
溶液(供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液),出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现.则乙
乙
(在甲、乙、丙中选)的猜想成立.③评价与反思:小娟同学认为实验方案1得出的结论不正确,其理由是
碳酸钠溶液也是碱性的
碳酸钠溶液也是碱性的
;实验室中的金属钠着火时,你的灭火方法是
用沙子覆盖
用沙子覆盖
.【拓展应用】
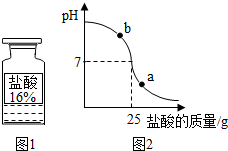
测定实验中使用的标有质量分数为16%的盐酸(图1)的实际质量分数.
(1)为了测定,需配制20%的氢氧化钠溶液100g.配制步骤有:①溶解 ②计算,需氢氧化钠
20
20
g ③装瓶并贴标签 ④称取氢氧化钠,量取水80
80
mL(水的密度为1g/mL).其正确的顺序为②④①③
②④①③
(填序号).配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、滴管及
玻璃棒
玻璃棒
.(2)小明同学在烧杯中加入配得的氢氧化钠溶液20g,再逐滴加入该盐酸.用pH测定仪测定滴加过程中溶液的pH.图2为测定仪打印出的滴加盐酸的质量与溶液pH的关系图.
①a点对应的溶液呈
酸性
酸性
(填“酸性”、“碱性”或“中性”);b点对应的溶液中的溶质为
NaCl、NaOH
NaCl、NaOH
(写化学式).②请以此次测定的数据,列式计算该盐酸的实际质量分数?
(3)该盐酸的实际质量分数与标签上标出的质量分数不一致的可能原因
盐酸具有挥发性
盐酸具有挥发性
(不考虑误差).