摘要: 於同一張繪圖紙上.以藍原子筆繪出pH值對鹽酸體積的滴定曲線.並指出滴定終點.
网址:http://m.1010jiajiao.com/timu3_id_146126[举报]
(2011?北京)在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如下表:
(1)已知t2>t1,HX的生成反应是
(2)HX的电子式是
 .
.
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是
(4)X2都能与H2反应生成HX,用原子结构解释原因:
(5)K的变化体现出X2化学性质的递变性,用原子结构解释原因:
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,
a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱.
查看习题详情和答案>>
| 化学方程式 | K(t1) | K(t2) |
F2+H2 2HF 2HF |
1.8×1036 | 1.9×1032 |
Cl2+H2 2HCl 2HCl |
9.7×1012 | 4.2×1011 |
Br2+H2 2HBr 2HBr |
5.6×107 | 9.3×106 |
I2+H2 2HI 2HI |
43 | 34 |
放热
放热
反应(填“吸热”或“放热”).(2)HX的电子式是


(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是
HF、HCl、HBr、HI
HF、HCl、HBr、HI
.(4)X2都能与H2反应生成HX,用原子结构解释原因:
卤素原子的最外层电子数均为7
卤素原子的最外层电子数均为7
.(5)K的变化体现出X2化学性质的递变性,用原子结构解释原因:
同一主族元素从上到下原子核外电子层数依次增多
同一主族元素从上到下原子核外电子层数依次增多
,原子半径逐渐增大,得电子能力逐渐减弱.(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,
abd
abd
(选填字母).a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱.
(2013?闸北区二模)工业上通常以铝土矿(主要成分为Al2O3)为原料制备无水氯化铝:2Al2O3+6Cl2
4AlCl3+3O2↑.请回答下列问题:
(1)上述反应涉及的元素中,最外层有2个未成对电子的元素是
(2)已知元素周期表中,镓(31Ga)与铝元素同一主族,写出Ga的最外层电子排布式:
(3)镓(Ga)有两种天然同位素,一种是
Ga,其原子在天然同位素原子中所占的百分比为60%.实验测得溴化镓(GaBr3)的摩尔质量为309.8g/mol,则由此推知镓的另一种同位素是
(4)为促进反应的进行,实际生产中需加入焦炭,其原因是
查看习题详情和答案>>
| △ |
(1)上述反应涉及的元素中,最外层有2个未成对电子的元素是
O
O
;简单离子的离子半径最小的元素,其原子核外有5
5
种不同能级的电子.(2)已知元素周期表中,镓(31Ga)与铝元素同一主族,写出Ga的最外层电子排布式:
4s24p1
4s24p1
(3)镓(Ga)有两种天然同位素,一种是
69 31 |
3171Ga
3171Ga
.(4)为促进反应的进行,实际生产中需加入焦炭,其原因是
碳与O2反应,有利于反应正向进行
碳与O2反应,有利于反应正向进行
.下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: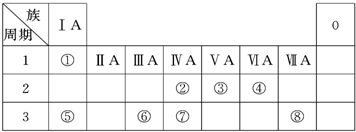
(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的离子化合物,写出其中一种化合物的电子式
 .
.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,下列物质不能做该反应催化剂的是(填序号)
a.MnO2 b.CuSO4 c.Na2SO3 d.FeCl3
(5)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应(如图):
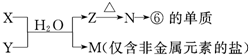
X溶液与Y溶液反应的离子方程式
N→⑥的单质的化学方程式为
M溶液中离子浓度由大到小的排列顺序是
M中阳离子的鉴定方法
查看习题详情和答案>>

(1)地壳中含量居于第二位的元素在周期表中的位置是
第三周期第IVA族
第三周期第IVA族
.(2)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:
同一主族元素从上到下原子核外电子层数依次增多
同一主族元素从上到下原子核外电子层数依次增多
,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱.(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的离子化合物,写出其中一种化合物的电子式


(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,下列物质不能做该反应催化剂的是(填序号)
c
c
.a.MnO2 b.CuSO4 c.Na2SO3 d.FeCl3
(5)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3═3H3PO4+H2W↑ |
| 1 | 还原性 还原性 |
H2SO3+Br2+2H2O=H2SO3+2HBr H2SO3+Br2+2H2O=H2SO3+2HBr |
| 2 | 酸性 酸性 |
H2SO3+2NaOH=Na2SO3+2H2O H2SO3+2NaOH=Na2SO3+2H2O |

X溶液与Y溶液反应的离子方程式
Al3++3NH3+3H2O=Al(OH)3↓+3NH4+
Al3++3NH3+3H2O=Al(OH)3↓+3NH4+
,N→⑥的单质的化学方程式为
2Al2O3(熔融)
4Al+3O2↑
| ||
| 冰晶石 |
2Al2O3(熔融)
4Al+3O2↑
,
| ||
| 冰晶石 |
M溶液中离子浓度由大到小的排列顺序是
c(Cl-)>c(NH4+)>c(H+)>c(OH-)或c(NO3-)>c(NH4+)>c(H+)>c(OH-)
c(Cl-)>c(NH4+)>c(H+)>c(OH-)或c(NO3-)>c(NH4+)>c(H+)>c(OH-)
,M中阳离子的鉴定方法
取少量M样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子
取少量M样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子
.