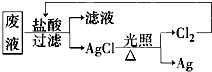
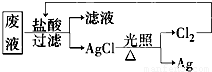
摘要:(1)该废液中可能大量存在的一种阴离子是 A.SO42- B.NO3- C.Cl- D.CO32- (2)经检测废液中铝元素的含量较高.需将其与其他三种离子分开.请选用合适的试剂.写出铝元素与该试剂反应时的离子方程式 . (3)为了回收废液中的金属银.某同学设计了如图所示的方案.若依该方案获得金属银108 g.为保证不污染环境和Cl2的循环利用.理论上应提供标准状况下的H2体积为 L.
网址:http://m.1010jiajiao.com/timu3_id_1305638[举报]
工业废水中常含有一定量的Cr2O2-7和CrO2-4,它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种.
方法1:还原沉淀法该法的工艺流程为:
CrO其中第①步存在平衡:2CrO![]() +2H+
+2H+![]() Cr2O
Cr2O![]() +H2O
+H2O
(1)若向含CeO2-4的溶液中加入H+,则溶液颜色将由________色变成________色.
(2)能说明第①步反应达平衡状态的是________.
a.Cr2O2-7和CrO2-4的浓度比为1∶2
b.v(Cr2O2-7)正=2v(CrO2-4)逆
c.溶液的离子总数不变
(3)写出第②步的离子方程式:________.
(4)第②步中,还原0.5 mol Cr2O2-7离子,需要________mol的FeSO4·7H2O.
(5)第③步生成的Cr(OH)2在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq).常温下,Cr(OH)3的溶液积KSP=10-32,将溶液pOH调整到3,Cr3+是否可认为沉淀完全________(填“是”或“否”)
Cr3+(aq)+3OH-(aq).常温下,Cr(OH)3的溶液积KSP=10-32,将溶液pOH调整到3,Cr3+是否可认为沉淀完全________(填“是”或“否”)
方法2:电解法该法用Fe做电极电解含Cr2O2-7的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(6)用Fe做电极的作用________.
(7)电解后的沉淀中有________.
在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:
(1)该废液中可能大量存在的一种阴离子是
A.SO42- B.NO3-C.Cl- D.CO32-
(2)为检测废液中铝元素的含量,需将其从废水样品中分离出来,所用的试剂是
(3)为了回收废液中的金属银,某同学设计了如图所示方案:
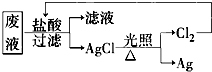
若依该方案获得108g Ag,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下H2的体积是
查看习题详情和答案>>
(1)该废液中可能大量存在的一种阴离子是
B
B
(填序号)A.SO42- B.NO3-C.Cl- D.CO32-
(2)为检测废液中铝元素的含量,需将其从废水样品中分离出来,所用的试剂是
NaOH溶液
NaOH溶液
;铝元素发生变化的离子方程式是Al3++4OH-═AlO2-+2H2O
Al3++4OH-═AlO2-+2H2O
;(3)为了回收废液中的金属银,某同学设计了如图所示方案:

若依该方案获得108g Ag,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下H2的体积是
11.2L
11.2L
.