摘要:如图所示的工具中.不属于金属加工的工具是( ) A.划规 B.手锯 C.样冲 D.刨
网址:http://m.1010jiajiao.com/timu3_id_1304405[举报]
 如图所示的木炭还原氧化铜的实验中:
如图所示的木炭还原氧化铜的实验中:(1)反应开始后,盛有澄清石灰水的试管中观察到的现象是
澄清的石灰水变浑浊
澄清的石灰水变浑浊
,说明反应中有二氧化碳
二氧化碳
生成,被加热的试管中发生的化学反应方程式是C+2CuO
2Cu+CO2↑
| ||
C+2CuO
2Cu+CO2↑
.
| ||
(2)反应完成后,把被加热的试管里的粉末倒出,可以看到有
红
红
色的铜,这是由于木炭与氧化铜反应生成了铜
木炭与氧化铜反应生成了铜
;木炭具有还原
还原
性,常用于冶金工业,写出木炭与氧化铁反应的化学方程式3C+2Fe2O3
4Fe+3CO2↑
| ||
3C+2Fe2O3
4Fe+3CO2↑
;
| ||
(3)图中的酒精灯上加金属网罩的作用是
集中火焰提高温度
集中火焰提高温度
;(4)实验结束后,应先
把导管从石灰水中移出
把导管从石灰水中移出
,再撤掉酒精灯
酒精灯
;(5)木炭常用作燃料,写出木炭充分及不充分燃烧时的化学方程式
C+O2
CO2;,C+O2
2CO
| ||
| ||
C+O2
CO2;,C+O2
2CO
.
| ||
| ||
金属是现代生活、工业生产以及科学研究中应用极为普遍的一类材料.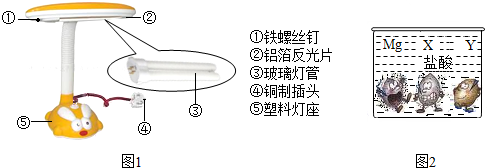
(1)青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.
①图1中标示的物质属于金属材料的有 (填序号).
②灯管后面的反光片为铝箔.铝块能制成铝箔是利用了铝的 性.
③铝比铁活泼,但铝箔却比铁螺丝钉耐腐蚀,其原因是 .
(2)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快.Mg、Cu、Fe三种金属在稀盐酸里的反应现象如右图2所示.
①右图中Y所代表的金属是 (填“Mg”或“Cu”或“Fe”);
②Mg、Cu、Fe三种金属的活动性由强到弱的顺序为 ;
(3)金属的开发和利用是人类文明和社会进步的标志.
①我国古代将炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉混合加热至800℃左右,即可得到与黄金外观相似的“药金”.
I.该方法不能制得金(Au)是因为 ;
II.“药金”是 (填“纯金属”或“合金”);
②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”.由钒钛磁铁矿提取金属钛的主要工艺过程如下: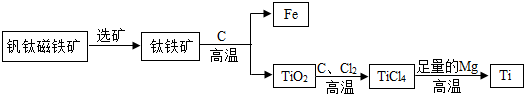
I.TiCl4在高温下与足量Mg反应置换生成金属Ti,该反应的化学方程式为: .
II.上述生产过程中得到的金属钛中混有少量金属杂质,可加入 除去.
查看习题详情和答案>>

(1)青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.
①图1中标示的物质属于金属材料的有
②灯管后面的反光片为铝箔.铝块能制成铝箔是利用了铝的
③铝比铁活泼,但铝箔却比铁螺丝钉耐腐蚀,其原因是
(2)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快.Mg、Cu、Fe三种金属在稀盐酸里的反应现象如右图2所示.
①右图中Y所代表的金属是
②Mg、Cu、Fe三种金属的活动性由强到弱的顺序为
(3)金属的开发和利用是人类文明和社会进步的标志.
①我国古代将炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉混合加热至800℃左右,即可得到与黄金外观相似的“药金”.
I.该方法不能制得金(Au)是因为
II.“药金”是
②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”.由钒钛磁铁矿提取金属钛的主要工艺过程如下:

I.TiCl4在高温下与足量Mg反应置换生成金属Ti,该反应的化学方程式为:
II.上述生产过程中得到的金属钛中混有少量金属杂质,可加入
金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)如图是铝的原子结构示意图。下列说法不正确的是_______。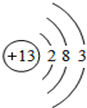
| A.铝原子中的质子数为13 |
| B.在化合物中铝通常显+3价 |
| C.铝是地壳中含量最多的元素 |
| D.铝可作导线是由于它具有良好的导电性 |

【提出问题】溶液A中的溶质可能有哪些?
【做出猜想】
① 只有Zn(NO3)2 ② Zn(NO3)2、AgNO3
③ Zn(NO3)2、Cu(NO3)2 ④ Zn(NO3)2、Cu(NO3)2、AgNO3
【交流讨论】不合理的猜想是_______(填标号),其理由是_______。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加_______ | 有气泡产生 | 固体B含有Cu 、Ag和_ |
(3)新型材料纳米级 Fe 粉具有广泛的用途,它比普通 Fe 粉更易与氧气反应,其制备工艺流程如图所示:
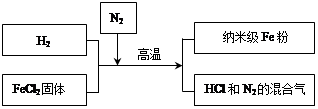
请回答下列问题:
①纳米级Fe粉在空气中易自燃。实验中通入N2的目的是_______。
②写出H2还原FeCl2,置换出铁的化学方程式_______。
③研究人员发现最后制得的纳米级 Fe 粉样品中混有少量的 FeCl2杂质。取样品20g,加入足量的盐酸,生成氢气 0.7 g。请计算该样品中单质 Fe 的质量分数(请写出计算过程)。_______ 查看习题详情和答案>>
 金属结构和性质等是化学研究的重要内容.
金属结构和性质等是化学研究的重要内容.
