摘要:18.镁条是 色的固体.在空气中燃烧的现象是:发出 .放出 .生成 .其反应的文字表达式为: .能证明这一变化是化学变化的依据是: .
网址:http://m.1010jiajiao.com/timu3_id_129920[举报]
镁在空气中燃烧生成氧化镁和氮化镁(其中氮为-3价),氮化镁与水反应生成氢氧化镁和氨气.
(1)写出氮化镁与水反应的化学方程式 ;
(2)12克镁在空气中燃烧所生成的产物的总质量 (填>、<或等于多少克);
(3)已知氮化镁是一种黄色的固体.根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的① 化合,理由是生成物② .
查看习题详情和答案>>
(1)写出氮化镁与水反应的化学方程式
(2)12克镁在空气中燃烧所生成的产物的总质量
(3)已知氮化镁是一种黄色的固体.根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的①
镁在空气中燃烧生成氧化镁和氮化镁(其中氮为-3价),氮化镁与水反应生成氢氧化镁和氨气.
(1)写出氮化镁与水反应的化学方程式 ;
(2)若有24g镁在空气中完全燃烧,则所得产物的总质量与40g的关系是 .
(3)已知氮化镁是一种黄绿色的固体.根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的 化合,理由是 .
(4)镁条还能在二氧化碳中燃烧,生成一种白色固体和一种黑色固体,请写出该反应的 该化学反应的基本类型 .
查看习题详情和答案>>
(1)写出氮化镁与水反应的化学方程式
(2)若有24g镁在空气中完全燃烧,则所得产物的总质量与40g的关系是
(3)已知氮化镁是一种黄绿色的固体.根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的
(4)镁条还能在二氧化碳中燃烧,生成一种白色固体和一种黑色固体,请写出该反应的
镁在空气中燃烧生成氧化镁和氮化镁(其中氮为-3价),氮化镁与水反应生成氢氧化镁(Mg(OH)2)和氨气(NH3),其化学方程式为
查看习题详情和答案>>
Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑
Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑
.已知氮化镁是黄绿色固体,根据镁条在空气中燃烧的实验现象,可知在这种条件下,镁更易与O2
O2
(填O2或N2)化合,理由是镁条在空气中燃烧生成一种白色固体,判断产物主要是白色固体,而氮化镁是黄绿色固体
镁条在空气中燃烧生成一种白色固体,判断产物主要是白色固体,而氮化镁是黄绿色固体
.镁在空气中燃烧除生成氧化镁外,还会生成氮化镁Mg3N2.写出镁与氮气反应生成氮化镁的化学方程式:
查看习题详情和答案>>
3Mg+N2
Mg3N2
| ||
3Mg+N2
Mg3N2
.已知24g镁在空气中完全燃烧,所得生成物总质量
| ||
<
<
(填“<”“=”或“>”)40g.已知氮化镁是黄绿色固体,根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更容易与氧气
氧气
(填“氧气”或“氮气”)反应,因为镁在空气中燃烧后生成物的颜色是白色的,而氧化镁是白色的,氮化镁是黄绿色的,说明生成氧化镁的量远比氮化镁要多
镁在空气中燃烧后生成物的颜色是白色的,而氧化镁是白色的,氮化镁是黄绿色的,说明生成氧化镁的量远比氮化镁要多
.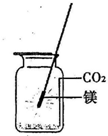 镁在空气中燃烧时既会与氧气反应生成氧化镁,同时也会与氮气反应生成氮化镁.已知氮化镁是黄绿色固体,根据镁条在空气中燃烧时的现象可知:在这样的条件下,镁更易与 O2 化合,理由是
镁在空气中燃烧时既会与氧气反应生成氧化镁,同时也会与氮气反应生成氮化镁.已知氮化镁是黄绿色固体,根据镁条在空气中燃烧时的现象可知:在这样的条件下,镁更易与 O2 化合,理由是反应的生成物为白色
反应的生成物为白色
.刘慧同学在一本参考书上发现,镁居然能在二氧化碳气体中燃烧,于是她迫不及待地做起了这个实验:将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末.
(1)根据实验现象,我能写出该反应的化学方程式:
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
| ||
(2)这个实验还引发了我对过去某些知识的反思,从而有些新的发现:
燃烧不一定有氧气进行
燃烧不一定有氧气进行
.