网址:http://m.1010jiajiao.com/timu3_id_1295160[举报]
I.如下图所示,将2molA气体和1molB气体充入一容积可变的密闭容器中。
发生反应:2A(g)+B(g)![]() 2C(g)。反应开始时可滑动的活塞的位置如图1所示,当反应达到平衡时,活塞位置如图2所示.则达到平衡时,A的转化率为________________;
2C(g)。反应开始时可滑动的活塞的位置如图1所示,当反应达到平衡时,活塞位置如图2所示.则达到平衡时,A的转化率为________________;
该条件下反应的平衡常数为_______________________________。
|
|

|
|
|
|
|
Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的化学方程式__________________________________________.
 (20利用该反应设计一个燃料电池:用氢氧化钾溶液做电解 质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式____________________________
(20利用该反应设计一个燃料电池:用氢氧化钾溶液做电解 质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式____________________________
![]() (3)有如右化学实验装置图,
(3)有如右化学实验装置图,
石墨棒上的电极反应式为_______________________________;
如果起始时盛有1000mLpH=5的硫酸铜溶液(25℃)(CuSO4 足量),一段时间后溶液的pH变为1,若要使溶液恢复到起始浓度(忽略溶液体积的变化),可向溶液中加入________(填物质名称),其质量为_______________.
查看习题详情和答案>>I.如下图所示,将2molA气体和1molB气体充入一容积可变的密闭容器中。
发生反应:2A(g)+B(g)![]() 2C(g)。反应开始时可滑动的活塞的位置如图1所示,当反应达到平衡时,活塞位置如图2所示.则达到平衡时,A的转化率为________________;
2C(g)。反应开始时可滑动的活塞的位置如图1所示,当反应达到平衡时,活塞位置如图2所示.则达到平衡时,A的转化率为________________;
该条件下反应的平衡常数为_______________________________。
|
|

|
|
|
|
|
Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的化学方程式__________________________________________.
 (20利用该反应设计一个燃料电池:用氢氧化钾溶液做电解 质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式____________________________
(20利用该反应设计一个燃料电池:用氢氧化钾溶液做电解 质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式____________________________
![]() (3)有如右化学实验装置图,
(3)有如右化学实验装置图,
石墨棒上的电极反应式为_______________________________;
如果起始时盛有1000mLpH=5的硫酸铜溶液(25℃)(CuSO4 足量),一段时间后溶液的pH变为1,若要使溶液恢复到起始浓度(忽略溶液体积的变化),可向溶液中加入________(填物质名称),其质量为_______________.
查看习题详情和答案>>(14分) 实验室需要少量某些气体时,通常使用快速的方法制备。下列几个实验可快速制取实验事所需的少量气体,并进行相关性质实验。(实验装置如右图所示)
实验室需要少量某些气体时,通常使用快速的方法制备。下列几个实验可快速制取实验事所需的少量气体,并进行相关性质实验。(实验装置如右图所示)
(1)若A中为15的H2O2溶液,B中固体为MnO2,C中盛有FeCl2和KSCN的混合液。回答下列问题:
① 装置A的名称是_________。
② 旋开E后,C中的现象是 ________。
③ 假设15的H2O2溶液和30的H2O2溶液的密度均为1g/cm3;如何用30H2O2溶液配制100克15的H2O2溶液:_______ 。
(2)若B中是生石灰,将A中液体逐滴加入B内,实验中观察到C的溶液中先出现沉淀、然后沉淀逐渐溶解,当溶液恰好澄清时,关闭E,将C装置放入盛有沸水的烧杯中,静置片刻,观察到试管内壁出现光亮的银镜。回答下列问题:
① C中是葡萄糖与__________(写化学式)的混合液。
② 仪器D在此实验中的作用是___________________。
(3)若A中浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,旋开E后,B中出现黄绿色气体,C中的现象是先出现蓝色后褪色.
甲同学认为:Cl2溶于水生成HClO, HClO具有漂白性。
乙同学认为:氯水具有强氧化性,把I2氧化IO3-。
丙同学为了证明甲、乙同学的观点谁的正确,做了如下实验:取C中褪色的溶液少许,加几滴淀粉溶液,结果溶液不变蓝色。则_________(填甲、乙同学)的观点正确。
有学生认为,此实验装置存在不足,请你指出________________________________ 查看习题详情和答案>>化学实验兴趣小组在实验室进行氢气在氯气中的燃烧实验
(一)设计如下图所示装置I制备和收集干燥纯净的氯气以备后续实验:
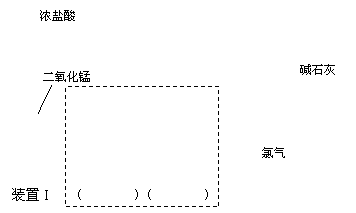

①烧瓶中发生反应的离子方程式为: ;
②请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;

 (二)在右图所示装置II中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
(二)在右图所示装置II中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
①检查制取氢气装置气密性的操作方法是
②当点燃氢气后,将导管伸入盛有氯气的集气瓶中,观察到的现象是
③试管中加入少量CuSO4溶液的作用是 ,其原理是
(三)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验,A组同学发现制取氢气后的试管中还有较多固体剩余。同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生。请解释可能原因(用离子方程式表示):
;B组同学向集气瓶中注入适量水,用力振荡后,向其中滴入少量Na2S2O3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。(已知Na2S2O3+ H2SO4= Na2SO4+S↓+SO2↑+ H2O),同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:
①
②
查看习题详情和答案>>某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如右图所示的实验装置(支撑用的铁架台省略),按要求回答问题:
(1)写出A中发生反应的化学方程式 。
(2)①. 装置B中盛放的试剂为 。
②. 装置D和E中出现的不同现象说明的问题是
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 和 之间(填两个装置字母序号),装置中应放入
(填写试剂或用品名称)。ks5u
(4)丙同学将4.48L氯气(标准状况下测定)通入到足量的石灰乳中,理论上可制得氧化产物质量 g。 