摘要:200水溶解一定质量的氯化镁配制成溶液.取此溶液一半.加入一定质量20%的氢氧化钠溶液恰好万全反应.生成5.8沉淀. (1)求配制成氯化镁溶液的总质量. (2)求反应后生成的溶液中溶质的质量分数.
网址:http://m.1010jiajiao.com/timu3_id_125639[举报]
(2008?包头)77.8克水溶解一定质量的氯化钾配制成溶液.取此溶液一半,加入一定质量10%的硝酸银溶液恰好完全反应,生成14.35克沉淀.
(1)求配制成氯化钾溶液的总质量.
(2)求反应后生成的溶液中溶质的质量分数.
查看习题详情和答案>>
(1)求配制成氯化钾溶液的总质量.
(2)求反应后生成的溶液中溶质的质量分数.
77.8克水溶解一定质量的氯化钾配制成溶液.取此溶液一半,加入一定质量10%的硝酸银溶液恰好完全反应,生成14.35克沉淀.
(1)求配制成氯化钾溶液的总质量.
(2)求反应后生成的溶液中溶质的质量分数.
查看习题详情和答案>>
77.8克水溶解一定质量的氯化钾配制成溶液.取此溶液一半,加入一定质量10%的硝酸银溶液恰好完全反应,生成14.35克沉淀.
(1)求配制成氯化钾溶液的总质量.
(2)求反应后生成的溶液中溶质的质量分数.
查看习题详情和答案>>
(1)求配制成氯化钾溶液的总质量.
(2)求反应后生成的溶液中溶质的质量分数.
某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:

①称量ag胆矾固体放入烧杯中,加水制成溶液,向其中滴加氢氧化钠溶液至溶解完全;
②把步骤①中的溶液和沉淀转移至蒸发皿中,加热至溶液中的沉淀全部变成黑色氧化铜为止;
③过滤、洗涤、干燥,称量所得固体质量为bg;
④取一定质量的上述氧化铜固体和一定质量的氯酸钾固体,混合均匀后加热,收集反应生成的氧气,如图所示.请回答下列问题:
(1)上述各步操作中,需要用到玻璃棒的是(填写序号) .
(2)由胆矾制备氧化铜的产率(实验产量与理论产量的百分比)为 ×100%.
(3)为保证Cu2+沉淀完全,步骤①中溶液的pH应大于10,简述pH试纸测定溶液pH的操作: .
(4)为证明氧化铜在氯酸钾的分解反应中起催化作用,在上述实验①~④后还应该进行的实验操作是(按实验先后顺序填写字母序号) .
a、过滤 b、烘干 c、溶解 d、洗涤 e、称量
(5)但有的同学认为,还必须另外再设计一个实验才能证明氧化铜在氯酸钾受热分解的实验中起催化作用.你认为还应该进行的另一个实验是 .
查看习题详情和答案>>

①称量ag胆矾固体放入烧杯中,加水制成溶液,向其中滴加氢氧化钠溶液至溶解完全;
②把步骤①中的溶液和沉淀转移至蒸发皿中,加热至溶液中的沉淀全部变成黑色氧化铜为止;
③过滤、洗涤、干燥,称量所得固体质量为bg;
④取一定质量的上述氧化铜固体和一定质量的氯酸钾固体,混合均匀后加热,收集反应生成的氧气,如图所示.请回答下列问题:
(1)上述各步操作中,需要用到玻璃棒的是(填写序号)
(2)由胆矾制备氧化铜的产率(实验产量与理论产量的百分比)为
(3)为保证Cu2+沉淀完全,步骤①中溶液的pH应大于10,简述pH试纸测定溶液pH的操作:
(4)为证明氧化铜在氯酸钾的分解反应中起催化作用,在上述实验①~④后还应该进行的实验操作是(按实验先后顺序填写字母序号)
a、过滤 b、烘干 c、溶解 d、洗涤 e、称量
(5)但有的同学认为,还必须另外再设计一个实验才能证明氧化铜在氯酸钾受热分解的实验中起催化作用.你认为还应该进行的另一个实验是
(2012?昆明)(1)如图1所示a、b、c、d四个点,表示可燃物容易着火的点是
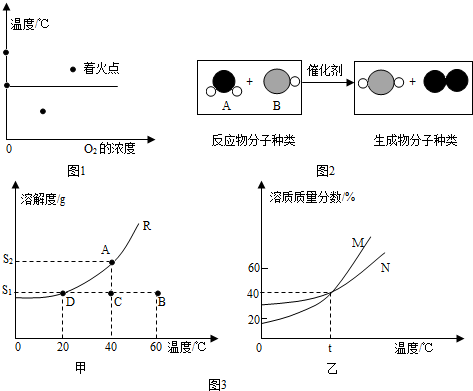
(2)请根据如图2反应的微观示意图分析:
参加反应的化合物A与化合物B的分子个数比为
(3)将一定质量的氯酸钾(不含催化剂)置于试管中加热一段时间,冷却后测得所得固体
中氯元素的质量分数为35.5%,则反应中已分解的氯酸钾的质量分数为
(4)请根据图3所示回答问题:
①甲图中R物质在室温(20℃)时的饱和状态为D点,40℃时的饱和状态为A点,现将甲图中的R溶液从A状态变到B状态,请设计并简述两个简单的实验操作途径:a.
②乙图是表示M、N两种物质饱和溶液的溶质质量分数随温度变化的曲线.现分别向50g M、80g N固体中各加入150g水,并加热至完全溶解,同时各蒸发掉50g水,冷却至t℃,下列分析正确的是
a.只有N析出晶体; b.M、N两种溶液的溶质质量分数相等;
c.只有M析出晶体; d.M、N均有晶体析出;
e.M、N两种物质的溶解度相同.
查看习题详情和答案>>
d
d
点(填字母序号).
(2)请根据如图2反应的微观示意图分析:
参加反应的化合物A与化合物B的分子个数比为
1:2或2:4
1:2或2:4
,生成物中单质分子与化合物分子的个数比为1:4
1:4
.(3)将一定质量的氯酸钾(不含催化剂)置于试管中加热一段时间,冷却后测得所得固体
中氯元素的质量分数为35.5%,则反应中已分解的氯酸钾的质量分数为
46.8
46.8
%.(4)请根据图3所示回答问题:
①甲图中R物质在室温(20℃)时的饱和状态为D点,40℃时的饱和状态为A点,现将甲图中的R溶液从A状态变到B状态,请设计并简述两个简单的实验操作途径:a.
可先将R溶液从A状态稀释到C状态,再将温度升高到60℃
可先将R溶液从A状态稀释到C状态,再将温度升高到60℃
;b.可先将A状态的R溶液温度降低到20℃,过滤后再将滤液温度升高到60℃
可先将A状态的R溶液温度降低到20℃,过滤后再将滤液温度升高到60℃
;c.A状态由两种不同途径变到B状态时,溶液的溶质质量分数是否相等是
是
(填“是”或“否”).②乙图是表示M、N两种物质饱和溶液的溶质质量分数随温度变化的曲线.现分别向50g M、80g N固体中各加入150g水,并加热至完全溶解,同时各蒸发掉50g水,冷却至t℃,下列分析正确的是
ae
ae
(填序号,多选、少选、错选均不给分).a.只有N析出晶体; b.M、N两种溶液的溶质质量分数相等;
c.只有M析出晶体; d.M、N均有晶体析出;
e.M、N两种物质的溶解度相同.