摘要:27.如图中学常见物质转化如下.金属A既能与强酸也能与强碱作用产生气体. (1)反应①化学上通常称为 引发该反应进行时通常要在混合物上加入少量物质是 (2)反应②得到物质C和D在一定条件下作用生成KCl和KClO与同时还能得到价态不同的另一种实验室常见物质.其化学式可能是 (3)高铁酸盐可以同时做净水剂和消毒剂.其在水中能缓慢放出氧气 4FeO42-+10H2O = 4Fe(OH)3+8OH-+3O2↑ 遇酸则有: 4FeO42-+20 H+ = 4Fe3++10H2O+3O2↑ ①若用如图所示装置完成工业某高铁酸钾盐中高铁酸钾含量测 定.需要的获取的实验数据是 . ②上图中用G.K.D生成K2FeO4反应中氧化剂和还原剂的物 质的量之比是 . ③用高铁酸钾和锌制成的高铁碱性电池能储存比普通碱性电池 多50%的电能.已知该电池的总反应是:2K2FeO4+3Zn= Fe2O3+ZnO+2K2ZnO2, 则负极的电极反应是 .
网址:http://m.1010jiajiao.com/timu3_id_1242742[举报]
中学常见物质A、B、D、E、G、M、Q之间有如下图所示变化关系(反应条件已省略):
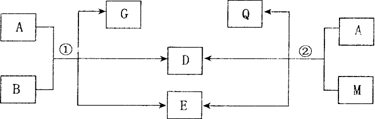
(1)若A是黑色非金属固体单质,G、Q、D是气体,E是水,D的化学式为________.
(2)若A是红色金属,B、M是同种溶质不同浓度的溶液,G、Q是气体,且G可通过化合反应生成Q.反应①的离子方程式是________.
(3)若A是Ca(OH)2,D是极易溶于水的气体.
①工业上合成D使用铁触媒作催化剂,采用500℃左右、20MPa-50MPa为生产条件的原因有________(填标号).
a.化学反应速率最大
b.催化剂的活性最大
c.反应物转化率最大
d.综合经济效益较好
上述反应中,每生成l mol D时放出热量46.2 kJ,该反应的热化学方程式是:
____________________________________
②当l mol Ca(OH)2分别与B、M完全反应时,反应①、②生成的D的物质的量之比为2∶1,B、M的化学式分别为________、________.
 如图表示常见物质的相互转化关系(图中反应条件及部分反应物或生成物略去).X是黄绿色气体;M、N为金属单质,其中M是地壳中含量最多的金属元素;E为红褐色固体;反应③常用于冶炼金属.试回答下列问题:
如图表示常见物质的相互转化关系(图中反应条件及部分反应物或生成物略去).X是黄绿色气体;M、N为金属单质,其中M是地壳中含量最多的金属元素;E为红褐色固体;反应③常用于冶炼金属.试回答下列问题:(1)物质E的化学式为
Fe(OH)3
Fe(OH)3
.(2)画出X的组成元素原子结构简图


(3)写出反应②的离子方程式
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.(4)分别写出反应①、③的化学方程式
2Al+3Cl2
2AlCl3
| ||
2Al+3Cl2
2AlCl3
、
| ||
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
.
| ||
中学常见的单质A、B、C(其中A为金属单质)和甲、乙、丙、丁四种化合物有如图的转化关系,已知C为密度最小的气体,甲是电解质.根据以上转化关系回答:

(1)写出下列物质的化学式:A: ;B: ;乙: ;丁: .
(2)①A与NaOH溶液反应的化学方程式: .
②乙与过量的CO2反应的离子方程式: .
查看习题详情和答案>>

(1)写出下列物质的化学式:A:
(2)①A与NaOH溶液反应的化学方程式:
②乙与过量的CO2反应的离子方程式:

 如图表示常见物质的相互转化关系(图中反应条件及部分反应物或生成物略去).X是黄绿色气体;M、N为金属单质,其中M是地壳中含量最多的金属元素;E为红褐色固体;反应③常用于冶炼金属.试回答下列问题:
如图表示常见物质的相互转化关系(图中反应条件及部分反应物或生成物略去).X是黄绿色气体;M、N为金属单质,其中M是地壳中含量最多的金属元素;E为红褐色固体;反应③常用于冶炼金属.试回答下列问题: