摘要:(一)下表是A.B.C.D.E.F六种短周期元素的化合价及电负性数据 A B C D E F 化合价 -4 -2 -1 -2 -1 -3 电负性 2.55 2.58 3.16 3.44 3.98 2.19 (1)下列说法正确的是 A.E的最高价氧化物对应水化物的酸性最强 B.六种元素的第一电离能的大小顺序是:F<A<B<C<D<E C.A的某种单质可以导电.证明其晶体中有金属键 D.F的最高价氧化物对应水化物具有强氧化性 (2)用氢键表示式写出E的氢化物水溶液中存在的所有氢键 . (3)相同条件下.与分子两者在水中的溶解度较大的是 .理由是 .
网址:http://m.1010jiajiao.com/timu3_id_1242070[举报]
下表是A、B、C、D、E、F六种短周期元素的化合价及电负性数据
下列说法正确的是( )
①E的最高价氧化物对应水化物的酸性最强
②六种元素的第一电离能的大小顺序是:F<A<B<C<D<E
③A的某种单质可以导电,其晶体中有共价键
④F的最高价氧化物对应水化物具有强氧化性.
| A | B | C | D | E | F | |
| 化合价 | -4 | -2 | -1 | -2 | -1 | -3 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 | 2.19 |
①E的最高价氧化物对应水化物的酸性最强
②六种元素的第一电离能的大小顺序是:F<A<B<C<D<E
③A的某种单质可以导电,其晶体中有共价键
④F的最高价氧化物对应水化物具有强氧化性.
| A、①② | B、②③ | C、③ | D、④ |
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.已知:A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2.请回答:
(1)元素C在周期表中的位置是
(2)元素D的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物与水反应的离子方程式
(3)D和E两种元素相比较,其原子得电子能力较强的是
以下说法中,可以证明上述结论的是
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(4)元素A、D、E与钠元素可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中反应的离子方程式是:
(5)由元素A、B、D组成的一元酸X为日常生活中的调味剂,元素A、F组成的化合物为Y.在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X
(6)元素F的单质常温下是一种气体,工业上主要是通过电解其钠盐的饱和溶液的方法获得该气体,假定装入的饱和溶液为100mL(电解前后溶液体积变化可忽略),当测得阴极上产生11.2mL(标准状况)气体时停止通电,将溶液摇匀,此时溶液的pH为
查看习题详情和答案>>
(1)元素C在周期表中的位置是
第二周期第ⅣA族
第二周期第ⅣA族
.(2)元素D的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物与水反应的离子方程式
2Na2O2 +2H2 O=4Na++4OH-+O2↑
2Na2O2 +2H2 O=4Na++4OH-+O2↑
.(3)D和E两种元素相比较,其原子得电子能力较强的是
氧
氧
(写名称).以下说法中,可以证明上述结论的是
bc
bc
(填写编号).a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(4)元素A、D、E与钠元素可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中反应的离子方程式是:
HSO3-+H+=SO2↑+H2O
HSO3-+H+=SO2↑+H2O
.(5)由元素A、B、D组成的一元酸X为日常生活中的调味剂,元素A、F组成的化合物为Y.在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X
>
>
Y(填“>”、“=”或“<”)(6)元素F的单质常温下是一种气体,工业上主要是通过电解其钠盐的饱和溶液的方法获得该气体,假定装入的饱和溶液为100mL(电解前后溶液体积变化可忽略),当测得阴极上产生11.2mL(标准状况)气体时停止通电,将溶液摇匀,此时溶液的pH为
12
12
.A、B、C、D、E、F六种短周期元素的原子序数依次增大.A是宇宙中含量最丰元素,B元素的原子价电子排布为nsnnpn,D元素的最外层电子数是其电子层数的3倍,F的最高价氧化物对应水化物有两性,能溶于C、E的最高价氧化物对应水化物中.试回答:
(1)写出C原子的价层电子轨道表示式: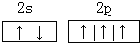
 ;D原子的价层电子排布式:
;D原子的价层电子排布式: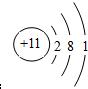
 ;
;
(2)B位于元素周期表的第
(3)C的基态原子核外有
(4)E单质在空气中燃烧生成物的电子式: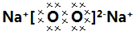
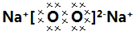 ,其中的阳离子与阴离子的个数比是
,其中的阳离子与阴离子的个数比是
(5)F的固态氧化物的用途有
查看习题详情和答案>>
(1)写出C原子的价层电子轨道表示式:


2s22p4
2s22p4
,E的原子结构示意图:

(2)B位于元素周期表的第
IVA
IVA
族,A、B形成原子个数比1:1且直线形分子的结构式:H-C≡C-H
H-C≡C-H
;(3)C的基态原子核外有
7
7
种不同运动状态的电子;(4)E单质在空气中燃烧生成物的电子式:
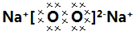
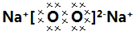
2:1
2:1
;(5)F的固态氧化物的用途有
耐火材料
耐火材料
(说出一种).F的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是4Al+3TiO2+3C
2Al2O3+3TiC
| ||
4Al+3TiO2+3C
2Al2O3+3TiC
.
| ||
A、B、C、D、E、F六种短周期元素,原子序数依次增大,A、E同主族,D、F同主族,A元素的原子半径是所有原子中最小的,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)F元素在周期表中的位置
 .
.
(2)D、F的气态氢化物,沸点较高的是
(3)A单质与C单质在一定条件下可化合为Z,常温下,向pH=a的Z的水溶液中加入等体积pH=b的X的水溶液,且a+b=14,充分作用后,溶液pH
查看习题详情和答案>>
(1)F元素在周期表中的位置
第三周期第ⅥA族
第三周期第ⅥA族
,在以上元素最高价氧化物的水化物中,碱性最强的化合物的电子式是:

(2)D、F的气态氢化物,沸点较高的是
H2O
H2O
(填分子式).(3)A单质与C单质在一定条件下可化合为Z,常温下,向pH=a的Z的水溶液中加入等体积pH=b的X的水溶液,且a+b=14,充分作用后,溶液pH
>
>
7(填“>”“<”或“=”),原因是弱碱与盐的混合溶液真弱碱的电离大于盐中弱碱阳离子的水解
弱碱与盐的混合溶液真弱碱的电离大于盐中弱碱阳离子的水解
.