网址:http://m.1010jiajiao.com/timu3_id_1241577[举报]
(1)医学上常用3%的双氧水来清洗创口和局部抗菌,将双氧水涂在伤口上会产生气泡,此气体应该是
(2)双氧水长久放置是否能失效呢?请表达你的观点及理由:
(3)有人通过比较双氧水和水的化学式,得出“双氧水的含氧量是普通水的2倍”的结论.判断这种说法是否正确,并说明原因:
(4)保存双氧水应注意下列事项:①阴凉处保存,避免阳光直射;②严禁与金属及金属氧化物混存;③严禁与易燃品混存…
请选择上述注意事项的任意一项,做出你的解释:
“碳铵”(NH4HCO3)是一种常用的化学肥料,易溶于水,受潮时在常温下就能分解,温度越高分解越快,分解产物为NH3、CO2、H2O。“碳铵”遇碱放出氨气,在土壤中不残留有害物质。
⑴“碳铵”属于化肥中的 ▲ 肥,化学性质 ▲ (填“稳定”或“不稳定”);保存时应
注意 ▲ 。(选填序号)
①贮存和运输时要密封,不要受潮和曝晒;施用后要立即盖土或立即灌溉
②不要与碱性物质混放或混用
③不能与易燃物质混在一起;结块时,不要用铁锤砸碎
④不宜长期施用
某兴趣小组欲在实验室利用如下图所示的装置研究“碳铵”的部分性质,请你一起参与。

⑵选择装置 ▲ (填序号)进行“碳铵”固体受热分解的实验,该反应的化学方程式为
▲ ;应用该装置,还可以在实验室进行的实验是 ▲ 。(答一个即可)
⑶利用装置①,写出实验室制取一种气体的化学方程式 ▲ ,收集该气体的装置应选择 ▲ 。
⑷取少量“碳铵”和熟石灰粉末放入装置②的大试管中,微热片刻立即移开酒精灯。将产生的氨气缓缓通入盛有酚酞试液的试管中,酚酞试液变红。
①由此可知,氨气易溶于水,其水溶液(氨水)显 ▲ 性(填“酸”、“碱”或“中”),pH ▲ 7(填“<”、“>”或“=”)。
②某同学认为可用装置③干燥氨气你认为他能否达到目的?简要分析原因。
▲ ;
③由于氨气具有强烈的刺激性气味,对人体的呼吸道粘膜有较大的伤害,我们可以选用上述的装置中的⑦和⑧连接收集并吸收逸散出来的多余氨气,则应将 ▲ (选填“a”或“ b”)与c相连接,烧杯中应盛放 ▲ 。
查看习题详情和答案>>(1)“碳铵”属于化肥中的
注意
①贮存和运输时要密封,不要受潮和曝晒;施用后要立即盖土或立即灌溉
②不要与碱性物质混放或混用
③不能与易燃物质混在一起;结块时,不要用铁锤砸碎
④不宜长期施用
某兴趣小组欲在实验室利用如下图所示的装置研究“碳铵”的部分性质,请你一起参与.
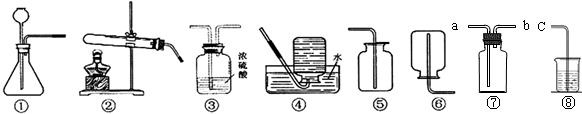
(2)选择装置
(3)利用装置①,写出实验室制取一种气体的化学方程式
(4)取少量“碳铵”和熟石灰粉末放入装置②的大试管中,微热片刻立即移开酒精灯.将产生的氨气缓缓通入盛有酚酞试液的试管中,酚酞试液变红.
①由此可知,氨气易溶于水,其水溶液(氨水)显
②某同学认为可用装置③干燥氨气你认为他能否达到目的?简要分析原因.
③由于氨气具有强烈的刺激性气味,对人体的呼吸道粘膜有较大的伤害,我们可以选用上述的装置中的⑦和⑧连接收集并吸收逸散出来的多余氨气,则应将
(1)“碳铵”属于化肥中的______肥,化学性质______(填“稳定”或“不稳定”);保存时应
注意______.(选填序号)
①贮存和运输时要密封,不要受潮和曝晒;施用后要立即盖土或立即灌溉
②不要与碱性物质混放或混用
③不能与易燃物质混在一起;结块时,不要用铁锤砸碎
④不宜长期施用
某兴趣小组欲在实验室利用如下图所示的装置研究“碳铵”的部分性质,请你一起参与.

(2)选择装置______(填序号)进行“碳铵”固体受热分解的实验,该反应的化学方程式为
______;应用该装置,还可以在实验室进行的实验是______.(答一个即可)
(3)利用装置①,写出实验室制取一种气体的化学方程式______,收集该气体的装置应选择______.
(4)取少量“碳铵”和熟石灰粉末放入装置②的大试管中,微热片刻立即移开酒精灯.将产生的氨气缓缓通入盛有酚酞试液的试管中,酚酞试液变红.
①由此可知,氨气易溶于水,其水溶液(氨水)显______性(填“酸”、“碱”或“中”),pH______7(填“<”、“>”或“=”).
②某同学认为可用装置③干燥氨气你认为他能否达到目的?简要分析原因.
______;
③由于氨气具有强烈的刺激性气味,对人体的呼吸道粘膜有较大的伤害,我们可以选用上述的装置中的⑦和⑧连接收集并吸收逸散出来的多余氨气,则应将______(选填“a”或“b”)与c相连接,烧杯中应盛放______.
[提出问题]1.金属钠能否置换出硫酸铜溶液中的铜?2.金属钠能否在其他气体(如:CO2)中燃烧?
[查阅资料]金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.金属钠还可以与水剧烈反应放出氢气.
[实验探究]实验一:①在实验室中,金属钠保存在煤油中;②用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中,观察到溶液中出现蓝色沉淀,但没有红色的物质析出;
③按照步骤②将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红.
实验二:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质.
[问题讨论](1)金属钠保存在煤油中的原因
(2)根据上述资料写出钠块投入水中所发生的反应方程式:
| ||
| ||
(3)实验二中生成的黑色颗粒是
①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是Na2O,乙认为是Na2CO3,丙认为是Na2O和Na2CO3的混合物,丁认为是NaOH.
我认为认为丁的猜想是错误的,理由是
②对白色物质是什么进行实验再探究,方案设计如下:
方案1:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质中一定有Na2O.
方案2:取该样品少量于试管里,滴加足量稀盐酸,溶液中有气泡冒出,结论:白色物质中一定有
方案3:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的
③评价与反思:大家认为实验方案1得出的结论不正确,其理由是
实验室中的金属钠着火时,你的灭火方法是
[拓展应用]小明同学为测定实验过程中所用的标示质量分数为32%的盐酸 (图1)的实际质量分数,他与小组的其他同学用pH测定仪组成实验装置(图2).实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加人该盐酸,测定仪打印出加入盐酸的质量与烧杯中溶液pH的关系图(图3).

①发生反应的化学方程式为:
②请以此次测定的结果,可计算出该盐酸的实际质量分数是
③请分析你的计算结果与标签标示的质量分数不一致的可能原因: