网址:http://m.1010jiajiao.com/timu3_id_1240456[举报]
I.飞机尾气中的NO会破坏臭氧层。利用催
化剂可使尾气中的NO和CO发生反应2NO +2CO
![]() 2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 1.20×10-3 | 124 | ||
| Ⅲ | 350 | 5.80×10-3 |
(1)请填全表中的各空格。
(2)请在右边给出的坐标图中,画出上表中的三
 个实验条件下混合气体中NO浓度随时间变
个实验条件下混合气体中NO浓度随时间变
化的趋势曲线图,并标明各条曲线的实验编号。
II.汽车内燃机工作时产生的高温会引起N2和O2的反应:
N2(g)+O2(g)![]() =2NO(g)是导致汽车尾气
=2NO(g)是导致汽车尾气
中含有NO的原因之一。
2000C时,向容积为2L的密闭容器中充入10molN2与5mol O2,达到平衡后NO的物质的量为2mol,则该反应的平衡常数K=___ _ 。该温度下,若开始时向上述容器中充入1 molN2和一定量的O2,平衡时O2与NO的物质的量恰好相等,则平 衡时N2的物质的量是 。
查看习题详情和答案>>I.飞机尾气中的NO会破坏臭氧层。利用催
化剂可使尾气中的NO和CO发生反应2NO +2CO![]() 2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 1.20×10-3 | 124 | ||
Ⅲ | 350 | 5.80×10-3 |
(1)请填全表中的各空格。
(2)请在右边给出的坐标图中,画出上表中的三
 个实验条件下混合气体中NO浓度随时间变
个实验条件下混合气体中NO浓度随时间变
化的趋势曲线图,并标明各条曲线的实验编号。
II.汽车内燃机工作时产生的高温会引起N2和O2的反应:
N2(g)+O2(g)![]() =2NO(g)是导致汽车尾气中含有NO的原因之一。
=2NO(g)是导致汽车尾气中含有NO的原因之一。
2000C时,向容积为2L的密闭容器中充入10molN2与5mol O2,达到平衡后NO的物质的量为2mol,则该反应的平衡常数K=___ _ 。该温度下,若开始时向上述容器中充入1 molN2和一定量的O2,平衡时O2与NO的物质的量恰好相等,则平 衡时N2的物质的量是 。
查看习题详情和答案>>| 催化剂 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)若上述反应的平衡常数K,随温度增高而减小,则反应的△H
(2)前2s内的平均反应速度v(N2)=
(3)该温度下,反应的平衡常数K=
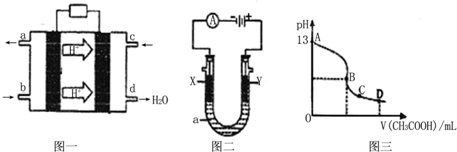
II、甲醇空气燃料电池(酸性电解质溶液)的工作原理如图一所示.

(1)该电池正极的电极反应式为
(2)以上述电池为电源,构成图二电解池,其中X、Y为石墨,a为KCl溶液,写出电解总反应的离子方程式
(3)常温时,按“(2)”电解一段时间后,取25mL上述电解后的溶液,滴加0.2mol/L的醋酸溶液,滴加过程的pH变化如图三所示,则C点对应溶液中各离子浓度的大小关系为(忽略电解后溶液中的其他成分,只考虑其中的碱与加入的酸)
| 催化剂 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)若上述反应的平衡常数K,随温度增高而减小,则反应的△H______0(填“>”、“<”或“=”).
(2)前2s内的平均反应速度v(N2)=______.
(3)该温度下,反应的平衡常数K=______.
II、甲醇空气燃料电池(酸性电解质溶液)的工作原理如图一所示.
(1)该电池正极的电极反应式为______.
(2)以上述电池为电源,构成图二电解池,其中X、Y为石墨,a为KCl溶液,写出电解总反应的离子方程式______.
(3)常温时,按“(2)”电解一段时间后,取25mL上述电解后的溶液,滴加0.2mol/L的醋酸溶液,滴加过程的pH变化如图三所示,则C点对应溶液中各离子浓度的大小关系为(忽略电解后溶液中的其他成分,只考虑其中的碱与加入的酸)______.
超音速飞机在平流层飞行时,尾气中的![]() 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的![]() 和
和![]() 转变成
转变成![]() 和
和![]() ,化学方程式如下:
,化学方程式如下:
2NO+2CO![]() 2CO2 + N2 ;为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2 + N2 ;为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
 请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的![]() 0(填写“>”、“<”、“=”。
0(填写“>”、“<”、“=”。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)在该温度下,反应的平衡常数K= 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验编号 | T/OC | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2·g-1 |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 124 | |||
| III | 350 | 124 |
①请在上表格中填入剩余的实验条件数据。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线是实验编号。
