摘要:23. (1)第三周期第ⅦA族 2Fe2++Cl2===2Fe3++2Cl- (2)2Mg+CO22MgO+C C+4HNO3(浓) CO2↑+4NO2↑+2H2O (3)原子晶体.O=C=O
网址:http://m.1010jiajiao.com/timu3_id_1223462[举报]
短周期元素X.Y.Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1:1的离子化合物A,X与Z能形成原子个数比为1:1的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):

(1)Z在周期表的位置是
 .
.
(2)反应①的离子方程式是
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应.某校的学生在实验室利用反应②的原理来制备纯净.干燥的Z2,仪器装置如下图所示(夹持固定装置的仪器已略去).
I.写出反应②的离子方程式
II.上述实验装置不够完善,改进方法是
Ⅲ.足量Z2 通入FeBr2溶液中发生反应的离子方程式是
查看习题详情和答案>>

(1)Z在周期表的位置是
第三周期第ⅦA族
第三周期第ⅦA族
;Y单质在空气中燃烧所得产物的电子式是

(2)反应①的离子方程式是
2Cl-+2H2O
2OH-+Cl2↑+H2↑
| ||
2Cl-+2H2O
2OH-+Cl2↑+H2↑
.
| ||
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应.某校的学生在实验室利用反应②的原理来制备纯净.干燥的Z2,仪器装置如下图所示(夹持固定装置的仪器已略去).

I.写出反应②的离子方程式
ClO-+Cl-+2H+=Cl2↑+H2O
ClO-+Cl-+2H+=Cl2↑+H2O
.II.上述实验装置不够完善,改进方法是
在a、b装置之间加一盛有饱和食盐水(或水)的洗气瓶,除去HCl
在a、b装置之间加一盛有饱和食盐水(或水)的洗气瓶,除去HCl
.Ⅲ.足量Z2 通入FeBr2溶液中发生反应的离子方程式是
2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2
2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2
.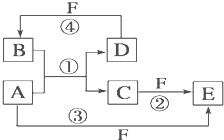 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).(1)若A为短周期金属单质,D为短周期非金属单质(一种黑色固体),且所含元素的原子序数A是D的2倍,原子的最外层电子数D是A的2倍,化合物F的浓溶液与单质A、D在一定条件下反应都有红棕色气体生成,则A在周期表中的位置为:
第三周期,ⅡA族
第三周期,ⅡA族
,B的电子式为::O::C::O:
:O::C::O:
,F的浓溶液与D在加热条件下反应的化学方程式为:C+4HNO3
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3
CO2↑+4NO2↑+2H2O
.
| ||
(2)若A是常见变价金属的单质,D、F是气态单质,且反应①②均在水溶液中进行.则反应②的离子方程式是
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(3)若A、D、F都是短周期非金属元素单质,且 A、D所含元素同主族,A、F所含元素同周期,B是制作光导纤维的基本原料,则B是
SiO2
SiO2
,C是CO
CO
,F是O2
O2
.(填化学式) A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件及部分产物未列出)
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件及部分产物未列出)(1)若A是常见金属单质,与B的水溶液反应生成C和D.D、F是气体单质,D在F中燃烧时发出苍白色火焰.则F所对应的元素在周期表位置是
第三周期、第ⅦA族
第三周期、第ⅦA族
,反应②(在水溶液中进行)的离子方程式为2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
;(2)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,且③④两个反应都有红棕色气体生成,则反应①、④的化学方程式分别为
①
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
,
| ||
④
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
;
| ||
(3)若A、D、F都是短周期非金属单质,且A、D所含元素同主族,A、F所含元素同周期,C是一种能与血红蛋白结合的有毒气体;则物质B的晶体类型是
原子晶体
原子晶体
,分子E的结构式是O=C=O
O=C=O
.短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1:1的离子化合物A,X与Z能形成原子个数比为1:1的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):

(1)Y在周期表的位置是
(2)反应①的离子方程式是
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应.某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示(夹持固定装置的仪器已略去).

I、写出反应②的离子方程式
II、上述实验装置不够完善,改进方法是
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是
查看习题详情和答案>>

(1)Y在周期表的位置是
第三周期第IA族
第三周期第IA族
;Z2的结构式是Cl-Cl
Cl-Cl
;(2)反应①的离子方程式是
2Cl-+2H2O 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑2Cl-+2H2O 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
; 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应.某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示(夹持固定装置的仪器已略去).

I、写出反应②的离子方程式
ClO-+Cl-+2H+=Cl2↑+H2O
ClO-+Cl-+2H+=Cl2↑+H2O
;II、上述实验装置不够完善,改进方法是
在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl
在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl
;Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是
2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2
2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2
.短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1:1的离子化合物A,X与Z能形成原子个数比为1:1的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):
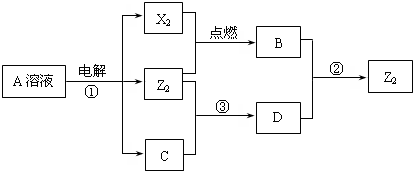
(1)Y在周期表的位置是第三周期第IA族第三周期第IA族;Z2的结构式是Cl-ClCl-Cl;
(2)反应①的离子方程式是2Cl-+2H2O

2OH-+Cl2↑+H2↑2Cl-+2H2O

2OH-+Cl2↑+H2↑;
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应.某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示(夹持固定装置的仪器已略去).
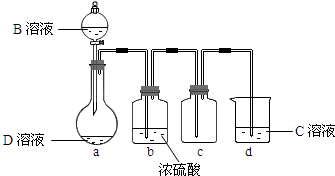
I、写出反应②的离子方程式ClO-+Cl-+2H+=Cl2↑+H2OClO-+Cl-+2H+=Cl2↑+H2O;
II、上述实验装置不够完善,改进方法是在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl;
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br22Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2.
查看习题详情和答案>>

(1)Y在周期表的位置是第三周期第IA族第三周期第IA族;Z2的结构式是Cl-ClCl-Cl;
(2)反应①的离子方程式是2Cl-+2H2O

2OH-+Cl2↑+H2↑2Cl-+2H2O

2OH-+Cl2↑+H2↑;
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应.某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示(夹持固定装置的仪器已略去).

I、写出反应②的离子方程式ClO-+Cl-+2H+=Cl2↑+H2OClO-+Cl-+2H+=Cl2↑+H2O;
II、上述实验装置不够完善,改进方法是在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl;
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br22Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2.