摘要:A.B.C.D.E.F六种短周期元素的原子序数依次增大.已知A.C.F三原子的最外层共有11个电子.且这三种元素的最高价氧化物的水化物之间两两皆能反应.均能生成盐和水.D元素原子的最外层电子数比次外层电子数少4个.E元素原子的次外层电子数比最外层电子数多3个.试完成下列问题: (1)写出下列元素的符号:A .D .E . (2)用电子式表示B.F形成的化合物 . (3)A.C两种元素最高价氧化物的水化物之间反应的离子方程式是 . (4)D的固态氧化物是 晶体.含n mol D的氧化物的晶体中含D-O共价键为 mol. 答案: (2) 3+OH-====+2H2O 解析:本题考查的是思维的严密性和连续性.是原子结构.周期表及元素化合物知识的综合应用.A.C.F三种元素最高价氧化物的水化物之间两两皆能反应.均能生成盐和水.确定其一必为Al.D原子的最外层电子数比次外层电子数少4个.确定D为Si.E原子的次外层电子数比最外层电子数多3个.确定E为P.又A.B.C.D.E.F六种短周期元素的原子序数依次增大.且A.C.F三原子的最外层共有11个电子.故A为Na.B为Mg.C为Al.F为Cl.在SiO2晶体中每个Si原子形成4个Si-O键.
网址:http://m.1010jiajiao.com/timu3_id_1219721[举报]
A、B、C、D、E、F六种短周期元素的原子序数依次增大,已知:①A原子核内只有1个质子;②B原子最外层电子数是次外层电子数的2倍;③C原子最外层电子数比次外层电子数多4个;④D原子的次外层电子数是最外层电子数的8倍;⑤E单质既能和盐酸反应又能和烧碱反应;⑥F与C同主族.用化学符号或化学用语回答下列问题:
(1)用电子式表示下列物质A2C2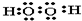
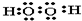 ,DCA
,DCA
 ;
;
(2)用电子式表示D与F形成化合物的过程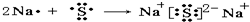
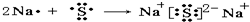 ;
;
(3)用“化学式”和“<或>”比较:A与C、A与F形成化合物的稳定性
(4)写出E与烧碱反应的离子方程式
查看习题详情和答案>>
(1)用电子式表示下列物质A2C2
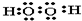
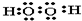


(2)用电子式表示D与F形成化合物的过程
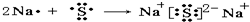
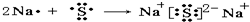
(3)用“化学式”和“<或>”比较:A与C、A与F形成化合物的稳定性
H2O>H2S
H2O>H2S
;沸点的高低H2O>H2S
H2O>H2S
,沸点高低的原因H2O分子间存在氢键
H2O分子间存在氢键
;(4)写出E与烧碱反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.A、B、C、D、E、F六种短周期元素的原子序数依次增大.A是宇宙中含量最丰元素,B元素的原子价电子排布为nsnnpn,D元素的最外层电子数是其电子层数的3倍,F的最高价氧化物对应水化物有两性,能溶于C、E的最高价氧化物对应水化物中.试回答:
(1)写出C原子的价层电子轨道表示式: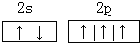
 ;D原子的价层电子排布式:
;D原子的价层电子排布式: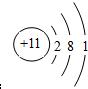
 ;
;
(2)B位于元素周期表的第
(3)C的基态原子核外有
(4)E单质在空气中燃烧生成物的电子式: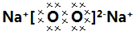
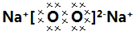 ,其中的阳离子与阴离子的个数比是
,其中的阳离子与阴离子的个数比是
(5)F的固态氧化物的用途有
查看习题详情和答案>>
(1)写出C原子的价层电子轨道表示式:


2s22p4
2s22p4
,E的原子结构示意图:

(2)B位于元素周期表的第
IVA
IVA
族,A、B形成原子个数比1:1且直线形分子的结构式:H-C≡C-H
H-C≡C-H
;(3)C的基态原子核外有
7
7
种不同运动状态的电子;(4)E单质在空气中燃烧生成物的电子式:
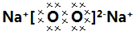
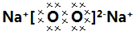
2:1
2:1
;(5)F的固态氧化物的用途有
耐火材料
耐火材料
(说出一种).F的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是4Al+3TiO2+3C
2Al2O3+3TiC
| ||
4Al+3TiO2+3C
2Al2O3+3TiC
.
| ||
A、B、C、D、E、F六种短周期元素的原子序数依次增大,已知:①A原子核内只有1个质子;②B原子最外层电子数是次外层电子数的2倍;③C原子最外层电子数比次外层电子数多4个;④D原子的次外层电子数是最外层电子数的8倍;⑤E单质既能和盐酸反应,又能和烧碱反应;⑥F与C同主族.用化学符号回答下列问题:
(1)用电子式表示下列物质A2C2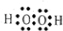
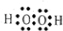 ,DCA
,DCA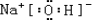
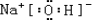 ;
;
(2)写出E与烧碱反应的离子方程式
(3)写出DCA与B的最高价氧化物反应的化学方程式:
查看习题详情和答案>>
(1)用电子式表示下列物质A2C2
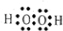
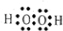
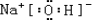
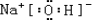
(2)写出E与烧碱反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.(3)写出DCA与B的最高价氧化物反应的化学方程式:
2NaOH+CO2=Na2CO3+H2O或NaOH+CO2=NaHCO3
2NaOH+CO2=Na2CO3+H2O或NaOH+CO2=NaHCO3
.A、B、C、D、E、F六种短周期元素的原子序数依次增大.B、E同主族,C、F也同主族,B、C同周期.A与B组成的化合物甲为气态,其中A、B原子个数比为4:1.由A与C组成的两种化合物乙与丙均为液态,乙中A、C原子个数比为1:1,丙中A、C原子个数比为2:1.一个D+离子中含有10个电子,D与C可以组成阳离子与阴离个数比为2:1,且相对分子质量为78的化合物丁.回答下列问题:
(1)甲、丁的电子式:甲 ,丁 ;BC2的结构式 ;F离子的结构示意图 .
(2)①原子半径:D E(填“>”或“<”,下同),
②最高价氧化物对应水化物的酸性:B E,
③稳定单质的熔点:B C.
(3)BC2属于 晶体,EC2属于 晶体(填:原子、分子、离子、金属).
(4)由A、C、D组成的常见化合物中含有的化学键有 .
(5)乙的水溶液与FC2反应的化学方程式 .
查看习题详情和答案>>
(1)甲、丁的电子式:甲
(2)①原子半径:D
②最高价氧化物对应水化物的酸性:B
③稳定单质的熔点:B
(3)BC2属于
(4)由A、C、D组成的常见化合物中含有的化学键有
(5)乙的水溶液与FC2反应的化学方程式
A、B、C、D、E、F六种短周期元素的原子序数依次增大。已知A、C、F三原子的最外层共有11个电子,且这三元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子数比次外层电子数少4,E元素原子的次外层电子数比最外层电子数多3。试回答:
(1)写出下列元素的符号:A_________,D_________,E_________。
(2)用电子式表示B、F形成化合物的过程:_____________________________________。
(3)A、C两种元素最高价氧化物的水化物反应的离子方程式:_________________________。
(4)D的固态氧化物是__________晶体,含n mol D的氧化物的晶体中含D—O共价键为____________mol。
查看习题详情和答案>>