摘要:同组的2个反应具有相同离子方程式的是( ) A.向NaHSO4和Na2SO4溶液中分别滴入少量Ba(OH)2溶液 B.向澄清石灰水中加入过量NaHCO3溶液.向NaHCO3溶液中加入过量澄清石灰水 C.向盐酸和氢碘酸中分别加入少量铁红粉(Fe2O3) D.向Na2SO3和K2SO3溶液中分别通入足量Cl2
网址:http://m.1010jiajiao.com/timu3_id_1217023[举报]
同组的2个反应具有相同离子方程式的是( )
A.向NaHSO4和Na2SO4溶液中分别滴入少量Ba(OH)2溶液
B.向澄清石灰水中加入过量NaHCO3溶液,向NaHCO3溶液中加入过量澄清石灰水
C.向盐酸和氢碘酸中分别加入少量铁红粉(Fe2O3)
D.向Na2SO3和K2SO3溶液中分别通入足量Cl2
查看习题详情和答案>>某化学兴趣小组的同学用如图所示实验装置进行研究,请对其方案进行完善或评价.

(1)浓硫酸和漂白粉可发生如下反应:
Ca(ClO)2+CaCl2+2H2SO4═2CaSO4+2Cl2↑+2H2O
实验室用此原理制取并收集氯气,可选用的装置组合是
(2)将A、C、D相连,利用实验室常用方法制取并收集氯气.在C中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
判断实验Ⅰ、Ⅱ推出相应结论是否合理;若合理,无需填写理由,若不合理,请说明.
实验Ⅰ:
(3)将A、C、D相连,可设计实验验证SO32-还原性强于Cl-.则C中发生反应的离子方程式是
查看习题详情和答案>>

(1)浓硫酸和漂白粉可发生如下反应:
Ca(ClO)2+CaCl2+2H2SO4═2CaSO4+2Cl2↑+2H2O
实验室用此原理制取并收集氯气,可选用的装置组合是
BCD
BCD
(填写装置序号)(2)将A、C、D相连,利用实验室常用方法制取并收集氯气.在C中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 |
实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气体产生 | 氯气与水反应的产物具有酸性 |
实验Ⅰ:
不合理
不合理
,理由没有事先证明干燥的氯气无漂白性
没有事先证明干燥的氯气无漂白性
;实验Ⅱ:不合理
不合理
,理由新制取的氯气中含HCl气体,溶于水也能与碳酸钠溶液反应产生气体
新制取的氯气中含HCl气体,溶于水也能与碳酸钠溶液反应产生气体
;(3)将A、C、D相连,可设计实验验证SO32-还原性强于Cl-.则C中发生反应的离子方程式是
SO32-+Cl2+H2O═SO42-+2Cl-+2H+
SO32-+Cl2+H2O═SO42-+2Cl-+2H+
;设计实验说明C中确实发生了上述反应(简述实验步骤、现象)取C中反应后的溶液少许,向其中电极盐酸酸化的氯化钡溶液,有白色沉淀生成
取C中反应后的溶液少许,向其中电极盐酸酸化的氯化钡溶液,有白色沉淀生成
.
某学习小组在通过反应Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O研究反应速率的影响因素后,对Na2S2O3产生了兴趣,查资料知Na2S2O3名称为硫代硫酸钠,俗称海波,可以看成是用一个S原子取代了Na2SO4中的一个O原子而形成.该实验小组运用类比学习的思想预测了Na2S2O3的某些性质,并通过实验探究验证自己的预测.
【提出假设】
(1)部分学生认为Na2S2O3与N2SO4结构相似,化学性质也相似,因此室温时Na2S2O3溶液的pH 7(填“>”、“=”或“<”).
(2)部分学生从S元素化合价推测Na2S2O3与SO2性质相似,均具有较强的 .
【实验探究】
取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)
【实验结论】
(6)探究①: .
(7)探究②: .
【问题讨论】
(8)甲同学向“探究②”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化.你认为该方案是否正确并说明理由 .
(9)请你重新设计二个实验方案,证明Na2S2O3被氯水氧化.你的方案是 .
查看习题详情和答案>>
【提出假设】
(1)部分学生认为Na2S2O3与N2SO4结构相似,化学性质也相似,因此室温时Na2S2O3溶液的pH
(2)部分学生从S元素化合价推测Na2S2O3与SO2性质相似,均具有较强的
【实验探究】
取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 探究① | (3) |
溶液pH=8 | (4) |
| 探究② | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (5) |
(6)探究①:
(7)探究②:
【问题讨论】
(8)甲同学向“探究②”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化.你认为该方案是否正确并说明理由
(9)请你重新设计二个实验方案,证明Na2S2O3被氯水氧化.你的方案是
某化学兴趣小组的同学用如图所示实验装置进行研究,请对其方案进行完善或评价.

(1)浓硫酸和漂白粉可发生如下反应:
Ca(ClO)2+CaCl2+2H2SO4═2CaSO4+2Cl2↑+2H2O
实验室用此原理制取并收集氯气,可选用的装置组合是______(填写装置序号)
(2)将A、C、D相连,利用实验室常用方法制取并收集氯气.在C中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气体产生 | 氯气与水反应的产物具有酸性 |
实验Ⅰ:______,理由______;实验Ⅱ:______,理由______;
(3)将A、C、D相连,可设计实验验证SO32-还原性强于Cl-.则C中发生反应的离子方程式是______;设计实验说明C中确实发生了上述反应(简述实验步骤、现象)______. 查看习题详情和答案>>
某化学兴趣小组的同学用如图所示实验装置进行研究,请对其方案进行完善或评价.
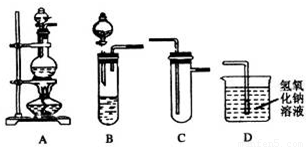
(1)浓硫酸和漂白粉可发生如下反应:
Ca(ClO)2+CaCl2+2H2SO4═2CaSO4+2Cl2↑+2H2O
实验室用此原理制取并收集氯气,可选用的装置组合是______(填写装置序号)
(2)将A、C、D相连,利用实验室常用方法制取并收集氯气.在C中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
判断实验Ⅰ、Ⅱ推出相应结论是否合理;若合理,无需填写理由,若不合理,请说明.
实验Ⅰ:______,理由______;实验Ⅱ:______,理由______;
(3)将A、C、D相连,可设计实验验证SO32-还原性强于Cl-.则C中发生反应的离子方程式是______;设计实验说明C中确实发生了上述反应(简述实验步骤、现象)______.
查看习题详情和答案>>

(1)浓硫酸和漂白粉可发生如下反应:
Ca(ClO)2+CaCl2+2H2SO4═2CaSO4+2Cl2↑+2H2O
实验室用此原理制取并收集氯气,可选用的装置组合是______(填写装置序号)
(2)将A、C、D相连,利用实验室常用方法制取并收集氯气.在C中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气体产生 | 氯气与水反应的产物具有酸性 |
实验Ⅰ:______,理由______;实验Ⅱ:______,理由______;
(3)将A、C、D相连,可设计实验验证SO32-还原性强于Cl-.则C中发生反应的离子方程式是______;设计实验说明C中确实发生了上述反应(简述实验步骤、现象)______.
查看习题详情和答案>>