摘要: 实验方案 实验现象 实验结论.化学方程式 方案一 看颜色和比较硬度法 Cu:黄色 Fe:银白色.质地坚硬 Al:银白色.质地较软 方案二 酸溶液法 不与酸反应的是铜.与酸反应速度快的是镁.另一个就是铁 Fe+2HCl=FeCl2+H2↑ Mg+2HCl=MgCl2+H2↑ Cu+HCl=不反应
网址:http://m.1010jiajiao.com/timu3_id_121414[举报]
22、化学课上,老师展示两瓶无标签的溶液,说:“它们分别是稀盐酸和氢氧化钠溶液.请同学们设计不同的区别方案,并进行实验”.
[交流与讨论]
几分钟后,我们设计了多种方案.
(1)我可以用二种不同的试剂来区别:
(2)交流实验方案时,小江同学设计的“用二氧化碳气体做试剂”引起了一场争论.
正方观点:可以区别;
反方观点:无法区别.
我赞同
[设计实验]
(3)验证氢氧化钠溶液与二氧化碳是否发生了反应,也可以从生成物的角度去探究,小涛利用提供的试剂(CaCl2溶液、盐酸、CaCO3固体、酚酞)对氢氧化钠溶液与二氧化碳是否发生了反应展开探究.他从提供的试剂中选取一种试剂进行实验发现原试液确已变质.取少量试液于试管中.滴入
[反思与评价]
(4)通过探究,让我明白:氢氧化钠溶液暴露在空气中会变质,故应
(5)通过探究,使用氢氧化钠和盐酸要注意安全,让我知道它们都具有
(6)探究小结时,小扬同学还提出:“碱与二氧化碳反应生成盐和水”,我还能写出二氧化碳与另一种碱反应的化学方程式
查看习题详情和答案>>
[交流与讨论]
几分钟后,我们设计了多种方案.
(1)我可以用二种不同的试剂来区别:
石蕊试液
、碳酸钠溶液
.(2)交流实验方案时,小江同学设计的“用二氧化碳气体做试剂”引起了一场争论.
正方观点:可以区别;
反方观点:无法区别.
我赞同
反方
(填“正方”或“反方”)的观点,其理由是虽二氧化碳不与盐酸反应,但氢氧化钠溶液中通入二氧化碳发生反应时无明显现象,因此不能对二者进行区别(合理即可,也可以赞同正方)
.[设计实验]
(3)验证氢氧化钠溶液与二氧化碳是否发生了反应,也可以从生成物的角度去探究,小涛利用提供的试剂(CaCl2溶液、盐酸、CaCO3固体、酚酞)对氢氧化钠溶液与二氧化碳是否发生了反应展开探究.他从提供的试剂中选取一种试剂进行实验发现原试液确已变质.取少量试液于试管中.滴入
盐酸(或CaCl2溶液)
,观察到有气泡产生(或有沉淀产生)
[反思与评价]
(4)通过探究,让我明白:氢氧化钠溶液暴露在空气中会变质,故应
密封
保存.(5)通过探究,使用氢氧化钠和盐酸要注意安全,让我知道它们都具有
很强的腐蚀
性.(6)探究小结时,小扬同学还提出:“碱与二氧化碳反应生成盐和水”,我还能写出二氧化碳与另一种碱反应的化学方程式
Ca(OH)2+CO2=CaCO3↓+H2O
.化学科代表和林民同学帮助实验老师整理化学药品室.发现分别放在两个试剂瓶中的两片用砂纸磨得光亮的银白色金属片,未贴上标签.到底它们是哪两种金属?两位同学首先对这两种金属X和Y的金属活动性顺序进行实验探究.
(1)进行猜想:①科代表猜想:活动性X大于Y
②林民同学猜想:活动性Y大于X
(2)设计实验方案、进行实验,获得结论.完成好如下实验报告,并回答后续有关问题.
(3)上述实验之前,实验老师只知道X、Y是银铁中的各一种,则根据实验结果说明Y就是
(4)实验老师经实验分析得知制得的Y粉末中含有未反应完的X粉末,同学们决定用化学方法将杂质X粉末除去,两个同学经讨论、交流一致认为可选用的除杂试剂是:
查看习题详情和答案>>
(1)进行猜想:①科代表猜想:活动性X大于Y
②林民同学猜想:活动性Y大于X
(2)设计实验方案、进行实验,获得结论.完成好如下实验报告,并回答后续有关问题.
| 实验步骤 | 实验现象 | 结论 |
将金属X、Y分别放入试管中, 将金属X、Y分别放入试管中, 再分别加入稀盐 再分别加入稀盐 或稀硫酸酸 或稀硫酸酸 | 金属Y表面无明显变化;金属X的表面有大量气泡冒出.将燃着的木条放在金属X的试管口,气体燃烧. | 科代表的猜想: 正确 正确 (“正确”或“不正确”) |
银或Ag
银或Ag
.实验室急需一定量的Y粉末.科代表认为可用现有的X金属粉末和Y的盐溶液、蒸馏水等药品,配以必要的仪器来制得急需的Y粉末,原因是(用反应的化学方程式表示):2AgNO3+Fe═2Ag+Fe(NO3)2
2AgNO3+Fe═2Ag+Fe(NO3)2
.(4)实验老师经实验分析得知制得的Y粉末中含有未反应完的X粉末,同学们决定用化学方法将杂质X粉末除去,两个同学经讨论、交流一致认为可选用的除杂试剂是:
盐酸(或稀硫酸)
盐酸(或稀硫酸)
.12、化学复习课上,老师将二氧化碳分别通入澄清的石灰水和氢氧化钠溶液中,我们观察到前者变浑浊,后者无明显现象.
我们的疑惑:二氧化碳和氢氧化钠是否确实发生了化学反应?
(1)我设计了如图实验装置来验证,实验现象是:软塑料瓶变瘪了.
小军同学认为我的实验是可行的,请你解释其中的原理是:
(2)小余同学认为还可以利用上述实验不同的原理,设计如下实验方案,请你帮他完成
方案①中滴加盐酸后发生反应的化学方程式是
查看习题详情和答案>>
我们的疑惑:二氧化碳和氢氧化钠是否确实发生了化学反应?
(1)我设计了如图实验装置来验证,实验现象是:软塑料瓶变瘪了.
小军同学认为我的实验是可行的,请你解释其中的原理是:
氢氧化钠溶液消耗CO2,使气体压强减小
.(2)小余同学认为还可以利用上述实验不同的原理,设计如下实验方案,请你帮他完成
| 方案 | 实验步骤 | 滴加试剂 | 实验现象 | 实验结论 |
| 方案 ① |
 |
稀盐酸 | 现象: 产生气泡. |
二氧化碳确实和氢氧化钠发生了化学反应 |
| 方案 ② |
CaCl2溶液 |
现象: 有白色沉淀产生 |
Na2CO3+2HCl=2NaCl+CO2↑+H2O
.
化学老师谢××交给某研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质.该小组的同学进行了如下实验探究:
【提出问题】猜想I:没变质,全部是NaOH;
猜想II:部分变质,既含有NaOH,又含有Na2CO3;
猜想Ⅲ:完全变质,全部是Na2CO3.
【查阅资料】①已知反应:BaCl2+Na2CO3=2NaCl+BaCO3↓
②部分盐溶液在常温下的pH如下:
【设计方案并进行实验】请你与他们一起共同完成,并回答所给问题.
上述步骤①中,所用称量仪器的名称是 ,滴加过量BaCl2溶液的目的是 .
【实验结论】通过实验,说明上述猜想中 是正确的.
【拓展】该小组同学为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为2.0g,则原试剂中NaOH的质量分数为 (假定试剂中无其它杂质).
【反思】久置的氢氧化钠变质的原因是 (用化学方程式表示).
查看习题详情和答案>>
【提出问题】猜想I:没变质,全部是NaOH;
猜想II:部分变质,既含有NaOH,又含有Na2CO3;
猜想Ⅲ:完全变质,全部是Na2CO3.
【查阅资料】①已知反应:BaCl2+Na2CO3=2NaCl+BaCO3↓
②部分盐溶液在常温下的pH如下:
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50mL水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块儿pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有 |
【实验结论】通过实验,说明上述猜想中
【拓展】该小组同学为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为2.0g,则原试剂中NaOH的质量分数为
【反思】久置的氢氧化钠变质的原因是
7、化学兴趣小组同学在进行“碱的性质”探究实验过程中,甲乙两组同学分别向相同体积的石灰水和烧碱溶液中,同时通入CO2气体,前者变浑浊,后者未见明显现象.对此,甲组同学认为:CO2能与石灰水反应,不能与烧碱溶液反应.乙组同学认为:甲组同学的结论不完全正确.乙组同学如何用实验证明自己的观点呢?请你利用下面的实验用品帮助他们完成以下实验方案.
(1)提出假设:烧碱溶液也能与CO2发生反应.
(2)设计方案:
①制取CO2气体;
a.化学反应原理(用化学方程式表示):
b.请你从下图中,选出正确的发生装置(填字母)
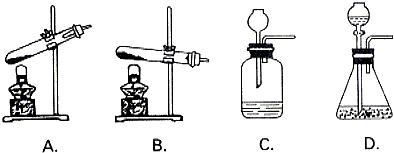
②组装实验装置:(除需要烧碱溶液外)还应选择下列装置中的
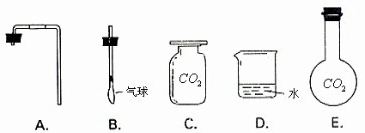
③验证假设进行实验:
④反思与应用:
a.本实验从反应物的角度,利用
b.在实验室中,久置的烧碱溶液会变质,其原因是(写化学方程式)
查看习题详情和答案>>
(1)提出假设:烧碱溶液也能与CO2发生反应.
(2)设计方案:
①制取CO2气体;
a.化学反应原理(用化学方程式表示):
CaCO3+2HCl=CaCl2+H2O+CO2↑
.b.请你从下图中,选出正确的发生装置(填字母)
D
,选择该装置的理由是
反应物为固体和液体,反应不需加热
.往装置中加药品前一定要
检查装置气密性
.
②组装实验装置:(除需要烧碱溶液外)还应选择下列装置中的
EB或EAD
.(填字母) 
③验证假设进行实验:

④反思与应用:
a.本实验从反应物的角度,利用
压强
的改变验证了反应的发生.b.在实验室中,久置的烧碱溶液会变质,其原因是(写化学方程式)
2NaOH+CO2=Na2CO3+H2O
.因此,烧碱溶液应
密封
保存.