摘要:下列性质属于物理性质的是( ) A. 的还原性, B.酒精的挥发性, C.铁在潮湿的空气中会生锈, D. 使澄清石灰水变浑浊.
网址:http://m.1010jiajiao.com/timu3_id_119687[举报]
 实验室常里用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;
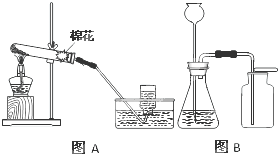
实验室常里用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.实验室制取氧气常用装置如下列图A、图B所示.请回答有关问题:
(1)请仔细分析图A的特点,推测所用制取氧气的方法是
b
b
(填“a”、“b”、“c”),写出该方法制取氧气的文字表达式
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
该反应属于| 加热 |
分解
分解
反应.A中的试管口应略向下倾斜原因是防止冷凝水倒流引起试管炸裂
防止冷凝水倒流引起试管炸裂
.(2)采用c方法制氧气,应选用装置
B
B
(填“图A”、“图B”).为检验装置B中氧气是否收集满,可用带火星的木条放在集气瓶口,这是利用了氧气支持燃烧
支持燃烧
的性质.利用图A装置制氧气,在结束实验时要先撤离导管出水面,再熄灭酒精灯,其目的是防止水倒流引起试管炸裂
防止水倒流引起试管炸裂
;利用图B装置制氧气时,长颈漏斗的下端要插入液面以下,其目的是防止装置漏气(或防止气体从长颈漏斗逸出)
防止装置漏气(或防止气体从长颈漏斗逸出)
.(3)实验室里,常用氯化铵晶体跟氢氧化钙粉末混合加热制取氨气.它是一种无色的,有刺激性气味的,密度比空气小,而溶于水且能跟水反应生成氨水的气体,制取氨气过程中还有氯化钙和水生成.实验室制取氨气可选用的发生装置为
A
A
(填“A”或“B”),其理由是反应物为固体,需要加热
反应物为固体,需要加热
;收集氨气可用向下排空气
向下排空气
法,理由是氨气的密度比空气小、溶于水
氨气的密度比空气小、溶于水
.(1)物质连连看:根据左栏物质的描述,在右栏中找出对应的物质的序号,填在横线上.
| 物质的描述 | 备选物质 |
| ①我能让气球飞起来,却不能燃烧 | A. 木炭 |
| ②我可以制汽水,也会引起温室效应 | B. 氦气 |
| ③我可以制造硝酸和氮肥 | C. 二氧化碳 |
| ④我有毒,可以和血红蛋白结合 | D. 氮气 |
| ⑤我是黑色固体,有还原性 | E.一氧化碳 |
(2)化学基础知识是学好化学的关键,请按下列要求填空.

|
Ⅰ.图1是某微粒的结构示意图.该微粒在化学反应中失去电子后形成粒子的符号 .
Ⅱ.写出一条从图2中获得的信息 .
Ⅲ.如图3所示是汽车尾气治理过程中某反应的微观示意图.其中属于化合物的有 ;生成C和D的质量比为 .
(3)除杂和推断是初中化学一种常见的题型.
Ⅰ.除去二氧化碳中混有的少量一氧化碳可用( );除去氧化铜混有的中少量碳粉可用( )
A.澄清石灰水 B.灼热氧化铜 C.点燃的方法
 D.在密闭容器中加强热 E.在氧气流中灼烧
D.在密闭容器中加强热 E.在氧气流中灼烧
Ⅱ.甲、乙、丙是初中化学中常见的三种物质,它们之间的转化
关系如图所示.“→”表示由一种物质转化成另一种物质(图中反应
条件及物质略去).
请分析:如果甲是单质,甲可能是 .
如果甲是化合物,甲可能是 .
查看习题详情和答案>>
绿矾(FeSO4?7H2O)、硫酸亚铁铵(FeSO4?(NH4)2SO4?6H2O)是重要的化学化工试剂.工业上常利用机械加工行业产生的废铁屑为原料制备.这种废铁屑中常混有FeS(其它杂质忽略不计),与稀硫酸反应为:FeS+H2SO4=FeSO4+H2S↑,H2S有毒,水溶液名称为氢硫酸.
请回答下列问题:
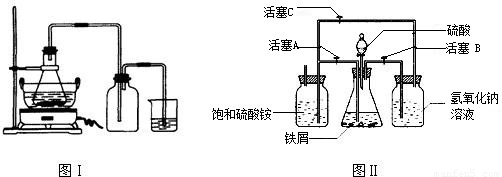
(1)图Ⅰ用于制备绿矾.锥形瓶中反应产生绿矾,其中盛放的药品或原料是______,发生的反应除前述化学方程式外,还一定有 (写化学方程式):______.
若知集气瓶的作用是作安全瓶,烧杯中发生的反应是:CuSO4+H2S=CuS↓+H2SO4,则烧杯中盛放的试剂是______,其作用为______.
(2)图Ⅱ用于制备硫酸亚铁铵(已知亚铁盐容易被氧化).在0~60℃的温度范围内,硫酸亚铁铵在水中的溶解度比硫酸铵、硫酸亚铁的溶解度小,所以硫酸亚铁与硫酸铵的混合溶液冷却至室温便析出硫酸亚铁铵.
具体操作:①打开活塞______,关闭活塞______,从______(填仪器名称)中滴下稀H2SO4到250mL规格的锥形瓶中,充分反应.②待锥形瓶中的铁屑快反应完时,关闭活塞______,打开活塞______.③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
实验中氢气的作用是______,
氢氧化钠溶液的作用是______.
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁铵,并对产品质量进行检测.检测结果如下:
已知产品质量标准:Fe3+的质量分数等于0.005%,产品质量定为Ⅰ级;Fe3+的质量分数等于0.01%,产品质量定为Ⅱ级,从实验结果中,可得出制备硫酸亚铁溶液时,反应控制______过量为最佳.
(4)处理胶片的废液中含大量AgNO3、Zn(NO3)2和Fe(NO3)2,若随意排放不仅会造成严重的污染,而且造成资源浪费.某同学从上述的废液中回收金属银并得到副产品绿矾(FeSO4?7H2O),其回收流程如下:
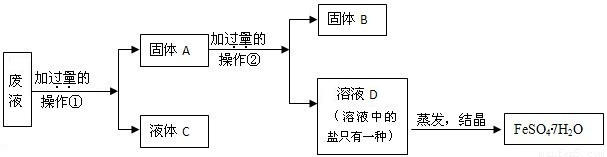
操作②是______,固体A中含______,固体B是______,
x是______,y是______,x、y过量的共同作用是______.
(5)硫酸最古老的生产方法是:把绿矾(FeSO4?7H2O)装入反应器中加强热,会流出油状液体,并放出有刺激性气味的气体(SO2),反应器中的固体变为红色.这个变化的过程可用两个化学方式表示.
①______ Fe2O3+SO2↑+SO3↑+14H2O 查看习题详情和答案>>

请回答下列问题:
(1)图Ⅰ用于制备绿矾.锥形瓶中反应产生绿矾,其中盛放的药品或原料是______,发生的反应除前述化学方程式外,还一定有 (写化学方程式):______.
若知集气瓶的作用是作安全瓶,烧杯中发生的反应是:CuSO4+H2S=CuS↓+H2SO4,则烧杯中盛放的试剂是______,其作用为______.
(2)图Ⅱ用于制备硫酸亚铁铵(已知亚铁盐容易被氧化).在0~60℃的温度范围内,硫酸亚铁铵在水中的溶解度比硫酸铵、硫酸亚铁的溶解度小,所以硫酸亚铁与硫酸铵的混合溶液冷却至室温便析出硫酸亚铁铵.
具体操作:①打开活塞______,关闭活塞______,从______(填仪器名称)中滴下稀H2SO4到250mL规格的锥形瓶中,充分反应.②待锥形瓶中的铁屑快反应完时,关闭活塞______,打开活塞______.③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
实验中氢气的作用是______,
氢氧化钠溶液的作用是______.
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁铵,并对产品质量进行检测.检测结果如下:
| 序号 | 反应物用量(n表示微粒个数) | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于1级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于1级 |
(4)处理胶片的废液中含大量AgNO3、Zn(NO3)2和Fe(NO3)2,若随意排放不仅会造成严重的污染,而且造成资源浪费.某同学从上述的废液中回收金属银并得到副产品绿矾(FeSO4?7H2O),其回收流程如下:

操作②是______,固体A中含______,固体B是______,
x是______,y是______,x、y过量的共同作用是______.
(5)硫酸最古老的生产方法是:把绿矾(FeSO4?7H2O)装入反应器中加强热,会流出油状液体,并放出有刺激性气味的气体(SO2),反应器中的固体变为红色.这个变化的过程可用两个化学方式表示.
①______ Fe2O3+SO2↑+SO3↑+14H2O 查看习题详情和答案>>
绿矾(FeSO4?7H2O)、硫酸亚铁铵(FeSO4?(NH4)2SO4?6H2O)是重要的化学化工试剂.工业上常利用机械加工行业产生的废铁屑为原料制备.这种废铁屑中常混有FeS(其它杂质忽略不计),与稀硫酸反应为:FeS+H2SO4=FeSO4+H2S↑,H2S有毒,水溶液名称为氢硫酸.

请回答下列问题:
(1)图Ⅰ用于制备绿矾.锥形瓶中反应产生绿矾,其中盛放的药品或原料是______,发生的反应除前述化学方程式外,还一定有 (写化学方程式):______.
若知集气瓶的作用是作安全瓶,烧杯中发生的反应是:CuSO4+H2S=CuS↓+H2SO4,则烧杯中盛放的试剂是______,其作用为______.
(2)图Ⅱ用于制备硫酸亚铁铵(已知亚铁盐容易被氧化).在0~60℃的温度范围内,硫酸亚铁铵在水中的溶解度比硫酸铵、硫酸亚铁的溶解度小,所以硫酸亚铁与硫酸铵的混合溶液冷却至室温便析出硫酸亚铁铵.
具体操作:①打开活塞______,关闭活塞______,从______(填仪器名称)中滴下稀H2SO4到250mL规格的锥形瓶中,充分反应.②待锥形瓶中的铁屑快反应完时,关闭活塞______,打开活塞______.③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
实验中氢气的作用是______,
氢氧化钠溶液的作用是______.
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁铵,并对产品质量进行检测.检测结果如下:
已知产品质量标准:Fe3+的质量分数等于0.005%,产品质量定为Ⅰ级;Fe3+的质量分数等于0.01%,产品质量定为Ⅱ级,从实验结果中,可得出制备硫酸亚铁溶液时,反应控制______过量为最佳.
(4)处理胶片的废液中含大量AgNO3、Zn(NO3)2和Fe(NO3)2,若随意排放不仅会造成严重的污染,而且造成资源浪费.某同学从上述的废液中回收金属银并得到副产品绿矾(FeSO4?7H2O),其回收流程如下:

操作②是______,固体A中含______,固体B是______,
x是______,y是______,x、y过量的共同作用是______.
(5)硫酸最古老的生产方法是:把绿矾(FeSO4?7H2O)装入反应器中加强热,会流出油状液体,并放出有刺激性气味的气体(SO2),反应器中的固体变为红色.这个变化的过程可用两个化学方式表示.
①______ Fe2O3+SO2↑+SO3↑+14H2O 查看习题详情和答案>>

请回答下列问题:
(1)图Ⅰ用于制备绿矾.锥形瓶中反应产生绿矾,其中盛放的药品或原料是______,发生的反应除前述化学方程式外,还一定有 (写化学方程式):______.
若知集气瓶的作用是作安全瓶,烧杯中发生的反应是:CuSO4+H2S=CuS↓+H2SO4,则烧杯中盛放的试剂是______,其作用为______.
(2)图Ⅱ用于制备硫酸亚铁铵(已知亚铁盐容易被氧化).在0~60℃的温度范围内,硫酸亚铁铵在水中的溶解度比硫酸铵、硫酸亚铁的溶解度小,所以硫酸亚铁与硫酸铵的混合溶液冷却至室温便析出硫酸亚铁铵.
具体操作:①打开活塞______,关闭活塞______,从______(填仪器名称)中滴下稀H2SO4到250mL规格的锥形瓶中,充分反应.②待锥形瓶中的铁屑快反应完时,关闭活塞______,打开活塞______.③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
实验中氢气的作用是______,
氢氧化钠溶液的作用是______.
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁铵,并对产品质量进行检测.检测结果如下:
| 序号 | 反应物用量(n表示微粒个数) | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于1级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于1级 |
(4)处理胶片的废液中含大量AgNO3、Zn(NO3)2和Fe(NO3)2,若随意排放不仅会造成严重的污染,而且造成资源浪费.某同学从上述的废液中回收金属银并得到副产品绿矾(FeSO4?7H2O),其回收流程如下:

操作②是______,固体A中含______,固体B是______,
x是______,y是______,x、y过量的共同作用是______.
(5)硫酸最古老的生产方法是:把绿矾(FeSO4?7H2O)装入反应器中加强热,会流出油状液体,并放出有刺激性气味的气体(SO2),反应器中的固体变为红色.这个变化的过程可用两个化学方式表示.
①______ Fe2O3+SO2↑+SO3↑+14H2O 查看习题详情和答案>>
 2010年上海世博会的主题是“城市,让生活更美好”.
2010年上海世博会的主题是“城市,让生活更美好”.(1)在世博会中应用了下列技术,其中能有效实现“节能环保”的是
ABC
ABC
.A.采用水循环为场馆降温
B.用竹、藤等天然材料建造场馆
C.构建生态绿化墙面
(2)由上汽集团自主研发的“叶子”概念车(如图所示)在中国馆低碳区展出,该车顶部的“大叶子”是一部光电转化器,把
光或太阳
光或太阳
能转化为电能.(3)次氯酸钠(NaClO)消毒剂是常用的饮用水消毒剂之一,它的消毒原理是NaClO溶于水发生水解生成次氯酸(HClO);利用HClO的强氧化性消毒杀菌.如果保存不当,NaClO还会与空气中的二氧化碳和水反应生成碳酸钠和次氯酸,次氯酸分解致使消毒剂变质而失效.用NaClO对饮用水进行消毒杀菌的方法属于
化学
化学
填:“物理”或“化学”)方法;在运输和储存NaClO消毒剂时,应注意密封
密封
保存.