摘要:12.氯化硼(BCl3)的熔点为-107℃.沸点为12.5℃.在其分子中键与键之间的夹角为120o.它能水解.有关叙述正确的是 A.氯化硼是电解质 B.氯化硼的水溶液能导电 C.氯化硼分子呈正三角形.属非极性分子 D.氯化硼B-Cl之间是sp3形成的σ键
网址:http://m.1010jiajiao.com/timu3_id_112482[举报]
化学与生活息息相关.
(1)食用下列食品所获取的主要营养素是 .

(2)锅里的油一旦着火,可用锅盖盖灭,其原理是 .
(3)埋藏于海底将来可能会替代化石燃料的新能源是 .
(4)餐具上的油污用加入洗洁精的水更容易洗掉,原因是洗洁精具有 作用.
(5)稀土元素铕是激光及原子能应用的重要材料.已知氯化铕的化学式为EuCl3,则氧化铕的化学式为 .
查看习题详情和答案>>
(1)食用下列食品所获取的主要营养素是

(2)锅里的油一旦着火,可用锅盖盖灭,其原理是
(3)埋藏于海底将来可能会替代化石燃料的新能源是
(4)餐具上的油污用加入洗洁精的水更容易洗掉,原因是洗洁精具有
(5)稀土元素铕是激光及原子能应用的重要材料.已知氯化铕的化学式为EuCl3,则氧化铕的化学式为
 (2013?闵行区一模)水和溶液在生命活动和生产、生活中起着十分重要的作用.回答下面有关水的问题.
(2013?闵行区一模)水和溶液在生命活动和生产、生活中起着十分重要的作用.回答下面有关水的问题.(1)如图是电解水的实验装置图,B为电源的
正
正
极,甲管内收集到的气体是氢气
氢气
.(2)净水器中有活性炭,活性炭起到
吸附
吸附
的作用.(3)自来水生产过程中常用明矾或氯化铁作凝聚剂,请写出氯化铁的化学式为
FeCl3
FeCl3
.(4)汽车、电动车一般使用铅酸蓄电池.某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸.若用100g质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸时,需要蒸馏水(密度为1g/cm3)的体积为
390
390
mL.
生石灰是重要的建筑材料,也常用作食品干燥剂.生石灰是通过高温锻烧石灰石制取的,所需的石灰石原料中碳酸钙的含量(纯度)要求在85%以上,小江同学为了寻找纯度符合要求的石灰石原料,对一石灰石样品进行了如下定量实验.
(1)写出实验中发生反应的化学方程式:
通过计算回答:
(2)该实验中生成的二氧化碳的质量是 g.
(3)假设石灰石样品中的杂质不与盐酸反应也不溶于水,则该样品中含碳酸钙的质量为 g.
(4)该石灰石样品的纯度是 .
(5)结论:计算结果显示,该石灰石样品的纯度 (符合或不符合)要求.
查看习题详情和答案>>
| 实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验图示 |  | |||
| 实验数据 | 烧杯的质量为 50.0g |
烧杯和盐酸的质量为 100.0g |
石灰石样品样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
通过计算回答:
(2)该实验中生成的二氧化碳的质量是
(3)假设石灰石样品中的杂质不与盐酸反应也不溶于水,则该样品中含碳酸钙的质量为
(4)该石灰石样品的纯度是
(5)结论:计算结果显示,该石灰石样品的纯度
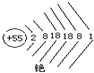 铯元素(Cs)是元素周期表中第55号元素,其相对原子质量为133,其原子结构示意图
铯元素(Cs)是元素周期表中第55号元素,其相对原子质量为133,其原子结构示意图如下图所示.回答下列问题:
(1)铯原子核外有
6
6
个电子层,最外层电子数为1
1
.(2)铯元素的化学性质与钠元素
相似
相似
(填“相似”或“不相似”),它是一种金属
金属
(填“金属”或“非金属”)元素,氯化铯的化学式为CsCl
CsCl
.(3)铯元素所形成的碳酸盐的化学式是
Cs2CO3
Cs2CO3
,铯元素形成的碱的化学式为CsOH
CsOH
.
石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水) 查看习题详情和答案>>
| 实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验图示 |  | |||
| 实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为100.0g | 石灰石样品样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水) 查看习题详情和答案>>