摘要:熟石灰是常见的碱.在生产中有很多用途. (1)由生石灰制取熟石灰的化学方程式 . (2)用石灰沙浆抹墙壁.墙壁面逐渐变得坚固.反应的化学方程式 . (3)除用上述用途外.再举出一个应用熟石灰的实例 .
网址:http://m.1010jiajiao.com/timu3_id_112054[举报]
方海同学在学习“常见的碱”时,提出如下问题:
①检验少量二氧化碳为什么一般用澄清石灰水而不用NaOH溶液?
②实验时吸收较多的CO2为什么一般用NaOH溶液而不用澄清石灰水?
【查阅资料】a.20℃时,熟石灰的溶解度为0.17g;b.熟石灰的溶解度随着温度升高而降低.
【实验探究】在教师指导下,方海同学进行了如下实验探究:
探究一、关于二氧化碳的检验
Ⅰ.在甲、乙、丙三支试管中加入等量NaOH或Ca(OH)2 溶液(如下图),在甲、乙中分别通入少量CO2.

Ⅱ.在实验后的乙和丙两种澄清溶液中,分别滴入足量稀盐酸(如下图).

回答问题:
(1)Ⅰ中甲、乙二支试管的现象分别是______.
(2)Ⅱ中乙试管可观察到有气泡产生,写出该反应的化学方程式:______;设计丙试管实验的目的是______.
【得出结论】检验少量CO2一般用石灰水而不用NaOH溶液.
探究二、关于二氧化碳的吸收
Ⅲ.进行如下图所示实验:

【实验现象】甲试管:液面上升最少;乙试管:液面上升较甲略高;
丙试管:倒吸接近完全,仅在管底留有一小气泡.
(3)小刚认为,可直接配制10%的石灰水代替甲中0.17%的石灰水,与丙进行对比实验.你同意小刚的观点吗?答:______(填“同意”或“不同意”),理由是______(4)比较乙、丙中进入试管内液体体积,得出的结论是______.
【得出结论】实验时吸收CO2选用较浓的NaOH溶液而不用Ca(OH)2溶液的理由是______.
【实验拓展】为了直观地观察到CO2与NaOH反应后的现象,再利用右图装置进行实验.随着NaOH溶液的滴入,可观察到的现象是______.
查看习题详情和答案>>
24、芋艿是一种常见的食品,既可当粮食,又可作蔬菜.
(1)新鲜芋艿在去皮时会产生一种白色汁液,汁液内台有一种碱性物质一皂角甙,沾上它会奇痒难忍.下列物质可用来涂抹止痒的是
A.食醋 B.熟石灰 C.纯碱
(2)有经验的人遇到这种情况,会将手靠近火源烘一烘,也可以达到止痒的效果;如果将带皮芋艿煮熟后,再用手去皮也不再会有痒的感觉.根据上述现象,请休推涮皂角甙的一种化学性质;
(3)去皮的芋艿在自然条件下,表面很快因氧化而变黄色,但并不影响营养价值.有些不法商贩会用亚硫酸钠溶液浸泡.便其外观变得嫩白.造成食品安全问题.下面做{去也会带来食品安全问题的是
A.粮库内充入氮气使粮食不易变质B.食盐中加碘防止甲状腺肿大
C.水发海产品用甲醛溶液保鲜 D.甩纯碱除去面团发酵产生的酸.
查看习题详情和答案>>
(1)新鲜芋艿在去皮时会产生一种白色汁液,汁液内台有一种碱性物质一皂角甙,沾上它会奇痒难忍.下列物质可用来涂抹止痒的是
A
.A.食醋 B.熟石灰 C.纯碱
(2)有经验的人遇到这种情况,会将手靠近火源烘一烘,也可以达到止痒的效果;如果将带皮芋艿煮熟后,再用手去皮也不再会有痒的感觉.根据上述现象,请休推涮皂角甙的一种化学性质;
受热要分解(写不稳定、易分解、受热易变质等含义正确也可)
.(3)去皮的芋艿在自然条件下,表面很快因氧化而变黄色,但并不影响营养价值.有些不法商贩会用亚硫酸钠溶液浸泡.便其外观变得嫩白.造成食品安全问题.下面做{去也会带来食品安全问题的是
C
.A.粮库内充入氮气使粮食不易变质B.食盐中加碘防止甲状腺肿大
C.水发海产品用甲醛溶液保鲜 D.甩纯碱除去面团发酵产生的酸.
17、方海同学在学习“常见的碱”时,提出如下问题:
①检验少量二氧化碳为什么一般用澄清石灰水而不用NaOH溶液?
②实验时吸收较多的CO2为什么一般用NaOH溶液而不用澄清石灰水?
[查阅资料]a.20℃时,熟石灰的溶解度为0.17g;b.熟石灰的溶解度随着温度升高而降低.
[实验探究]在教师指导下,方海同学进行了如下实验探究:
探究一、关于二氧化碳的检验
Ⅰ.在甲、乙、丙三支试管中加入等量NaOH或Ca(OH)2 溶液(如下图),在甲、乙中分别通入少量CO2.
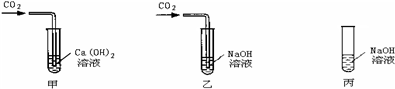
Ⅱ.在实验后的乙和丙两种澄清溶液中,分别滴入足量稀盐酸(如下图).

回答问题:
(1)Ⅰ中甲、乙二支试管的现象分别是
(2)Ⅱ中乙试管可观察到有气泡产生,写出该反应的化学方程式:
[得出结论]检验少量CO2一般用石灰水而不用NaOH溶液.
探究二、关于二氧化碳的吸收
Ⅲ.进行如下图所示实验:
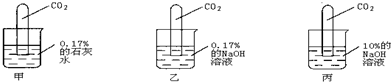
[实验现象]甲试管:液面上升最少; 乙试管:液面上升较甲略高;
丙试管:倒吸接近完全,仅在管底留有一小气泡.
(3)小刚认为,可直接配制10%的石灰水代替甲中0.17%的石灰水,与丙进行对比实验.你同意小刚的观点吗?答:
[得出结论]实验时吸收CO2选用较浓的NaOH溶液而不用Ca(OH)2溶液的理由是
[实验拓展]为了直观地观察到CO2与NaOH反应后的现象,再利用右图装置进行实验.随着NaOH溶液的滴入,可观察到的现象是
查看习题详情和答案>>
①检验少量二氧化碳为什么一般用澄清石灰水而不用NaOH溶液?
②实验时吸收较多的CO2为什么一般用NaOH溶液而不用澄清石灰水?
[查阅资料]a.20℃时,熟石灰的溶解度为0.17g;b.熟石灰的溶解度随着温度升高而降低.
[实验探究]在教师指导下,方海同学进行了如下实验探究:
探究一、关于二氧化碳的检验
Ⅰ.在甲、乙、丙三支试管中加入等量NaOH或Ca(OH)2 溶液(如下图),在甲、乙中分别通入少量CO2.

Ⅱ.在实验后的乙和丙两种澄清溶液中,分别滴入足量稀盐酸(如下图).

回答问题:
(1)Ⅰ中甲、乙二支试管的现象分别是
甲试管产生白色沉淀(或变浑浊),乙试管无明显现象
.(2)Ⅱ中乙试管可观察到有气泡产生,写出该反应的化学方程式:
Na2CO3+2HCl═2NaCl+CO2↑+H2O
;设计丙试管实验的目的是用作乙试管的对比实验,证明乙试管中CO2与NaOH发生了化学反应
.[得出结论]检验少量CO2一般用石灰水而不用NaOH溶液.
探究二、关于二氧化碳的吸收
Ⅲ.进行如下图所示实验:

[实验现象]甲试管:液面上升最少; 乙试管:液面上升较甲略高;
丙试管:倒吸接近完全,仅在管底留有一小气泡.
(3)小刚认为,可直接配制10%的石灰水代替甲中0.17%的石灰水,与丙进行对比实验.你同意小刚的观点吗?答:
不同意
(填“同意”或“不同意”),理由是20℃时,熟石灰的溶解度是0.17g,无法配制出10%的石灰水(或20℃时0.17%的石灰水是饱和溶液,石灰水的溶质质量分数不可能达到10%;其他合理答案也给分)
(4)比较乙、丙中进入试管内液体体积,得出的结论是NaOH溶液的溶质质量分数越大,吸收CO2能力越强
.[得出结论]实验时吸收CO2选用较浓的NaOH溶液而不用Ca(OH)2溶液的理由是
吸收时要尽量除尽CO2,NaOH极易溶于水,形成的溶液浓度大,吸收量多,效益高,而Ca(OH)2微溶,用它来吸收CO2要配大量溶液
.[实验拓展]为了直观地观察到CO2与NaOH反应后的现象,再利用右图装置进行实验.随着NaOH溶液的滴入,可观察到的现象是
小气球逐渐胀大
.氢氧化钠(NaOH)和氢氧化钙[Ca(OH)2]是常见的碱,在现实生活中有广泛的用途.根据所学知识回答:
(1)将氢氧化钠和氢氧化钙暴露在空气中都会变质生成某一类盐,该类盐的阴离子符号是
(2)实验室常用澄清的石灰水来检验二氧化碳,将饱和的石灰水溶液升高温度,溶液浓度将
(3)长期不合理使用化肥(例如使用硫酸铵)会使土壤酸化(含有硫酸),熟石灰常用来改良酸性土壤,反应的化学方程式是
(4)农业生产中常用氢氧化钙和硫酸铜配置波尔多液来防治果树的霉叶病等,配制波尔多液时
(5)氢氧化钠常用来干燥某些气体,其干燥原理是
查看习题详情和答案>>
(1)将氢氧化钠和氢氧化钙暴露在空气中都会变质生成某一类盐,该类盐的阴离子符号是
CO32-
CO32-
.(2)实验室常用澄清的石灰水来检验二氧化碳,将饱和的石灰水溶液升高温度,溶液浓度将
减小
减小
(填“增大”、“减小”或“不变”).(3)长期不合理使用化肥(例如使用硫酸铵)会使土壤酸化(含有硫酸),熟石灰常用来改良酸性土壤,反应的化学方程式是
Ca(OH)2+H2SO4═CaSO4↓+2H2O
Ca(OH)2+H2SO4═CaSO4↓+2H2O
.(4)农业生产中常用氢氧化钙和硫酸铜配置波尔多液来防治果树的霉叶病等,配制波尔多液时
不能
不能
(填“能”或“不能”)用铁制容器.(5)氢氧化钠常用来干燥某些气体,其干燥原理是
氢氧化钠易吸收水分
氢氧化钠易吸收水分
.氢氧化钠(NaOH)和氢氧化钙[Ca(OH)2]是常见的碱,在现实生活中有广泛的用途.根据所学知识回答:
(1)将氢氧化钠和氢氧化钙暴露在空气中都会变质生成某一类盐,该类盐的阴离子符号是
(2)实验室常用澄清的石灰水来检验二氧化碳,将饱和的石灰水溶液升高温度,溶液质量分数将
(3)长期不合理使用化肥(例如使用硫酸铵)会使土壤酸化(含有硫酸),熟石灰常用来改良酸性土壤,反应的化学方程式是
(4)农业生产中常用氢氧化钙和硫酸铜配置波尔多液来防治果树的霉叶病等,配制波尔多液时
查看习题详情和答案>>
(1)将氢氧化钠和氢氧化钙暴露在空气中都会变质生成某一类盐,该类盐的阴离子符号是
CO32-
CO32-
.(2)实验室常用澄清的石灰水来检验二氧化碳,将饱和的石灰水溶液升高温度,溶液质量分数将
减小
减小
(填“增大”、“减小”或“不变”).(3)长期不合理使用化肥(例如使用硫酸铵)会使土壤酸化(含有硫酸),熟石灰常用来改良酸性土壤,反应的化学方程式是
Ca(OH)2+H2SO4═CaSO4↓+2H2O
Ca(OH)2+H2SO4═CaSO4↓+2H2O
.(4)农业生产中常用氢氧化钙和硫酸铜配置波尔多液来防治果树的霉叶病等,配制波尔多液时
不能
不能
(填“能”或“不能”)用铁制容器.