摘要:在置换反应A+BC+D中, (1)若D为H2.B为稀硫酸.则A的选择应满足什么条件 . (2)若D为Cu.化合物B的物质类别可能为 (填“氧化物 “酸 “碱 或“盐 ). (3)某些非金属也有活动性顺序.已知在溶液中可发生下列反应.Cl2+2NaBr====2NaCl+Br2.Br2+2NaI====2NaBr+I2.则在I2.Cl2.Br2三种非金属中.活动性最强的是 .活动性最弱的是 . 解析:根据金属活动顺序表.结合题目信息.活泼金属或非金属能够置换出不活泼的金属或非金属单质. 答案:(1)此物质为位于金属活动顺序表氢元素前面的金属元素 Cl2 I2
网址:http://m.1010jiajiao.com/timu3_id_110707[举报]
 19、建立宏观、微观和符号之间的联系是化学学科的特点.
19、建立宏观、微观和符号之间的联系是化学学科的特点.(1)构成氯化钠的基本微粒是
离子
(填“分子”、“原子”或“离子”).(2)用符号表示下列微粒.2个氧原子
2O
;3个钠离子3Na+
.(3)A、B、C、D表示4种物质,其微观示意图见下表.A和B在一定条件下反应可生成C和D.下列说法正确的是
①③
(填数字序号).①4种物质均由分子构成 ②该反应属于置换反应
③C、D两种物质的质量比为11:7 ④4种物质中属于氧化物的是A、B.
 某同学用如图形式对所学知识进行归纳,其中甲包含了乙、丙、丁…下列关系中,有错误的一组是( ) 某同学用如图形式对所学知识进行归纳,其中甲包含了乙、丙、丁…下列关系中,有错误的一组是( )
|
| A、A | B、B | C、C | D、D |
(2013?常熟市模拟)某化学实验小组实验结束时,将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,为回收有关金属和盐,同学们设计了如图1实验方案: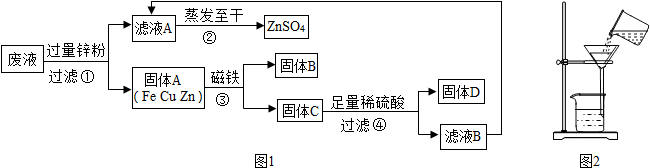
试回答:
(1)步骤①中锌粉必须过量的原因是
(2)写出步骤①中任一反应的化学方程式
(3)检验步骤④中加入的稀硫酸是否足量的方法是
(4)指出如图2的过滤操作的错误
(5)若实验过程中的物质损失忽略,最终所得硫酸锌的质量
查看习题详情和答案>>

试回答:
(1)步骤①中锌粉必须过量的原因是
将废液中的Cu2+和Fe2+全部置换出来
将废液中的Cu2+和Fe2+全部置换出来
;(2)写出步骤①中任一反应的化学方程式
Zn+CuSO4=ZnSO4+Cu或Zn+FeSO4═ZnSO4+Fe
Zn+CuSO4=ZnSO4+Cu或Zn+FeSO4═ZnSO4+Fe
;(3)检验步骤④中加入的稀硫酸是否足量的方法是
继续加入少量稀硫酸,观察是否有气泡产生
继续加入少量稀硫酸,观察是否有气泡产生
;(4)指出如图2的过滤操作的错误
没用玻璃棒引流、滤纸边缘高于漏斗口
没用玻璃棒引流、滤纸边缘高于漏斗口
;在蒸发滤液A的过程中,用玻璃棒不断搅拌的作用使液体均匀受热,防止飞溅
使液体均匀受热,防止飞溅
;(5)若实验过程中的物质损失忽略,最终所得硫酸锌的质量
大于
大于
(填“大于”、“小于”或“等于”)原废液中硫酸锌的质量.要计算该废液中硫酸铜质量,必须要称量固体D或铜
固体D或铜
的质量. (2009?泉港区质检)已知某两种物质在光照条件下能发生化学反应,其微观示意图如下:
(2009?泉港区质检)已知某两种物质在光照条件下能发生化学反应,其微观示意图如下: