摘要:设计实验方案:区分Na2SO4.Na2CO3.BaCl2.稀盐酸四种无色溶液. 作业:
网址:http://m.1010jiajiao.com/timu3_id_107436[举报]
(2013?槐荫区二模)现有某不纯的碳酸钠固体样品,已知其中含有的杂质可能是Na2SO4、CuSO4、NaCl、CaCl2中的一种或几种.为确定其杂质的成分,进行如下实验,出现的现象如图所示(设过程中所有发生的反应都恰好完全进行).
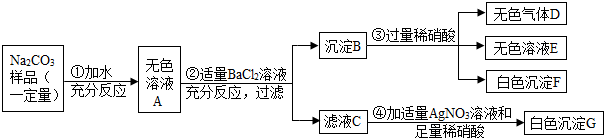
请你根据实验过程和发生的现象做出分析判断,并填写以下空白:
(1)把气体D通入紫色石蕊试液中,观察到的现象是
(2)碳酸钠固体样品中一定含有的杂质是(写化学式)
(3)碳酸钠固体样品中一定不含有的杂质是(写化学式)
(4)请写出过程②中发生反应的一个化学方程式
(5)碳酸钠固体样品中还不能确定的物质是(写化学式)
查看习题详情和答案>>

请你根据实验过程和发生的现象做出分析判断,并填写以下空白:
(1)把气体D通入紫色石蕊试液中,观察到的现象是
石蕊试液变红
石蕊试液变红
.白色沉淀G的化学式是AgCl
AgCl
.(2)碳酸钠固体样品中一定含有的杂质是(写化学式)
Na2CO3
Na2CO3
.(3)碳酸钠固体样品中一定不含有的杂质是(写化学式)
CuSO4
CuSO4
.(4)请写出过程②中发生反应的一个化学方程式
BaCl2+Na2CO3=BaCO3↓+2NaCl
BaCl2+Na2CO3=BaCO3↓+2NaCl
.(5)碳酸钠固体样品中还不能确定的物质是(写化学式)
NaCl
NaCl
,要确定它是否存在,可用溶液A再实验.请简述你的设计方案(说明实验操作步骤、发生的现象及结论):在A溶液中加入适量硝酸钡溶液,然后过滤,向滤液中加入适量硝酸银溶液和稀硝酸,若有白色沉淀,则说明含有氯化钠
在A溶液中加入适量硝酸钡溶液,然后过滤,向滤液中加入适量硝酸银溶液和稀硝酸,若有白色沉淀,则说明含有氯化钠
.(2012?历城区二模)现欲探究一固体混合物的组成,已知其中可能含有Cu、Cu(OH)2、BaCl2、Na2CO3、Na2SO4五种物质中的两种或多种(假设所有可能发生的反应都恰好完全进行),设计实验方案如下:
第一步:取少量的固体样品放入一只烧杯中,加入足量的水充分溶解,过滤,得到无色滤液A和滤渣B.
第二步:将无色滤液A平均分成两份.
(1)向一份中滴加少量无色酚酞试液,得到红色溶液C.
(2)向另一份中滴加适量的Ba(NO3)2溶液,观察到有白色沉淀产生.然后滴加足量的稀硝酸,充分反应后,仍有部分沉淀未溶解.
第三步:向滤渣B中加入过量的稀硫酸,充分反应后过滤,得到蓝色滤液D和滤渣E.
根据以上信息,回答下列问题:
(1)滤渣E的化学式为
(2)滤液D中一定大量存在的阳离子
(3)原固体混合物中一定不含有
(4)若向红色溶液C中滴加澄清石灰水至恰好完全反应,溶液呈
(5)写出向滤液A中加Ba(NO3)2溶液的一个化学方程式
查看习题详情和答案>>
第一步:取少量的固体样品放入一只烧杯中,加入足量的水充分溶解,过滤,得到无色滤液A和滤渣B.
第二步:将无色滤液A平均分成两份.
(1)向一份中滴加少量无色酚酞试液,得到红色溶液C.
(2)向另一份中滴加适量的Ba(NO3)2溶液,观察到有白色沉淀产生.然后滴加足量的稀硝酸,充分反应后,仍有部分沉淀未溶解.
第三步:向滤渣B中加入过量的稀硫酸,充分反应后过滤,得到蓝色滤液D和滤渣E.
根据以上信息,回答下列问题:
(1)滤渣E的化学式为
Cu
Cu
.(2)滤液D中一定大量存在的阳离子
Cu2+
Cu2+
.(写离子符号)(3)原固体混合物中一定不含有
BaCl2
BaCl2
.(4)若向红色溶液C中滴加澄清石灰水至恰好完全反应,溶液呈
浑浊
浑浊
色.并解释原因:碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠
碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠
.(5)写出向滤液A中加Ba(NO3)2溶液的一个化学方程式
Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3
Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3
. (2013?海淀区二模)小明见妈妈买了些取暖袋,他很好奇,打开了一袋,发现里面是黑色的粉末.那么,取暖袋里是什么物质在发生反应、释放热量呢?
(2013?海淀区二模)小明见妈妈买了些取暖袋,他很好奇,打开了一袋,发现里面是黑色的粉末.那么,取暖袋里是什么物质在发生反应、释放热量呢?[查找资料]
①取暖袋由原料层、明胶层、无纺布袋三部分组成.原料层中的黑色粉末的主要成分是铁粉、活性炭、蛭石、可溶性无机盐、吸水性树脂(含水).
②蛭石是当今世界首屈一指的保温材料,起保温作用;吸水性树脂可反复释水、吸水,起吸水、保水的作用;二者均不参加反应.
③使用时应注意:不使用产品时请勿拆开密封包装.
[提出猜想]
①可溶性无机盐可能是氯化钠、硫酸钠、碳酸钠中一种或几种.
②取暖袋发热时,可能是铁粉、氧气、无机盐、水、活性炭几种物质间发生了化学反应.
[实验准备]
用NaCl溶液、Na2SO4溶液、Na2CO3溶液进行如下实验,为确定无机盐的成分提供参考.
| NaCl溶液 | Na2SO4溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 无明显变化 | 无明显变化 | 现象Ⅰ |
| 加入BaCl2溶液 | 无明显变化 | 产生白色沉淀 | 产生白色沉淀 |
| 加入AgNO3溶液 | 产生白色沉淀 | 溶液略呈浑浊 | 产生淡黄色沉淀 |
有气泡冒出
有气泡冒出
.(2)BaCl2溶液与Na2SO4溶液混合发生复分解反应,则白色沉淀的化学式为
BaSO4
BaSO4
.[实验过程]
分别取没有使用的取暖袋和失效后的取暖袋中的黑色粉末完成以下实验,探究无机盐的成分及参加反应的物质.
| 序号 | 加入试剂及操作 | 没有使用的暖袋 | 失效后的暖袋 |
I |
加入足量水观察 | 无色溶液,大量固体在烧杯底部 | 无色溶液,大量固体在烧杯底部 |
| Ⅱ | 取I中上层清液,向其中滴加盐酸 | 无变化 | 无变化 |
| Ⅲ | 取I中上层清液,向其中滴加BaCl2溶液 | 无变化 | 无变化 |
| Ⅳ | 取I中上层清液,向其中滴加AgNO3溶液 | 白色沉淀 | 白色沉淀 |
| Ⅴ | 另取黑色粉末加入足量盐酸 | 大量气泡,溶液呈浅绿色 | 无气泡,溶液呈黄色溶液 |
Fe+2HCl=FeCl2+H2↑
Fe+2HCl=FeCl2+H2↑
.
(4)通过上述实验,可以得出以下结论:
①取暖袋中无机盐的成分是
氯化钠
氯化钠
.②取暖袋发热时,原料层中一定参加反应的物质是
铁粉
铁粉
.(5)利用如图装置,设计实验方案探究氧气是否参加了反应:
在盛有氧气的集气瓶中加入潮湿的铁粉,过一段时间,水被倒吸
在盛有氧气的集气瓶中加入潮湿的铁粉,过一段时间,水被倒吸
,则氧气参加了反应. [反思与评价]
(6)小明根据IV中的现象判定无机盐未参加反应.他的结论是否合理,说明理由:
合理,因为失效以后还有白色沉淀
合理,因为失效以后还有白色沉淀
.