摘要:10.( )现用Na2SO4 .NaCl .NaOH 三种试剂.将NaNO3 溶液中含有的AgNO3 .Ba(NO3)2 .Cu(NO3)2 依次除去.则加入试剂的顺序为 A.NaCl .NaOH .Na2SO4 B.NaOH .Na2SO4 .NaCl C.Na2SO4 .NaCl .NaOH D.NaCl .Na2SO4 .NaOH
网址:http://m.1010jiajiao.com/timu3_id_107224[举报]
氮化铝(AlN)是一种新型无机材料,广泛应用与集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,现用图Ⅰ中的一些装置来进行检验,使氮化铝样品和NaOH溶液反应AlN+NaOH+H2O=NaAlO2+NH3↑,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)
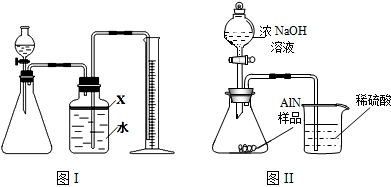
(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为 .
(2)本试验中检查装置气密性的方法是 .
(3)广口瓶中的试剂X可选用 (填选项的标号).A 汽油 B 酒精 C 植物油 D CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将 (填偏大、偏小或不变).
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是 .
(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为 (AlN的相对分子质量为41,每22、4L氨气质量为17g).
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行? (填入“可行”、“不可行”).原因是 ,改进的方法为 .
(8)在mg 20%的氢氧化钠溶液中滴加2~3滴酚酞试液,然后边搅拌边逐滴向其中加入硫酸镁溶液,至溶液的红色完全褪去时,滤去沉淀,称得剩余溶液总质量为3mg.
①计算所加硫酸镁溶液的质量分数;(3分)
②用N表示溶液中离子的数目,不同种离子用离子符号注明[如N (Na')表示钠离子的数目],请建立坐标系,绘制上述滴加过程中各种离子的数目随溶液的不断加入而变化的关系图.(3分) 查看习题详情和答案>>

(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为
(2)本试验中检查装置气密性的方法是
(3)广口瓶中的试剂X可选用
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?
(8)在mg 20%的氢氧化钠溶液中滴加2~3滴酚酞试液,然后边搅拌边逐滴向其中加入硫酸镁溶液,至溶液的红色完全褪去时,滤去沉淀,称得剩余溶液总质量为3mg.
①计算所加硫酸镁溶液的质量分数;(3分)
②用N表示溶液中离子的数目,不同种离子用离子符号注明[如N (Na')表示钠离子的数目],请建立坐标系,绘制上述滴加过程中各种离子的数目随溶液的不断加入而变化的关系图.(3分) 查看习题详情和答案>>
 22、已知Fe(OH)2在潮湿的空气中氧化成Fe(OH)3
22、已知Fe(OH)2在潮湿的空气中氧化成Fe(OH)3(1)该反应的化学方程式为
4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(2)现用下面两种方法制白色的Fe(OH)2沉淀.
方法一:用FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备.
①除去蒸馏水中溶解的O2常采用的方法是
煮沸
:②生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,伸到FeSO4溶液液面
下
(填“上”或“下”),再挤出NaOH溶液,这样操作的理由是避免Fe(OH)2与空气中的氧气接触而被氧化.方法二:在如图装置中,用NaOH溶液,铁屑,稀硫酸制备.
(3)制备Fe(OH)2的原理是
Fe+H2SO4=FeSO4+H2↑
、FeSO4+2NaOH=Fe(OH)2↓+Na2SO4
(用化学方程式表示).(4)在试管 I里加入的试剂是
铁屑和稀H2SO4
.(5)为了使生成的Fe(OH)2沉淀能较长时间保持白色,在试管 I和试管 II中加入试剂,塞紧塞子后,打开止水夹,当观察到试管 I里出现
大量气泡产生
现象时,应在a处进行的实验是验纯
(填实验名称).10、A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠和盐酸四种无色溶液中的一种,现用一种无色溶液X把A、B、C、D一一鉴别了出来,已知X是含有镁元素的化合物,鉴别方法见下图所示.(所加溶液均过量,使反应完全)

完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):A
(2)写出下列有关反应的化学方程式:
X和B:
X和D:
查看习题详情和答案>>

完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):A
HCl
,BBa(NO3)2
,CNaCl
,DNaOH
,XMgSO4
.(2)写出下列有关反应的化学方程式:
X和B:
MgSO4+Ba(NO3)2═Mg(NO3)2+BaSO4↓
.X和D:
MgSO4+2NaOH═Na2SO4+Mg(OH)2↓
.10、A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠和盐酸四种无色溶液中的一种,现用一种无色溶液X把A、B、C、D一一鉴别了出来,已知X是含有镁元素的化合物.鉴别方法见下图所示.(所加溶液均过量,使反应完全)

完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):
A
(2)写出下列有关反应的化学方程式:
X和B:
X和D:
查看习题详情和答案>>

完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):
A
HCl
,BBa(NO3)2
,CNaCl
,DNaOH
,XMgSO4
.(2)写出下列有关反应的化学方程式:
X和B:
MgSO4+Ba(NO3)2═Mg(NO3)2+BaSO4↓
.X和D:
MgSO4+2NaOH═Na2SO4+Mg(OH)2↓
. 22、实验室常用亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取SO2,常温下SO2是无色有刺激性气味的气体,它的密度比空气大,可溶于水生成亚硫酸(H2SO3),H2SO3能使湿润的PH试纸变红,请回答:
22、实验室常用亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取SO2,常温下SO2是无色有刺激性气味的气体,它的密度比空气大,可溶于水生成亚硫酸(H2SO3),H2SO3能使湿润的PH试纸变红,请回答:(1)写出上述装置中①、②的仪器名称 ①
铁架台
;②锥形瓶
;(2)现用亚硫酸钠与稀硫酸制取二氧化硫,你选择的反应发生装置是
B
(填代码);化学方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
;不选择另一种反应发生装置的理由是①
固体和液体反应
;②反应在常温下能够发生
;(3)当用装置C收集SO2时,导气管的下端应放在
b
(填a或b)处,其目的是使收集的气体更纯
;(4)写出检验装置C中SO2是否已收集满的 操作方法是:
把湿润的PH试纸放在集气瓶口
.