摘要:14.某金属放入稀盐酸中.不产生气泡.该金属可能是 A.Mg B.Zn C.Fe D.Ag
网址:http://m.1010jiajiao.com/timu3_id_106063[举报]
28、已知某金属粉末中可能含有铁、铝、铜三种金属中的两种或三种,化学小组的同学对该粉末进行探究.
【提出猜想】
猜想一:该粉末由铜、铝组成; 猜想二:该粉末由铁、铝组成;
猜想三:该粉末由铁、铝、铜组成; 猜想四:该粉末由
【查阅资料】铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气,反应的化学方程式为2Al+2H2O+2NaOH=2NaAlO2+3H2↑,铁和铜与氢氧化钠溶液均不发生反应.
【供选药品】稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液、澄清石灰水、蒸馏水.
【进行实验】
【反思与评价】若将原粉末中的铜全部回收,请写出实验过程
查看习题详情和答案>>
【提出猜想】
猜想一:该粉末由铜、铝组成; 猜想二:该粉末由铁、铝组成;
猜想三:该粉末由铁、铝、铜组成; 猜想四:该粉末由
铁和铜
组成.【查阅资料】铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气,反应的化学方程式为2Al+2H2O+2NaOH=2NaAlO2+3H2↑,铁和铜与氢氧化钠溶液均不发生反应.
【供选药品】稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液、澄清石灰水、蒸馏水.
【进行实验】
| 实验目的 | 实验操作 | 实验现象 | 实验结论 |
| 证明粉末中是否含有 铝 |
取一个小烧杯,加入适量的粉末,再向其中加入足量的 氢氧化钠溶液 |
无明显变化 |
猜想四成立; 实验中发生反应 的化学方程式为 Fe+2HCl=FeCl2+H2↑ |
| 证明粉末中是否含有 铁、铜 |
过滤,将得到的固体洗涤后放入小烧杯,再向其中加入足量的稀盐酸 | ①有气泡产生 ②固体未完全溶解 |
向粉末中加入过量的稀盐酸(或硫酸铜溶液),充分反应后过滤,再将固体洗涤干燥.
.(2013?江宁区二模)某金属冶炼厂的管道烟泥中含有炭黑及金属铜、锌、硫.综合实践活动小组的同学设计了从管道烟泥中回收金属铜并利用废气中的二氧化硫制备硫酸的实验方案,实验过程如图所示:
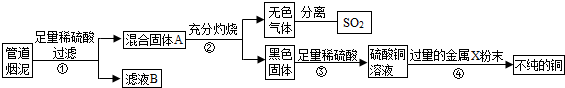
请回答:
(1)步骤①中,过滤操作使用了玻璃棒,其作用是
(2)步骤④中,所加入的金属X与Zn的活动性顺序是Zn>X,金属X具有广泛用途,X是
(3)除去不纯铜中的杂质金属X,可选用的试剂或用品有
a.磁铁 b.稀盐酸 c.蒸馏水 d.氯化铜溶液.
(4)将分离出的SO2通过下列碘循环工艺过程既能制H2SO4,又能制取H2,其流程如下:
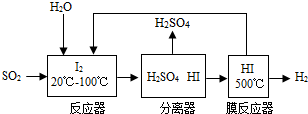
试写出反应器、膜反应器中的化学反应方程式
查看习题详情和答案>>

请回答:
(1)步骤①中,过滤操作使用了玻璃棒,其作用是
引流
引流
;如何确定硫酸已经过量取少量滤液放入试管内,向试管内加入锌粒,如果有气泡产生,说明加入的硫酸是过量的,如果没有气泡产生,说明硫酸没有过量
取少量滤液放入试管内,向试管内加入锌粒,如果有气泡产生,说明加入的硫酸是过量的,如果没有气泡产生,说明硫酸没有过量
.(2)步骤④中,所加入的金属X与Zn的活动性顺序是Zn>X,金属X具有广泛用途,X是
Fe
Fe
,有关反应的化学方程式CuSO4+Fe═Cu+FeSO4
CuSO4+Fe═Cu+FeSO4
.(3)除去不纯铜中的杂质金属X,可选用的试剂或用品有
abd
abd
(填标号).a.磁铁 b.稀盐酸 c.蒸馏水 d.氯化铜溶液.
(4)将分离出的SO2通过下列碘循环工艺过程既能制H2SO4,又能制取H2,其流程如下:

试写出反应器、膜反应器中的化学反应方程式
SO2+2H2O+I2═H2SO4+2HI
SO2+2H2O+I2═H2SO4+2HI
、2HI
H2+I2
| ||
2HI
H2+I2
.
| ||