摘要:11.我国煤炭资源十分丰富.至今煤仍是我国工业和民用的主要燃料.煤的大量燃烧使我国大部分地区的空气质量严重下降.给农业生产及人民健康造成极大危害.你认为煤燃烧产生的造成大气污染的主要物质是 . . 和 .
网址:http://m.1010jiajiao.com/timu3_id_102957[举报]
我国海洋资源十分丰富,请根据所学知识完成下列过程:
(1)海水晒盐可得到粗盐和苦卤,利用苦卤.石灰乳.稀盐酸可制得应用于飞机制造业的金属
镁.其中发生反应的化学方程式是
①
②
③
(2)为了除去粗盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如下图所示的①至⑤步除杂方案:
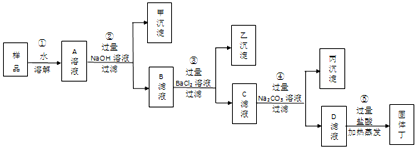
请根据上述除杂方案,回答下列问题:
①沉淀甲是
②假设整个操作过程中物质转化无损失,则固体丁中NaCl的质量比原样品中NaCl的质量
查看习题详情和答案>>
(1)海水晒盐可得到粗盐和苦卤,利用苦卤.石灰乳.稀盐酸可制得应用于飞机制造业的金属
镁.其中发生反应的化学方程式是
①
MgCl2﹢Ca(OH)2=Mg(OH)2↓﹢CaCl2
MgCl2﹢Ca(OH)2=Mg(OH)2↓﹢CaCl2
;②
Mg(OH)2﹢2HCl=MgCl2﹢2H2O
Mg(OH)2﹢2HCl=MgCl2﹢2H2O
;③
MgCl2
Mg﹢Cl2↑
| ||
MgCl2
Mg﹢Cl2↑
.
| ||
(2)为了除去粗盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如下图所示的①至⑤步除杂方案:

请根据上述除杂方案,回答下列问题:
①沉淀甲是
氢氧化镁[或Mg(OH)2]
氢氧化镁[或Mg(OH)2]
;滤液C中的溶质是氯化钠、氢氧化钠、氯化钡(或NaCl、NaOH、BaCl2)
氯化钠、氢氧化钠、氯化钡(或NaCl、NaOH、BaCl2)
;操作⑤中加入过量盐酸的作用是除去滤液D中的NaOH和Na2CO3
除去滤液D中的NaOH和Na2CO3
.②假设整个操作过程中物质转化无损失,则固体丁中NaCl的质量比原样品中NaCl的质量
增大
增大
(填增大、不变或减小);若在操作②中改为加过量的KOH溶液,固体丁中可能含有的杂质是氯化钾(或KCl)
氯化钾(或KCl)
.我国海洋资源十分丰富,请根据所学知识完成下列过程:
⑴海水晒盐可得到粗盐和苦卤,利用苦卤.石灰乳.稀盐酸可制得应用于飞机制造业的金属
镁。其中发生反应的化学方程式是
① ![]() ;
;
② ;
③ 。
(2)为了除去粗盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如下图所示的①至⑤步除杂方案:

请根据上述除杂方案,回答下列问题:
①沉淀甲是 ;滤液C中的溶质是 ;
操作⑤中加入过量盐酸的作用是 。
②假设整个操作过程中物质转化无损失,则固体丁中NaCl的质量比原样品中NaCl的质量 (填增大、不变或减小);若在操作②中改为加过量的KOH溶液,固体丁中可能含有的杂质是 。
查看习题详情和答案>> 28、我国海洋资源十分丰富.随着科学技术的不断发展,不仅可以通过高分子材料来淡化海水,还可以从海水中提取食盐、金属镁等重要的化学物质.
28、我国海洋资源十分丰富.随着科学技术的不断发展,不仅可以通过高分子材料来淡化海水,还可以从海水中提取食盐、金属镁等重要的化学物质.(1)海水晒盐所获得的粗盐中含有难溶性杂质和MgCl2、CaCl2、KCl等可溶性杂质.在实验室中粗盐经过溶解、
过滤
、蒸发
可得到初步提纯.(2)如图是MgCl2、KCl和MgSO4三种物质的溶解度曲线示意图.
①设t1℃时MgCl2、KCl和MgSO4三种物质的溶解度分别为a、b、c,则它们的大小关系为
a>b=c
.②t2℃时,MgCl2、KCl两物质的饱和溶液中溶质质量分数较大的是
MgCl2
.(3)目前世界上60%的镁是从海水中提取的.其主要步骤如下:
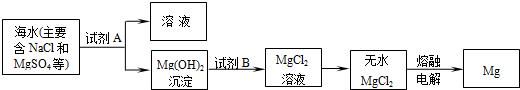
①电解熔融氯化镁的过程中,
电
能转化为化学
能.②提取Mg的过程中,试剂A可以选用
氢氧化钠溶液
,试剂B选用稀盐酸
.③分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中按照下图所示步骤进行实验即可.请将相关内容填写在图中相应的空格中.
