摘要:36.指出下图中仪器的名称 (1)A B C (2)瓶中盛有红棕色的气体.向其中投入几块活性炭.会有何现象 . .
网址:http://m.1010jiajiao.com/timu3_id_100951[举报]
下图是实验室中用于制取和收集气体的装置图.

请回答:
(1)写出编号①、②、③仪器的名称①
(2)以上装置图中有一处明显的错误,请指出错误.
(3)实验室制取二氧化碳的发生装置应选用
(4)若在实验室用加热高锰酸钾的方法制取氧气,发生装置应选用
(5)若用双氧水制氧气,其反应的文字表达式为
(6)用以上所示装置F来测量生成CO2气体的体积,其中在水面上放一层植物油的目的是
(7)由此我们得到启示实验室选择气体发生装置时,应考虑
查看习题详情和答案>>

请回答:
(1)写出编号①、②、③仪器的名称①
酒精灯
酒精灯
②试管
试管
③集气瓶
集气瓶
.(2)以上装置图中有一处明显的错误,请指出错误.
D中的导管太短
D中的导管太短
(3)实验室制取二氧化碳的发生装置应选用
B
B
(填序号,下同),其反应的文字表达式为碳酸钙+盐酸→氯化钙+水+二氧化碳
碳酸钙+盐酸→氯化钙+水+二氧化碳
;收集装置应选用E
E
;(4)若在实验室用加热高锰酸钾的方法制取氧气,发生装置应选用
A
A
,该装置缺少棉花团
棉花团
,实验结束时先将导管移出水面,再熄灭酒精灯的目的是防止水倒流而炸裂试管
水倒流而炸裂试管
.收集装置可选用C或E
C或E
.如用D装置收集,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了
将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了
(5)若用双氧水制氧气,其反应的文字表达式为
过氧化氢
水+氧气
| 催化剂 |
过氧化氢
水+氧气
,该反应会| 催化剂 |
放出
放出
热量(放出或吸收).如用G来收集氧气,氧气从a
a
(a或b)通入,如果G中装满水来收集氧气,氧气又该从b
b
(a或b)通入.(6)用以上所示装置F来测量生成CO2气体的体积,其中在水面上放一层植物油的目的是
防止二氧化碳溶于水
防止二氧化碳溶于水
并与水反应
并与水反应
,植物油上方原有的空气对实验结果无
无
(有或无)影响.(7)由此我们得到启示实验室选择气体发生装置时,应考虑
反应物的状态
反应物的状态
和反应的条件
反应的条件
.下图是实验室用高锰酸钾制取氧气的实验装置图,请回答:

(1)指出编号仪器名称:
A
写出该反应的文字表达式:
(2)在试管口处放一小团棉花其作用是
等集气瓶内的水完全排出后,用玻璃片盖住瓶口,把集气瓶小心移出水槽后,集气瓶应
查看习题详情和答案>>

(1)指出编号仪器名称:
A
酒精灯
酒精灯
B试管
试管
C集气瓶
集气瓶
D水槽
水槽
E铁架台
铁架台
写出该反应的文字表达式:
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
(2)在试管口处放一小团棉花其作用是
防止加热时高锰酸钾粉末进入导管
防止加热时高锰酸钾粉末进入导管
加热反应物,开始收集氧气的适宜时刻是导管口气泡连续、均匀冒出时收集
导管口气泡连续、均匀冒出时收集
.等集气瓶内的水完全排出后,用玻璃片盖住瓶口,把集气瓶小心移出水槽后,集气瓶应
正放在桌面上
正放在桌面上
,是因为氧气的密度比空气大
氧气的密度比空气大
.停止加热时,先把导管从水槽中取出
导管从水槽中取出
,然后熄灭酒精灯
熄灭酒精灯
,其原因是防止水倒吸入试管,引起试管炸裂
防止水倒吸入试管,引起试管炸裂
.下图是实验室常用的实验仪器与装置.依据题目要求回答下列问题:
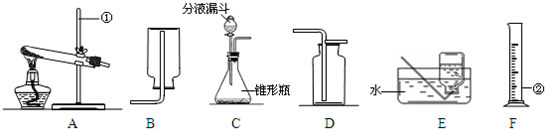
(1)写出标号仪器的名称 ①
(2)实验制取氧气常采用分解过氧化氢溶液的方法,选择的发生装置为
①产物无污染 ②不需加热 ③需加热 ④生成物只有氧气
(3)乙同学用大理石和稀盐酸反应来制取二氧化碳,其反应的文字表达式为
(4)某化学兴趣小组的同学,利用下列仪器进行实验(所有装置的气密性都已检查完毕)
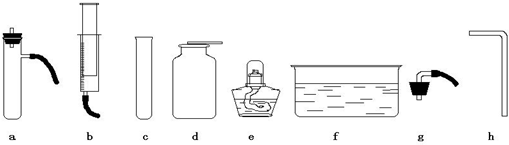
①把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并用排气法收集氧气,完成该实验你所选用的仪器有
写出发生反应的化学符号表达式
②某同学继续探究“红砖粉末是否也可以作过氧化氢分解反应的催化剂?”实验步骤和现象如下:
a、他分别向两支试管中加入相同的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
b、将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
c、用称量后的固体重复步骤a的实验,现象与步骤a完全相同.
试回答:步骤a中他除了选用试管外还用到上面列出的仪器有
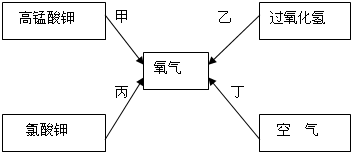
(5)在学习中我们了解到常用制取氧气的方法有如图所示的四种:
请回答问题:在实验室按绿色化学的要求你认为那种制取氧气的方法较好的是
查看习题详情和答案>>

(1)写出标号仪器的名称 ①
铁架台
铁架台
; ②量筒
量筒
.(2)实验制取氧气常采用分解过氧化氢溶液的方法,选择的发生装置为
C
C
,理由是在常温下,过氧化氢在二氧化锰做催化剂的条件下就能反应
在常温下,过氧化氢在二氧化锰做催化剂的条件下就能反应
该方法制氧气有许多优点,如:①②
①②
(填序号).①产物无污染 ②不需加热 ③需加热 ④生成物只有氧气
(3)乙同学用大理石和稀盐酸反应来制取二氧化碳,其反应的文字表达式为
碳酸钙+盐酸→氯化钙+水+二氧化碳
碳酸钙+盐酸→氯化钙+水+二氧化碳
_,制取并收集二氧化碳应分别选择C、D
C、D
装置(填字母);收集气体后如何检验集气瓶中的二氧化碳是否已经收集满?将一根带燃烧的木条平放在集气瓶口,木条熄灭,证明满了
将一根带燃烧的木条平放在集气瓶口,木条熄灭,证明满了
.(4)某化学兴趣小组的同学,利用下列仪器进行实验(所有装置的气密性都已检查完毕)

①把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并用排气法收集氧气,完成该实验你所选用的仪器有
abdh
abdh
(填字母).写出发生反应的化学符号表达式
H2O2
H2O+O2
| MnO2 |
H2O2
H2O+O2
.这种方法与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比有| MnO2 |
可以控制反应的进行,节约药品
可以控制反应的进行,节约药品
的优点.②某同学继续探究“红砖粉末是否也可以作过氧化氢分解反应的催化剂?”实验步骤和现象如下:
a、他分别向两支试管中加入相同的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
b、将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
c、用称量后的固体重复步骤a的实验,现象与步骤a完全相同.
试回答:步骤a中他除了选用试管外还用到上面列出的仪器有
ghf
ghf
(填字母).步骤c的实验目的是检验红砖粉的化学性质在反应前后是否有变化
检验红砖粉的化学性质在反应前后是否有变化
.该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来反应前没有称出红砖粉的质量
反应前没有称出红砖粉的质量
.(5)在学习中我们了解到常用制取氧气的方法有如图所示的四种:
请回答问题:在实验室按绿色化学的要求你认为那种制取氧气的方法较好的是
乙
乙
方法.(填“甲、乙、丙、丁”)写出甲方法制取氧气的化学符号表达式KMnO4
K2MnO4+MnO2+O2↑
| △ |
KMnO4
K2MnO4+MnO2+O2↑
| △ |

下图是实验室制取气体的一些装置,据图1回答有关问题.(以下所选装置均填装置序号)
(1)写出指定仪器的名称:①
(2)C装置中试管口略向下倾斜的原因是
(3)收集二氧化碳的收集装置
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是

查看习题详情和答案>>
(1)写出指定仪器的名称:①
试管
试管
;②集气瓶
集气瓶
;(2)C装置中试管口略向下倾斜的原因是
防止加热时冷凝水倒流引起试管炸裂
防止加热时冷凝水倒流引起试管炸裂
;(3)收集二氧化碳的收集装置
E
E
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是
A
A
;如果用图2所示装置收集乙炔,气体应从b
b
(填“a”或“b”)端管口通人.


