题目内容
(20分)在一个带活塞的圆筒内装配着著名的托里拆利装置。在水银柱上方有氢气,在圆筒内有空气。第一步,水银柱高度h1=70cm,空气压强pk1=1.314atm=133.4kPa=100cmHg,温度为00C=273K。第二步,向上提升活塞,直至水银柱高度降为h2=40cm,这时空气压强为pk2=0.79atm=80kPa=60cmHg。第三步,保持体积不变,提高温度到T3,此时水银柱的高度为h3=50cm。最后,第四步,温度为T4,水银柱的高度为h4=45cm,空气压强没有改变。求出最后一步中氢气的温度和压强。
解析:我们将空气和氢气的数据列成表。两者温度是相同的。玻璃管的长度用L表示。为了简单起见,我们以装有氢气的管子长度的厘米数来度量氢气的体积。压强全部用cmHg为单位给出(见图2第一步至第四步)。

从第一步到第二步,对氢气应用玻意耳定律:(L-70)(100-70)=(L-40)(60-40)
由此式求得玻璃管的长度L=130cm,
因此,氢气在第一步至第四步中体积分别为:V h1=60cm,V h2=90cm,V h3=80cm,V h4=85cm
从第二步到第三步,氢气的状态方程为:![]()
对空气应用盖吕萨克定律:![]()
从第三步到第四步,我们只有向上提升活塞,以便使空气压强保持不变。氢气的状态方程为:![]()
解以上方程组,得:pk3=pk4=80cmHg, T3=364K, T4=451K,
所以氢气的压强为:ph3=30cmHg ph4=35cmHg
算出空气的体积比为:V k1:V k2:V k4=6:10:12.4
(注:cmHg为实用单位,应转换成国际单位Pa)

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目
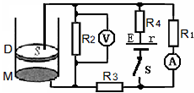 (2011?静安区二模)如图,一质量不计,可上下自由移动的活塞将理想气体封闭在圆筒内,筒的侧壁为绝缘体,下底M及活塞D均为导体并按图连接,活塞面积S=2cm2.闭合电键前,DM间距l1=5μm,闭合电键后,活塞D与下底M分别带有等量异种电荷,并各自产生匀强电场(D与M间的电场为各自产生的电场的叠加).在电场力作用下活塞D发生移动.稳定后,DM间距l2=4μm,此时安培表读数为0.75A,伏特表读数为2V.
(2011?静安区二模)如图,一质量不计,可上下自由移动的活塞将理想气体封闭在圆筒内,筒的侧壁为绝缘体,下底M及活塞D均为导体并按图连接,活塞面积S=2cm2.闭合电键前,DM间距l1=5μm,闭合电键后,活塞D与下底M分别带有等量异种电荷,并各自产生匀强电场(D与M间的电场为各自产生的电场的叠加).在电场力作用下活塞D发生移动.稳定后,DM间距l2=4μm,此时安培表读数为0.75A,伏特表读数为2V.
 ,活塞移动前后气体温度不变) ;
,活塞移动前后气体温度不变) ;